某温度下,在一个2 L的密闭容器中加入4 mol A和2 mol B进行如下反应:3A(g)+2B(g) 4C(s)+D(g),反应2 min后达到平衡,测得生成1.6 mol C,下列说法正确的是( )
4C(s)+D(g),反应2 min后达到平衡,测得生成1.6 mol C,下列说法正确的是( )
 4C(s)+D(g),反应2 min后达到平衡,测得生成1.6 mol C,下列说法正确的是( )
4C(s)+D(g),反应2 min后达到平衡,测得生成1.6 mol C,下列说法正确的是( )| A.前2 min D的平均反应速率为0.2 mol·L-1·min-1 |
| B.此时,B的平衡转化率是40% |
| C.增大该体系的压强,平衡不移动,化学平衡常数不变 |
| D.增加B,平衡向右移动,B的平衡转化率增大 |
13-14高三·全国·课时练习 查看更多[7]
北京市第三十一中学2021-2022学年高二上学期期中考试化学试题广东省东莞市七校2020-2021学年高二上学期联考化学试题(已下线)2.3.3+化学平衡常数-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)广东省深圳市科学高中2018-2019学年第一学期高二入学考试化学试题2017届河北省沧州一中高三上学期9.22周测化学卷(已下线)2014年高考化学一轮复习课后规范训练7-3练习卷吉林省辽源市第五中学2016-2017学年高一下学期第二次月考化学试题
更新时间:2020-09-24 10:34:32
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列描述正确的是

A.反应开始到10 s,用X表示的反应速率为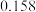 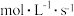 |
B.反应开始到10 s,Y的物质的量浓度减少了  |
C.反应10s时达到化学平衡状态,Z的平衡浓度为  |
D.反应的化学方程式为 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】向某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图甲所示[0~t1阶段c(B)未画出]。图乙中四个阶段各改变一种不同的条件。已知,t3~t4阶段为使用催化剂。下列说法错误的是
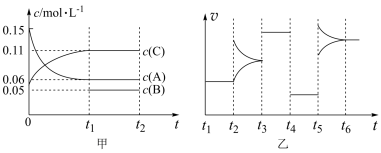

| A.若t1=15s,则在0-t1时间段用C表示的化学反应速率为0.004mol.L-1.s-1 |
| B.B的起始物质的量为0.02mol |
| C.t5~t6阶段改变的条件可能是升高温度 |
| D.t1~t2阶段的K等于t3~t4阶段的K |
您最近半年使用:0次
【推荐1】氮及其化合物在生产生活中具有广泛应用。氮气经过一系列的变化可以合成氨、氮的氧化物、硝酸等重要的化工原料;NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,减少环境污染。对于反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g)∆H<0,下列有关说法不正确的是
4NO(g)+6H2O(g)∆H<0,下列有关说法不正确的是
 4NO(g)+6H2O(g)∆H<0,下列有关说法不正确的是
4NO(g)+6H2O(g)∆H<0,下列有关说法不正确的是| A.升高温度,该反应的平衡常数增大 |
| B.催化剂降低了正、逆反应的活化能 |
| C.1molN-H断裂同时有1molO-H断裂,说明达该条件下的平衡状态 |
| D.其它条件不变,加入高效的催化剂能提高单位体积内的活化分子百分数 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】在一定体积的密闭容器中,进行化学反应:CO2(g)+H2(g)  CO(g)+H2O(g),化学平衡常数K和温度的关系如下表所示:根据以上信息推断以下说法正确的是
CO(g)+H2O(g),化学平衡常数K和温度的关系如下表所示:根据以上信息推断以下说法正确的是
 CO(g)+H2O(g),化学平衡常数K和温度的关系如下表所示:根据以上信息推断以下说法正确的是
CO(g)+H2O(g),化学平衡常数K和温度的关系如下表所示:根据以上信息推断以下说法正确的是| T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
| A.此反应为放热反应 |
B.各物质的平衡浓度符合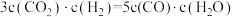 时,此时的温度为1000℃ 时,此时的温度为1000℃ |
| C.该反应的化学平衡常数越大,反应正向进行的程度越大 |
| D.若 1200℃时,某时刻体系中 CO2、H2、CO、H2O 的浓度(mol·L- 1)分别为2、2、4、4,则此时上述反应向正反应方向进行 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
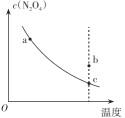
【推荐1】如图所示的曲线是恒容密闭容器中充入一定量N2O4,其他条件一定时,反应N2O4 2NO2 △H>0中N2O4,的平衡浓度与温度的关系曲线,下列有关说法正确的是
2NO2 △H>0中N2O4,的平衡浓度与温度的关系曲线,下列有关说法正确的是
 2NO2 △H>0中N2O4,的平衡浓度与温度的关系曲线,下列有关说法正确的是
2NO2 △H>0中N2O4,的平衡浓度与温度的关系曲线,下列有关说法正确的是
| A.逆反应速率:c点<a点 | B.b点所处状态的v(正)>v(逆) |
| C.N2O4的转化率:c点<a点 | D.化学平衡常数:b点>c点 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】一定条件下,在体积为10L的密闭容器中,1molA和1molB进行反应:2A(g)+B(g) 2C(g),达到平衡时生成0.6molC。下列说法正确的是( )
2C(g),达到平衡时生成0.6molC。下列说法正确的是( )
 2C(g),达到平衡时生成0.6molC。下列说法正确的是( )
2C(g),达到平衡时生成0.6molC。下列说法正确的是( )| A.当容器内密度保持不变时,可以判断反应已达到平衡 |
| B.其他条件不变,将容器体积变为5L,C的平衡浓度变为原来的2倍 |
| C.达到平衡时,C的体积百分含量为0.353 |
| D.其他条件不变,若增大压强,则物质A的转化率减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】如图,甲是由导热材料制成的刚性密闭容器,乙是一耐化学腐蚀且易于传热的气球,关闭 ,将等量且少量的NO2通过
,将等量且少量的NO2通过 、
、 分别充入甲乙中。反应起始时,甲、乙的体积相同,并发生如下反应:2NO2(g)
分别充入甲乙中。反应起始时,甲、乙的体积相同,并发生如下反应:2NO2(g) N2O4(g),甲、乙装置分别反应达到平衡后,下列说法不正确的是
N2O4(g),甲、乙装置分别反应达到平衡后,下列说法不正确的是

 ,将等量且少量的NO2通过
,将等量且少量的NO2通过 、
、 分别充入甲乙中。反应起始时,甲、乙的体积相同,并发生如下反应:2NO2(g)
分别充入甲乙中。反应起始时,甲、乙的体积相同,并发生如下反应:2NO2(g) N2O4(g),甲、乙装置分别反应达到平衡后,下列说法不正确的是
N2O4(g),甲、乙装置分别反应达到平衡后,下列说法不正确的是
| A.甲、乙中生成的N2O4的速率是v甲<v乙 |
| B.若打开活塞K2,气球乙将变大 |
| C.若向甲容器中再充入与初始量相等的NO2,则再次平衡时甲中NO2的转化率将增大 |
| D.若向甲容器中再充入等量的氖气,则再次平衡时甲中NO2的转化率将不变 |
您最近半年使用:0次

 2C(g),若经2s后测得C的浓度为0.6mol·L-1,现有下列几种说法,其中正确的是
2C(g),若经2s后测得C的浓度为0.6mol·L-1,现有下列几种说法,其中正确的是 催化加氢合成甲醇技术是有效利用
催化加氢合成甲醇技术是有效利用
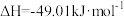 。下列有关说法正确的是
。下列有关说法正确的是 的产量
的产量 的平衡转化率
的平衡转化率

