某温度时,水的离子积Kw=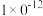 。
。
(1)将此温度下 的NaOH溶液与
的NaOH溶液与 的盐酸等体积混合(设混合后溶液体积的变化忽略不计,下同),混合后溶液的
的盐酸等体积混合(设混合后溶液体积的变化忽略不计,下同),混合后溶液的
________________________ 。
(2)将此温度下 的NaOH溶液
的NaOH溶液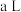 与
与 的稀硫酸
的稀硫酸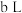 混合。
混合。
①若所得的混合溶液呈中性,则a:b=________________________ 。
②若所得的混合溶液 ,则a:b=
,则a:b=________________________ 。
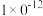 。
。(1)将此温度下
 的NaOH溶液与
的NaOH溶液与 的盐酸等体积混合(设混合后溶液体积的变化忽略不计,下同),混合后溶液的
的盐酸等体积混合(设混合后溶液体积的变化忽略不计,下同),混合后溶液的
(2)将此温度下
 的NaOH溶液
的NaOH溶液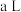 与
与 的稀硫酸
的稀硫酸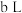 混合。
混合。①若所得的混合溶液呈中性,则a:b=
②若所得的混合溶液
 ,则a:b=
,则a:b=
更新时间:2020/10/06 12:16:38
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】Ⅰ.某温度(t℃)时,水的Kw=10-13,则该温度(填 “大于”“小于”或“等于”)______ 25℃,理由是_________ ,将此温度下pH =11的NaOH溶液aL与pH=1的H2SO4溶液bL混合,
(1)若所得混合液为中性,则a∶b=_________ ;
(2)若所得混合液的pH=2,则a∶b=_________ 。
Ⅱ.25℃时,0.1mol·L-1的某一元酸HA在水中有0.1%发生电离,下列说法不正确的是___________
A.该溶液pH=4 B.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
C.此酸的电离平衡常数约为1×10-7 D.升高温度,溶液的pH增大
(1)若所得混合液为中性,则a∶b=
(2)若所得混合液的pH=2,则a∶b=
Ⅱ.25℃时,0.1mol·L-1的某一元酸HA在水中有0.1%发生电离,下列说法不正确的是
A.该溶液pH=4 B.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
C.此酸的电离平衡常数约为1×10-7 D.升高温度,溶液的pH增大
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1) 时,
时, 的盐酸中由水电离出的
的盐酸中由水电离出的 为
为___________ mol·L-1。
(2) 时,向
时,向 的蒸馏水中加入
的蒸馏水中加入 晶体,保持温度不变,测得溶液的
晶体,保持温度不变,测得溶液的 。此时水的离子积
。此时水的离子积
___________ ,溶液中 为
为___________ mol·L-1。
(3) 时,
时,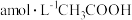 溶液的
溶液的 ,用含a和b的代数式表示
,用含a和b的代数式表示 的电离平衡常数
的电离平衡常数
___________ 。
(1)
 时,
时, 的盐酸中由水电离出的
的盐酸中由水电离出的 为
为(2)
 时,向
时,向 的蒸馏水中加入
的蒸馏水中加入 晶体,保持温度不变,测得溶液的
晶体,保持温度不变,测得溶液的 。此时水的离子积
。此时水的离子积
 为
为(3)
 时,
时,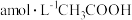 溶液的
溶液的 ,用含a和b的代数式表示
,用含a和b的代数式表示 的电离平衡常数
的电离平衡常数
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)在25°C时,纯水中C(H+)·C(OH-)=_________________ ;
(2)在NH4Cl溶液中C(H+)______ 10-7mol/L(大于、小于或等于),pH______ 7(大于、小于或等于);
(3)在Na2CO3溶液中C(H+)______ 10-7mol/L (大于、小于或等于),pH______ 7(大于、小于或等于)
(4)在NaCl溶液中C(H+)______ 10-7mol/L (大于、小于或等于),pH______ 7(大于、小于或等于).
(2)在NH4Cl溶液中C(H+)
(3)在Na2CO3溶液中C(H+)
(4)在NaCl溶液中C(H+)
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐1】已知水在25℃和95℃时,水电离平衡曲线如图所示:

(1)则95℃时,水的电离平衡曲线应为B,请说明理由______________________ .
25℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,所得混合溶液的pH=7,则NaOH溶液与硫酸溶液的体积比为______________ 。
(2)95℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是______________ .
(3)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程度分别用α1、α2表示,则α1______________ α2(填“大于”、“小于”、“等于”或“无法确定”)。
(4)曲线B对应温度下,将0.02mol/LBa(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合后,混合溶液的pH=________________ 。

(1)则95℃时,水的电离平衡曲线应为B,请说明理由
25℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,所得混合溶液的pH=7,则NaOH溶液与硫酸溶液的体积比为
(2)95℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是
(3)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程度分别用α1、α2表示,则α1
(4)曲线B对应温度下,将0.02mol/LBa(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合后,混合溶液的pH=
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题
(1)常温下,0.05mol/L硫酸溶液中,
___________ mol/L,pH值为___________ ,水电离的
___________ mol/L;25℃ 的盐酸中,由水电离产生的
的盐酸中,由水电离产生的 的物质的量浓度为
的物质的量浓度为___________ 。
(2)氨水和稀盐酸反应后的溶液呈中性,所得溶液中的离子浓度大小关系是___________ 。
(3)某温度(t℃)时,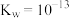 ,则该温度(填大于、等于或小于)
,则该温度(填大于、等于或小于)___________ 25℃,理由是___________ 。将此温度下pH=11的NaOH溶液a L与pH=l的 溶液b L混合,若所得混合溶液为中性,则a:b=
溶液b L混合,若所得混合溶液为中性,则a:b=___________ ;
(4)已知 的
的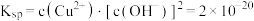 。当溶液中各种离子的浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。则①某
。当溶液中各种离子的浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。则①某 溶液里
溶液里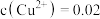 mol/L,如要生成
mol/L,如要生成 沉淀,应调整溶液的pH大于
沉淀,应调整溶液的pH大于___________ 。
②要使0.2
 溶液中
溶液中 沉淀较为完全(使
沉淀较为完全(使 浓度降至原来的千分之一),则应向溶液里加入
浓度降至原来的千分之一),则应向溶液里加入 溶液,使溶液的pH为
溶液,使溶液的pH为___________ 。
(1)常温下,0.05mol/L硫酸溶液中,


 的盐酸中,由水电离产生的
的盐酸中,由水电离产生的 的物质的量浓度为
的物质的量浓度为(2)氨水和稀盐酸反应后的溶液呈中性,所得溶液中的离子浓度大小关系是
(3)某温度(t℃)时,
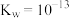 ,则该温度(填大于、等于或小于)
,则该温度(填大于、等于或小于) 溶液b L混合,若所得混合溶液为中性,则a:b=
溶液b L混合,若所得混合溶液为中性,则a:b=(4)已知
 的
的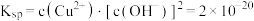 。当溶液中各种离子的浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。则①某
。当溶液中各种离子的浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。则①某 溶液里
溶液里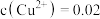 mol/L,如要生成
mol/L,如要生成 沉淀,应调整溶液的pH大于
沉淀,应调整溶液的pH大于②要使0.2

 溶液中
溶液中 沉淀较为完全(使
沉淀较为完全(使 浓度降至原来的千分之一),则应向溶液里加入
浓度降至原来的千分之一),则应向溶液里加入 溶液,使溶液的pH为
溶液,使溶液的pH为
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题。(lg2=0.3、lg5=0.7)
(1)25℃时,0.01mol/L的NaOH溶液的pH=_____ ;由水电离出的c(H+)=_____ mol/L。
(2)25℃时,pH=2的盐酸与pH=5的盐酸等体积混合后溶液的pH=_____ 。
(3)25℃时,将10mLpH=2醋酸溶液稀释到1000mL后溶液的pH_____ 4(填“大于”“小于”或“等于”)。
(4)某温度下纯水中c(H+)=4×10-7mol/L,则此时溶液中的c(OH-)=_____ mol/L。
(5)某温度时,Ksp[AgI]=9.0×10-16,求AgI饱和溶液中c(Ag+)=_____ mol/L。
(1)25℃时,0.01mol/L的NaOH溶液的pH=
(2)25℃时,pH=2的盐酸与pH=5的盐酸等体积混合后溶液的pH=
(3)25℃时,将10mLpH=2醋酸溶液稀释到1000mL后溶液的pH
(4)某温度下纯水中c(H+)=4×10-7mol/L,则此时溶液中的c(OH-)=
(5)某温度时,Ksp[AgI]=9.0×10-16,求AgI饱和溶液中c(Ag+)=
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)某温度下,纯水中的c (H+)= 4.0×10-7 mol/L, 则此温度下纯水中的c (OH-)=___ mol/L; 若温度不变, 滴入稀NaOH溶液, 使c (OH-)= 5.0×10-6 mol/L,则溶液的c (H+)= _________________ mol/L。
(2)在25℃时,100ml 1.0mol/L的盐酸与等体积1.2mol/L的氢氧化钠溶液混合, 混合后溶液的pH=_______________ 。
(2)在25℃时,100ml 1.0mol/L的盐酸与等体积1.2mol/L的氢氧化钠溶液混合, 混合后溶液的pH=
您最近半年使用:0次

 方法的示意图如下:
方法的示意图如下:
 溶液吸收一定量的
溶液吸收一定量的 ,则该溶液的
,则该溶液的 的
的 )。
)。


