已知部分弱酸的电离常数如表:下列叙述不正确的是( )
| 弱酸 | H2CO3 | HClO | HF |
| 电离平衡常数(25℃) | Ka1=4.3×10﹣7 Ka2=5.6×10﹣11 | Ka=2.98×10﹣8 | Ka=3.6×10﹣4 |
| A.氢氟酸与NaClO溶液混合能够发生反应:HF+NaClO═HClO+NaF |
| B.物质的量浓度相同的四种溶液:①NaF②Na2CO3③NaClO④NaHCO3,pH由大到小的顺序为:②>③>④>① |
| C.Na2CO3溶液不能与次氯酸发生反应 |
D.少量CO2通入NaClO溶液中的离子反应:CO2+H2O+ClO﹣= +HClO +HClO |
更新时间:2020-10-19 22:18:51
|
【知识点】 电离平衡常数及影响因素解读
相似题推荐
单选题
|
适中
(0.65)
【推荐1】25℃时有关酸的电离平衡常数
则下列有关说法正确的是
| 酸 | HF | Al(OH)3 | H2CO3 |
| 电离平衡常数(25℃) | 6.6×10—4 | 6.3×10—13 | K1=4.3×10—7 K2=5.6×10—11 |
| A.Al(OH)3为二元弱酸 |
| B.a mol·L-1NaOH溶液与b mol·L-1HF溶液等体积混合后,所得溶液中c(Na+)>c(F—),则a一定大于b |
C.同温下,NaHCO3溶液中HCO 的电离常数大于K2(碳酸的二级电离) 的电离常数大于K2(碳酸的二级电离) |
D.NaHCO3和Na2CO3混合溶液中,一定存在:c(Na+)+c(H+)=c(OH—)+c(HCO )+2c(CO )+2c(CO ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列离子方程式与所述事实相符的是
A.已知电离平衡常数: ,向 ,向 溶液中通入少量 溶液中通入少量 : :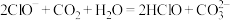 |
B.氢氧化铁溶于氢碘酸(强酸):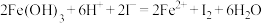 |
| C.将nmolCl2通入含有nmolFeBr2的溶液中:2Br-+Cl2=Br2+2Cl- |
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+Fe(OH)3= +3Cl-+H2O+H+ +3Cl-+H2O+H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知:常温下,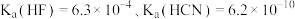 ,下列说法正确的是
,下列说法正确的是
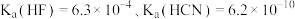 ,下列说法正确的是
,下列说法正确的是A.同 的 的 溶液和 溶液和 溶液,中和 溶液,中和 的能力: 的能力: 强于 强于 |
B.同物质的量浓度的 溶液和 溶液和 溶液,溶液 溶液,溶液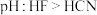 |
C.向 溶液中滴加 溶液中滴加 溶液,反应的离子方程式为: 溶液,反应的离子方程式为: |
D.将 溶液和 溶液和 溶液混合,反应的离子方程式为; 溶液混合,反应的离子方程式为; |
您最近一年使用:0次



