能基于物质的量认识物质的组成及其化学变化,是学生必备的学科素养。
(1)已知:①5.6LH2S(标准状况下)②1.204×1023个NH3分子③4.8gCH4④4℃时,5.4mL水,其中含有的氢原子数由大到小的顺序为__ 。
(2)同浓度的三种溶液:Na2SO4、MgSO4、Al2(SO4)3,其体积比为3:2:1,则SO 浓度之比为
浓度之比为__ 。
(3)在标准状况下,将VLHCl溶于0.1L水中,所得溶液的密度为dg·cm-3,则形成溶液的物质的量浓度为__ mol·L-1。
(4)某工厂废液中含有K2Cr2O7,排放废液前要将废液中的Cr2O 还原成Cr3+,取100mL此工厂的废液样品进行实验时,恰好消耗纯净NaHSO3固体3.12g。则此废液中含有K2Cr2O7的浓度为
还原成Cr3+,取100mL此工厂的废液样品进行实验时,恰好消耗纯净NaHSO3固体3.12g。则此废液中含有K2Cr2O7的浓度为__ mol·L-1。
(5)联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。实验室中可用次氯酸钠溶液与氨气反应制备联氨(N2H4),反应的化学方程式为__ 。
(6)用零价铁(Fe)去除水体中的硝酸盐(NO )已成为环境修复研究的热点之一。
)已成为环境修复研究的热点之一。
实验研究表明,将足量铁粉投入 =2.5的水体中,经24小时测得水体中NO
=2.5的水体中,经24小时测得水体中NO 去除率为100%。已知:反应的铁元素以氧化物形式存在于溶液中,NO3-全部转化为NH
去除率为100%。已知:反应的铁元素以氧化物形式存在于溶液中,NO3-全部转化为NH ,反应0.1molNO
,反应0.1molNO 恰好消耗16.8gFe,则反应的离子方程式为
恰好消耗16.8gFe,则反应的离子方程式为__ 。
(1)已知:①5.6LH2S(标准状况下)②1.204×1023个NH3分子③4.8gCH4④4℃时,5.4mL水,其中含有的氢原子数由大到小的顺序为
(2)同浓度的三种溶液:Na2SO4、MgSO4、Al2(SO4)3,其体积比为3:2:1,则SO
 浓度之比为
浓度之比为(3)在标准状况下,将VLHCl溶于0.1L水中,所得溶液的密度为dg·cm-3,则形成溶液的物质的量浓度为
(4)某工厂废液中含有K2Cr2O7,排放废液前要将废液中的Cr2O
 还原成Cr3+,取100mL此工厂的废液样品进行实验时,恰好消耗纯净NaHSO3固体3.12g。则此废液中含有K2Cr2O7的浓度为
还原成Cr3+,取100mL此工厂的废液样品进行实验时,恰好消耗纯净NaHSO3固体3.12g。则此废液中含有K2Cr2O7的浓度为(5)联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。实验室中可用次氯酸钠溶液与氨气反应制备联氨(N2H4),反应的化学方程式为
(6)用零价铁(Fe)去除水体中的硝酸盐(NO
 )已成为环境修复研究的热点之一。
)已成为环境修复研究的热点之一。实验研究表明,将足量铁粉投入
 =2.5的水体中,经24小时测得水体中NO
=2.5的水体中,经24小时测得水体中NO 去除率为100%。已知:反应的铁元素以氧化物形式存在于溶液中,NO3-全部转化为NH
去除率为100%。已知:反应的铁元素以氧化物形式存在于溶液中,NO3-全部转化为NH ,反应0.1molNO
,反应0.1molNO 恰好消耗16.8gFe,则反应的离子方程式为
恰好消耗16.8gFe,则反应的离子方程式为
20-21高三上·陕西渭南·阶段练习 查看更多[4]
陕西省渭南市大荔县同州中学2021届高三上学期第一次月考化学试题(已下线)解密02 物质的量(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密02 物质的量(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练河南省潢川第一中学2023-2024学年高三上学期第一次月考化学试题
更新时间:2020-10-24 19:45:13
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)质量相同的①H2、②SO2、③O3三种气体中,含有分子数目由多到少的顺序为_______ (填序号,下同);在同温同压下,密度由大到小的顺序为_______ 。
(2)固体A在一定温度下分解生成气体B、C、D,反应方程式为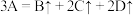 。若测得生成物气体对氢气的密度是15,则固体A的摩尔质量是
。若测得生成物气体对氢气的密度是15,则固体A的摩尔质量是_______ 。
(3)将8g铁片放入100mL硫酸铜溶液中,溶液中的Cu2+全部被还原时,铁片变为8.6g,则原c(CuSO4)为_______ mol/L。
(4)将部分在空气中被氧化的金属钠5.08g投入到水中充分反应得到100mL溶液,在该溶液中加入足量的金属铝,收集到标准状况下的气体6720mL(溶液体积变化忽略不计)。计算:
①最后所得的溶液的物质的量浓度为_______ mol/L。
②被氧化的金属钠的质量为_______ g。
(1)质量相同的①H2、②SO2、③O3三种气体中,含有分子数目由多到少的顺序为
(2)固体A在一定温度下分解生成气体B、C、D,反应方程式为
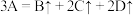 。若测得生成物气体对氢气的密度是15,则固体A的摩尔质量是
。若测得生成物气体对氢气的密度是15,则固体A的摩尔质量是(3)将8g铁片放入100mL硫酸铜溶液中,溶液中的Cu2+全部被还原时,铁片变为8.6g,则原c(CuSO4)为
(4)将部分在空气中被氧化的金属钠5.08g投入到水中充分反应得到100mL溶液,在该溶液中加入足量的金属铝,收集到标准状况下的气体6720mL(溶液体积变化忽略不计)。计算:
①最后所得的溶液的物质的量浓度为
②被氧化的金属钠的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】按要求进行计算,直接写出结果
(1)标准状况下,2.24 L CH4所含氢原子的物质的量为____ mol。
(2)含0.2 mol氧原子的NO2的质量是____ g。
(3)100 mL 0.5mol· L-1 H2SO4溶液中,H+的物质的量浓度为____ mol· L-1。
(4)1mol碳在一定量氧气中反应,生成气体的质量为36 g。所得气体的物质的量为____ mol。
(1)标准状况下,2.24 L CH4所含氢原子的物质的量为
(2)含0.2 mol氧原子的NO2的质量是
(3)100 mL 0.5mol· L-1 H2SO4溶液中,H+的物质的量浓度为
(4)1mol碳在一定量氧气中反应,生成气体的质量为36 g。所得气体的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】化学计量在化学中占有重要的地位,请回答下列问题 设
设 表示阿伏加德罗常数的值
表示阿伏加德罗常数的值 。
。
(1)标准状况下,0.2molNH3的体积是__________ L,其中含有的NH3分子数是__________ 个,含氢原子数是_______ 个,其中含有的电子数是__________ 个,其中含有的质子数是__________ 个。
(2)49g的H2SO4中含有______ mol氧原子,能与______ molNaOH恰好完全反应。
(3)已知16gA和20gB恰好完全反应生成0.04molC和31.7gD,则C的摩尔质量为_________ g/mol。
 设
设 表示阿伏加德罗常数的值
表示阿伏加德罗常数的值 。
。 (1)标准状况下,0.2molNH3的体积是
(2)49g的H2SO4中含有
(3)已知16gA和20gB恰好完全反应生成0.04molC和31.7gD,则C的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)某气体氧化物的化学式为 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为___________ ,R的相对原子质量为___________ 。
(2)标准状况下有① ,②
,② 个
个 分子,③
分子,③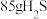 三种气体,对这三种气体的物质的量从大到小的顺序是
三种气体,对这三种气体的物质的量从大到小的顺序是___________ (填序号)。
(3)某混合盐溶液中含有离子: 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则
___________  。
。
(4)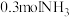 中含有质子数与
中含有质子数与___________ 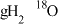 分子中所含质子数相等。
分子中所含质子数相等。
(5) 溶液中
溶液中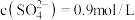 ,则
,则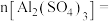
___________ 。
(1)某气体氧化物的化学式为
 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为(2)标准状况下有①
 ,②
,② 个
个 分子,③
分子,③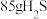 三种气体,对这三种气体的物质的量从大到小的顺序是
三种气体,对这三种气体的物质的量从大到小的顺序是(3)某混合盐溶液中含有离子:
 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则
 。
。(4)
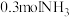 中含有质子数与
中含有质子数与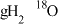 分子中所含质子数相等。
分子中所含质子数相等。(5)
 溶液中
溶液中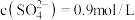 ,则
,则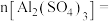
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)0.2molNH3的质量为_______ g
(2)配制250mL1.0mol/LH2SO4溶液,需要18mol/LH2SO4溶液体积是___ 。
(3)我国古代四大发明之一的黑火药是由硫粉、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C=K2S+N2↑+3CO2↑,反应中被还原的物质是____ (填化学式);1mol硫参加反应时转移电子数为_____ 。
(4)已知NH3和Cl2可以发生氧化还原反应,配平该方程式:NH3+Cl2=N2+HCl,_______ 。
(2)配制250mL1.0mol/LH2SO4溶液,需要18mol/LH2SO4溶液体积是
(3)我国古代四大发明之一的黑火药是由硫粉、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C=K2S+N2↑+3CO2↑,反应中被还原的物质是
(4)已知NH3和Cl2可以发生氧化还原反应,配平该方程式:NH3+Cl2=N2+HCl,
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】取58.85g由NaCl和Na2CO3组成的固体样品,加入足量稀盐酸完全反应,生成的气体在标准状况下体积为11.2L。回答下列问题:
(1)发生反应的离子方程式为_______ 。
(2)列式计算固体样品中Na2CO3和NaCl的物质的量之比_______ 。
(1)发生反应的离子方程式为
(2)列式计算固体样品中Na2CO3和NaCl的物质的量之比
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】工业上常以铝土矿为原料来冶炼金属铝。已知:铝土矿的主要成分是 (其中含有
(其中含有 、
、 等杂质)。为检测某铝土矿样品中
等杂质)。为检测某铝土矿样品中 的含量,进行如下实验过程:
的含量,进行如下实验过程:
①取矿样10.0g加入过量稀盐酸溶解,过滤弃去不溶残渣。
②将滤液稀释并在250mL容量瓶中定容后,取25.0mL逐滴加入 的NaOH溶液。得到如右图所示的变化关系。
的NaOH溶液。得到如右图所示的变化关系。___________ 。
(2)最后所得不溶于NaOH溶液的沉淀的化学式为___________ ,其物质的量为___________ 。
(3)该铝土矿样中 的质量分数为
的质量分数为___________ 。
 (其中含有
(其中含有 、
、 等杂质)。为检测某铝土矿样品中
等杂质)。为检测某铝土矿样品中 的含量,进行如下实验过程:
的含量,进行如下实验过程:①取矿样10.0g加入过量稀盐酸溶解,过滤弃去不溶残渣。
②将滤液稀释并在250mL容量瓶中定容后,取25.0mL逐滴加入
 的NaOH溶液。得到如右图所示的变化关系。
的NaOH溶液。得到如右图所示的变化关系。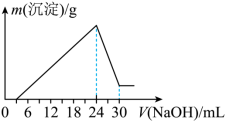
(2)最后所得不溶于NaOH溶液的沉淀的化学式为
(3)该铝土矿样中
 的质量分数为
的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】从一瓶放置较长时间的 溶液中取出20mL,向该溶液中逐滴加入
溶液中取出20mL,向该溶液中逐滴加入 盐酸至过量,反应产生的
盐酸至过量,反应产生的 气体的物质的量与加入盐酸的体积关系如图所示(忽略
气体的物质的量与加入盐酸的体积关系如图所示(忽略 溶解和
溶解和 挥发),请回答下列问题:
挥发),请回答下列问题:

(1)O-a段发生反应的离子方程式为______________________ ,______________________ 。
(2)O点溶液中所含溶质的物质的量为___________ ,___________ 。
(3)原 溶液的物质的量浓度为
溶液的物质的量浓度为_____________ 。
 溶液中取出20mL,向该溶液中逐滴加入
溶液中取出20mL,向该溶液中逐滴加入 盐酸至过量,反应产生的
盐酸至过量,反应产生的 气体的物质的量与加入盐酸的体积关系如图所示(忽略
气体的物质的量与加入盐酸的体积关系如图所示(忽略 溶解和
溶解和 挥发),请回答下列问题:
挥发),请回答下列问题:
(1)O-a段发生反应的离子方程式为
(2)O点溶液中所含溶质的物质的量为
(3)原
 溶液的物质的量浓度为
溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)次磷酸钠(NaH2PO2)可用于化学镀镍,即通过化学反应在塑料镀件表面沉积镍—磷合金。化学镀镍的溶液中含有Ni2+和 ,在酸性条件下发生以下镀镍反应:Ni2++
,在酸性条件下发生以下镀镍反应:Ni2++ +=Ni+
+=Ni+ +。
+。
①请完成并配平上述方程式_____ 。
②上述反应中,若生成1 mol ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为_____ 。
(2)①高铁酸盐也是常用的水处理剂。高铁酸钠(Na2FeO4)可用如下反应制备:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,若生成2 mol Na2FeO4,则反应中电子转移的物质的量为____ mol。
②高铁酸盐可将水体中的Mn2+氧化为MnO2进行除去,若氧化含Mn2+1 mg的水体样本,需要1.2 mg·L-1高铁酸钾____ L。
(3)铁红是一种红色颜料,其成分是Fe2O3,将一定量的铁红溶于160 mL 5mol/L盐酸中,再加入一定量铁粉恰好溶解,收集到2.24 L(标准状况)气体,经检测,溶液中无Fe3+,则参加反应的铁粉的质量为____ 。
 ,在酸性条件下发生以下镀镍反应:Ni2++
,在酸性条件下发生以下镀镍反应:Ni2++ +=Ni+
+=Ni+ +。
+。①请完成并配平上述方程式
②上述反应中,若生成1 mol
 ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为(2)①高铁酸盐也是常用的水处理剂。高铁酸钠(Na2FeO4)可用如下反应制备:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,若生成2 mol Na2FeO4,则反应中电子转移的物质的量为
②高铁酸盐可将水体中的Mn2+氧化为MnO2进行除去,若氧化含Mn2+1 mg的水体样本,需要1.2 mg·L-1高铁酸钾
(3)铁红是一种红色颜料,其成分是Fe2O3,将一定量的铁红溶于160 mL 5mol/L盐酸中,再加入一定量铁粉恰好溶解,收集到2.24 L(标准状况)气体,经检测,溶液中无Fe3+,则参加反应的铁粉的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】已知亚磷酸(H3PO3)的结构如图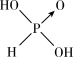 ,是具有强还原性的二元弱酸,可以被银离子氧化为磷酸。
,是具有强还原性的二元弱酸,可以被银离子氧化为磷酸。
(1)已知亚磷酸可由PCl3水解而成,请写出相应的离子方程式_____ ;
(2)亚磷酸与银离子反应时氧化剂与还原剂的物质的量之比为_____ ;
(3)某温度下,0.10mol•L-1的H3PO3溶液的pH为1.6,即c(H+)=2.5×10-2mol•L-1,该温度下H3PO3的一级电离平衡常数K=____ ;(H3PO3第二步电离忽略不计,结果保留两位有效数字)
(4)向H3PO3溶液中滴加NaOH溶液至中性,所得溶液中:c(Na+)__ c(H2PO3-)+2c(HPO32-)(填“>”、“<”或“=”,下同)。
 ,是具有强还原性的二元弱酸,可以被银离子氧化为磷酸。
,是具有强还原性的二元弱酸,可以被银离子氧化为磷酸。(1)已知亚磷酸可由PCl3水解而成,请写出相应的离子方程式
(2)亚磷酸与银离子反应时氧化剂与还原剂的物质的量之比为
(3)某温度下,0.10mol•L-1的H3PO3溶液的pH为1.6,即c(H+)=2.5×10-2mol•L-1,该温度下H3PO3的一级电离平衡常数K=
(4)向H3PO3溶液中滴加NaOH溶液至中性,所得溶液中:c(Na+)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】(1)3.01×1023个OH-的物质的量为_______ ,含有电子的物质的量为_______ ,这些OH-和_______ g的Na+含有的电子数相同。
(2)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、 ,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(
,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c( )=
)=_______ 。
(3)实验室可用KMnO4和浓盐酸反应制取氯气。其变化可表述为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
①请将上述化学方程式改写为离子方程式_______ 。
②浓盐酸在反应中显示出来的性质是_______ (填字母)。
a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
③此反应中氧化产物是_______ (填化学式),还原性Cl-______ Mn2+(填>、<或=)。
④用双线桥法表示该反应电子转移的方向和数目:_______ 。
(2)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、
 ,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(
,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c( )=
)=(3)实验室可用KMnO4和浓盐酸反应制取氯气。其变化可表述为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
①请将上述化学方程式改写为离子方程式
②浓盐酸在反应中显示出来的性质是
a.只有还原性 b.还原性和酸性 c.只有氧化性 d.氧化性和酸性
③此反应中氧化产物是
④用双线桥法表示该反应电子转移的方向和数目:
您最近一年使用:0次



