已知亚磷酸(H3PO3)的结构如图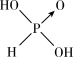 ,是具有强还原性的二元弱酸,可以被银离子氧化为磷酸。
,是具有强还原性的二元弱酸,可以被银离子氧化为磷酸。
(1)已知亚磷酸可由PCl3水解而成,请写出相应的离子方程式_____ ;
(2)亚磷酸与银离子反应时氧化剂与还原剂的物质的量之比为_____ ;
(3)某温度下,0.10mol•L-1的H3PO3溶液的pH为1.6,即c(H+)=2.5×10-2mol•L-1,该温度下H3PO3的一级电离平衡常数K=____ ;(H3PO3第二步电离忽略不计,结果保留两位有效数字)
(4)向H3PO3溶液中滴加NaOH溶液至中性,所得溶液中:c(Na+)__ c(H2PO3-)+2c(HPO32-)(填“>”、“<”或“=”,下同)。
 ,是具有强还原性的二元弱酸,可以被银离子氧化为磷酸。
,是具有强还原性的二元弱酸,可以被银离子氧化为磷酸。(1)已知亚磷酸可由PCl3水解而成,请写出相应的离子方程式
(2)亚磷酸与银离子反应时氧化剂与还原剂的物质的量之比为
(3)某温度下,0.10mol•L-1的H3PO3溶液的pH为1.6,即c(H+)=2.5×10-2mol•L-1,该温度下H3PO3的一级电离平衡常数K=
(4)向H3PO3溶液中滴加NaOH溶液至中性,所得溶液中:c(Na+)
更新时间:2019-04-18 18:26:40
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】将10g铁粉置于40mL较浓的硝酸中,微热完全反应时,收集到NO2和NO混合气体1792mL(标准状况下),还残留4.4g固体。求:
(1)该反应中被还原的硝酸和未被还原的硝酸的物质的量之比_______ ;
(2)原硝酸的物质的量浓度_______ ;
(3)NO和NO2的体积比_______ ;
(4)写出总的化学方程式_______ 。
(1)该反应中被还原的硝酸和未被还原的硝酸的物质的量之比
(2)原硝酸的物质的量浓度
(3)NO和NO2的体积比
(4)写出总的化学方程式
您最近一年使用:0次
【推荐2】把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2
(1)用单线桥表示反应的电子转移方向和数目:_______ 。
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:_______ 。
(3)若反应中有3.4克氨发生氧化反应,则反应中有生成氮气的质量为_______ 。
(4)高铁酸钠(Na2FeO4)(铁为+6 价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+ NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中 (用化学式表示, 下同),还原产物为_______ ,_______ 元素被氧化。
②配平该反应的方程式并用双线桥在方程式中标出电子转移的情况:_______ 。
(1)用单线桥表示反应的电子转移方向和数目:
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:
(3)若反应中有3.4克氨发生氧化反应,则反应中有生成氮气的质量为
(4)高铁酸钠(Na2FeO4)(铁为+6 价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+ NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中 (用化学式表示, 下同),还原产物为
②配平该反应的方程式并用双线桥在方程式中标出电子转移的情况:
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)Cl2通入水中制氯水,反应的离子方程式:____ 。
(2)高铁酸钾(K2FeO4)被人们称为“绿色化学”净水剂。高铁酸钾在酸性至弱碱性条件下不稳定。工业上用KClO与Fe(NO3)3溶液反应制得K2FeO4,反应的离子方程式:____ 。
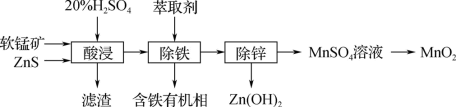
(3)以软锰矿(主要成分为MnO2、SiO2等)为原料制备高纯MnO2的流程如图:
①滤渣中含大量硫单质,酸浸时主要反应的化学方程式:____ 。
②酸性条件下,用合适的氧化剂可以将MnSO4转化为高纯MnO2。用NaClO3作氧化剂时会同时产生NaCl,该反应的离子方程式:____ 。
(4)已知次氯酸可被FeSO4等物质还原。用下列实验方案测定某次试验所得溶液中次氯酸的物质的量浓度:量取10.00mL上述次氯酸溶液,并稀释至100mL,再从其中取出10.00mL于锥形瓶中,并加入10.00mL0.8000mol/L的FeSO4溶液,充分反应后,用0.05000mol/L的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液24.00mL,则原次氯酸溶液的浓度为____ (写出计算过程)。
(1)Cl2通入水中制氯水,反应的离子方程式:
(2)高铁酸钾(K2FeO4)被人们称为“绿色化学”净水剂。高铁酸钾在酸性至弱碱性条件下不稳定。工业上用KClO与Fe(NO3)3溶液反应制得K2FeO4,反应的离子方程式:
(3)以软锰矿(主要成分为MnO2、SiO2等)为原料制备高纯MnO2的流程如图:

①滤渣中含大量硫单质,酸浸时主要反应的化学方程式:
②酸性条件下,用合适的氧化剂可以将MnSO4转化为高纯MnO2。用NaClO3作氧化剂时会同时产生NaCl,该反应的离子方程式:
(4)已知次氯酸可被FeSO4等物质还原。用下列实验方案测定某次试验所得溶液中次氯酸的物质的量浓度:量取10.00mL上述次氯酸溶液,并稀释至100mL,再从其中取出10.00mL于锥形瓶中,并加入10.00mL0.8000mol/L的FeSO4溶液,充分反应后,用0.05000mol/L的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液24.00mL,则原次氯酸溶液的浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】在废水处理领域中,H2S或Na2S能使某些金属离子生成极难溶的硫化物而除去。已知:25℃H2S电离常数分别为Ka1=1.3×10—7,Ka2=7.0×10—15,某溶液含0.02mol/LMn2+、0.1mol/LH2S,向该溶液中通入HCl气体或加入NaOH固体以调节溶液pH,(忽略溶液体积的变化、H2S的挥发)。当溶液的pH=5时,Mn2+开始沉淀为MnS,则:
(1)HS—的电离常数表达式为______________ ;
(2)Na2S溶液中的微粒有_____________ 种;
(3)NaHS溶液的pH_____________ 7(填“>”、“=”或“<”),理由是__________________ ;
(4)当溶液的pH=5时,c(S2—)∶c(H2S)=______________ ;
(5)MnS的溶度积为_____________ ;
(6)当Mn2+完全沉淀时,溶液中c(S2—)=____________ mol/L。
(1)HS—的电离常数表达式为
(2)Na2S溶液中的微粒有
(3)NaHS溶液的pH
(4)当溶液的pH=5时,c(S2—)∶c(H2S)=
(5)MnS的溶度积为
(6)当Mn2+完全沉淀时,溶液中c(S2—)=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1) 时,
时, 的盐酸中由水电离出的
的盐酸中由水电离出的 为
为_________ 。
(2) 时,向
时,向 的蒸馏水中加入
的蒸馏水中加入 晶体,保持温度不变,测得溶液的
晶体,保持温度不变,测得溶液的 。此时水的离子积
。此时水的离子积
________ ,溶液中 为
为________ 。
(3) 时,
时,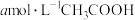 溶液的
溶液的 ,用含a和b的代数式表示
,用含a和b的代数式表示 的电离平衡常数
的电离平衡常数
_______ 。
(4) 时,
时, 的
的 溶液和
溶液和 的NaOH溶液等体积混合后,溶液呈
的NaOH溶液等体积混合后,溶液呈_____ (填“酸”“中”或“碱”)性。
(5) 时,
时, ,
,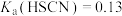 。该温度下将
。该温度下将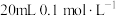
 溶液和
溶液和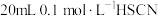 溶液分别与
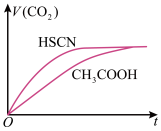
溶液分别与 溶液混合,实验测得产生的气体体积(V)随时间(t)变化的曲线如图所示,反应初始阶段,两种溶液产生
溶液混合,实验测得产生的气体体积(V)随时间(t)变化的曲线如图所示,反应初始阶段,两种溶液产生 气体的速率存在明显差异的原因是
气体的速率存在明显差异的原因是____ 。
(1)
 时,
时, 的盐酸中由水电离出的
的盐酸中由水电离出的 为
为(2)
 时,向
时,向 的蒸馏水中加入
的蒸馏水中加入 晶体,保持温度不变,测得溶液的
晶体,保持温度不变,测得溶液的 。此时水的离子积
。此时水的离子积
 为
为(3)
 时,
时,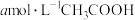 溶液的
溶液的 ,用含a和b的代数式表示
,用含a和b的代数式表示 的电离平衡常数
的电离平衡常数
(4)
 时,
时, 的
的 溶液和
溶液和 的NaOH溶液等体积混合后,溶液呈
的NaOH溶液等体积混合后,溶液呈(5)
 时,
时, ,
,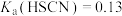 。该温度下将
。该温度下将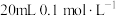
 溶液和
溶液和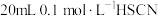 溶液分别与
溶液分别与 溶液混合,实验测得产生的气体体积(V)随时间(t)变化的曲线如图所示,反应初始阶段,两种溶液产生
溶液混合,实验测得产生的气体体积(V)随时间(t)变化的曲线如图所示,反应初始阶段,两种溶液产生 气体的速率存在明显差异的原因是
气体的速率存在明显差异的原因是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】常温下,向amol·L-1CH3COONa溶液中滴加等体积的bmol·L-1盐酸使溶液呈中性(不考虑盐酸和醋酸的挥发),则醋酸的电离常数Ka=___________ (用含a和b的代数式表示)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】人类向大气中排放的NOx和SO2对环境会产生危害,烟气的脱硝(除NOx)技术和脱硫(除SO2)技术都是环境科学研究的热点。
(1)选择性催化还原技术是目前最成熟的烟气脱硝技术,即在催化剂作用下,用还原剂(如NH3选择性地与NOx反应生成N2和H2O。
已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH1=-905.5kJ·mol-1
N2(g)+O2(g)=2NO(g) ΔH2=+180kJ·mol-1
则4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) ΔH3=__ 。
(2)碱性KMnO4氧化法也可将NOx进行脱除。
①用KMnO4(NaOH)溶液进行烟气中NO的脱除,将该离子方程式补充完整。__
□NO+□MnO4-+□__=NO2-+3NO3-+□MnO42-+□__
②下列叙述正确的是__ (填字母序号)。
A.将脱除后的混合溶液进行分离可获得氮肥
B.反应后混合溶液中:c(MnO4-)+2c(MnO42-)=c(K+)
C.在不同酸碱性条件下,KMnO4发生还原反应的产物可能不同
(3)催化剂V2O5可用于处理NOx和SO2。
V2O5在催化降解NOx的过程中,也会对SO2和O2反应起到一定的催化作用,其反应式如下:
a.V2O5+SO2=V2O4+SO3
b.__
c.2VOSO4=V2O5+SO2+SO3
SO3进一步与烟气中逃逸的氨反应,生成硫酸氢铵和硫酸铵。
(1)选择性催化还原技术是目前最成熟的烟气脱硝技术,即在催化剂作用下,用还原剂(如NH3选择性地与NOx反应生成N2和H2O。
已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH1=-905.5kJ·mol-1
N2(g)+O2(g)=2NO(g) ΔH2=+180kJ·mol-1
则4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) ΔH3=
(2)碱性KMnO4氧化法也可将NOx进行脱除。
①用KMnO4(NaOH)溶液进行烟气中NO的脱除,将该离子方程式补充完整。
□NO+□MnO4-+□__=NO2-+3NO3-+□MnO42-+□__
②下列叙述正确的是
A.将脱除后的混合溶液进行分离可获得氮肥
B.反应后混合溶液中:c(MnO4-)+2c(MnO42-)=c(K+)
C.在不同酸碱性条件下,KMnO4发生还原反应的产物可能不同
(3)催化剂V2O5可用于处理NOx和SO2。
V2O5在催化降解NOx的过程中,也会对SO2和O2反应起到一定的催化作用,其反应式如下:
a.V2O5+SO2=V2O4+SO3
b.
c.2VOSO4=V2O5+SO2+SO3
SO3进一步与烟气中逃逸的氨反应,生成硫酸氢铵和硫酸铵。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列问题:
(1)H3PO2 是一种一元中强酸,写出其电离方程式:_____ 。
(2)H3PO2 及 NaH2PO2 均可将溶液中的银离子还原为银单质,从而可用于化学镀银。
①利用 H3PO2 进行化学镀银反应中,氧化剂与还原剂的物质的量之比为 4︰1,则氧化产物为:____ (填化学式)
②NaH2PO2 是____ (填“正盐”或“酸式盐”),其溶液显_____ (填“弱酸性”、“中性”或者“弱碱性”),其溶液中离子浓度由大到小的顺序为_____
(3)H3PO2 的工业制法是:将白磷(P4)与氢氧化钡溶液反应生成 PH3 气体和 Ba(H2PO2)2,后者再与硫酸反应,写出白磷与氢氧化钡溶液反应的化学方程式:_____ 。
(4)常温下将amol·L−1的醋酸与 b mol·L−1的Ba(OH)2溶液等体积混合,充分反应后溶液恰好呈中性,醋酸的电离常数Ka =______ (用含 a 和 b 的代数式表示)。
(1)H3PO2 是一种一元中强酸,写出其电离方程式:
(2)H3PO2 及 NaH2PO2 均可将溶液中的银离子还原为银单质,从而可用于化学镀银。
①利用 H3PO2 进行化学镀银反应中,氧化剂与还原剂的物质的量之比为 4︰1,则氧化产物为:
②NaH2PO2 是
(3)H3PO2 的工业制法是:将白磷(P4)与氢氧化钡溶液反应生成 PH3 气体和 Ba(H2PO2)2,后者再与硫酸反应,写出白磷与氢氧化钡溶液反应的化学方程式:
(4)常温下将amol·L−1的醋酸与 b mol·L−1的Ba(OH)2溶液等体积混合,充分反应后溶液恰好呈中性,醋酸的电离常数Ka =
您最近一年使用:0次



