(1)汽车发动机工作时会引发 和
和 反应,生成
反应,生成 等污染大气,其中生成
等污染大气,其中生成 的能量变化如图1所示,则图1中三种分子最稳定的是
的能量变化如图1所示,则图1中三种分子最稳定的是______ ,图1中对应反应的热化学方程式为_____ 。
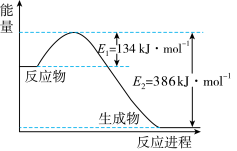
(2)图2是 与
与 反应转化为
反应转化为 和
和 过程中的能量变化示意图,根据图2分析,若
过程中的能量变化示意图,根据图2分析,若 被氧化,该过程放出的热量
被氧化,该过程放出的热量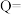
________  。若该反应是可逆反应,在相同条件下将
。若该反应是可逆反应,在相同条件下将 与
与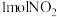 混合,则充分反应后放出的热量
混合,则充分反应后放出的热量_________ (填“>”“<”或“=”)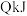 。
。
(3)仿照图2的形式,在图3中绘制出 与
与 反应生成
反应生成 的能量变化曲线
的能量变化曲线______ 。
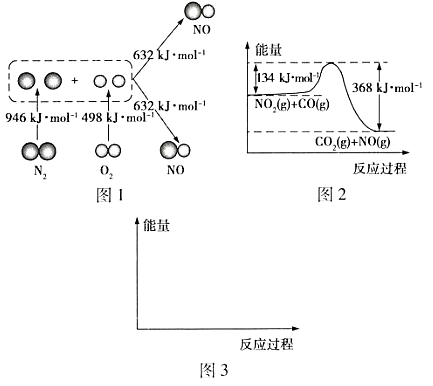
 和
和 反应,生成
反应,生成 等污染大气,其中生成
等污染大气,其中生成 的能量变化如图1所示,则图1中三种分子最稳定的是
的能量变化如图1所示,则图1中三种分子最稳定的是(2)图2是
 与
与 反应转化为
反应转化为 和
和 过程中的能量变化示意图,根据图2分析,若
过程中的能量变化示意图,根据图2分析,若 被氧化,该过程放出的热量
被氧化,该过程放出的热量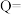
 。若该反应是可逆反应,在相同条件下将
。若该反应是可逆反应,在相同条件下将 与
与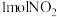 混合,则充分反应后放出的热量
混合,则充分反应后放出的热量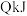 。
。(3)仿照图2的形式,在图3中绘制出
 与
与 反应生成
反应生成 的能量变化曲线
的能量变化曲线
更新时间:2020-10-12 15:03:46
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】下列变化属于①放热反应 ②吸热反应
A:分解反应 B:化合反应C:置换反应
(1)氯酸钾分解制氧气,既是_______ (填①或②)又是______ 。(填A或B或C,下同)
(2)生石灰跟水反应生成熟石灰,既是_______ 又是______ 。
(3)锌粒与稀硫酸的反应,既是_______ 又是_________ 。
A:分解反应 B:化合反应C:置换反应
(1)氯酸钾分解制氧气,既是
(2)生石灰跟水反应生成熟石灰,既是
(3)锌粒与稀硫酸的反应,既是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】化学反应中常伴随着能量变化。
I.将Al条打磨后,插入6 mol/L盐酸中。
(1)如果Al条不打磨,开始一段时间没有气泡冒出,用离子方程式说明其原因___________ 。
(2)该反应的能量变化可用下图中的___________ 表示(填序号)。___________ 。t2~t3速率变化的主要原因是___________ 。
(4)铝与某些金属氧化物在高热条件下发生的反应,同时放出巨大的热,铁路工人经常用铝热剂焊接铁轨,写出化学方程式___________ 。
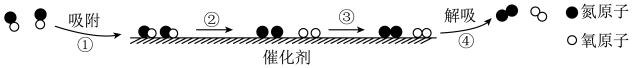
Ⅱ. 利用固体表面催化工艺进行NO分解的过程如下图所示。___________ 键断裂,此过程___________ (放出或者吸收)能量。
I.将Al条打磨后,插入6 mol/L盐酸中。
(1)如果Al条不打磨,开始一段时间没有气泡冒出,用离子方程式说明其原因
(2)该反应的能量变化可用下图中的


(4)铝与某些金属氧化物在高热条件下发生的反应,同时放出巨大的热,铁路工人经常用铝热剂焊接铁轨,写出化学方程式
Ⅱ. 利用固体表面催化工艺进行NO分解的过程如下图所示。
您最近一年使用:0次
【推荐1】Ⅰ.如图是1molC(s)和1molH2O(g)反应生成1molCO(g)、1molH2(g)的途径和三个状态的能量。

(1)该反应_____ (填“吸热”或“放热”)反应。
(2)比较E1、E2、E3的大小:_____ 。
Ⅱ.已知2mol氢气燃烧生成液态水时放出572kJ的热量,请回答下列问题:
(3)若2mol氢气完全燃烧生成水蒸气,则放出的热量_____ (填“大于”、“小于”或 “等于”)572kJ。
(4)若1mol液态水分解生成氢气和氧气,该反应_____ (填“吸收”或“放出”) _____ kJ的能量。
Ⅲ.已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示。
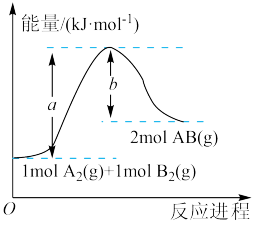
(5)该反应_____ (填“吸收”或“放出”)_____ kJ(用a、b表示)的能量。

(1)该反应
(2)比较E1、E2、E3的大小:
Ⅱ.已知2mol氢气燃烧生成液态水时放出572kJ的热量,请回答下列问题:
(3)若2mol氢气完全燃烧生成水蒸气,则放出的热量
(4)若1mol液态水分解生成氢气和氧气,该反应
Ⅲ.已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示。

(5)该反应
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知氮化硅陶瓷材料可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得: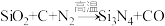 (未配平)。该反应过程中的能量变化如图所示:
(未配平)。该反应过程中的能量变化如图所示:
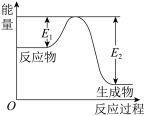
试回答下列问题。
(1)该反应中的氧化剂是________ ,还原产物是________ 。
(2)该反应是________ (填“吸热反应”或“放热反应”),
________ (填“>” “<”或“=”)0。
(3)该反应过程中,断裂旧化学键吸收的总能量________ (填“>”“<”或“=”)形成新化学键释放的总能量。
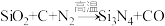 (未配平)。该反应过程中的能量变化如图所示:
(未配平)。该反应过程中的能量变化如图所示:
试回答下列问题。
(1)该反应中的氧化剂是
(2)该反应是

(3)该反应过程中,断裂旧化学键吸收的总能量
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】反应焓变
(1)概念:___________ 的焓与___________ 的焓之差。
(2)表达式:ΔH=___________ ,单位是___________ 。
(3)反应焓变与反应热的关系:对于等压条件下进行的化学反应,如果反应中物质的能量变化只与热能发生转化,则反应热Qp与焓变ΔH的关系是___________ 。
(4)反应焓变与吸热反应和放热反应的关系
(1)概念:
(2)表达式:ΔH=
(3)反应焓变与反应热的关系:对于等压条件下进行的化学反应,如果反应中物质的能量变化只与热能发生转化,则反应热Qp与焓变ΔH的关系是
(4)反应焓变与吸热反应和放热反应的关系
| 图示 |  |  |
| 体系能 量变化 | 反应产物的焓 | 反应产物的焓 |
| 反应类型 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)有① 、
、 、
、 ;②H2、D2、T2;③石墨、金刚石;④
;②H2、D2、T2;③石墨、金刚石;④ 、
、 、
、 ;四组微粒或物质。互为同位素的是
;四组微粒或物质。互为同位素的是________ (填编号,下同),互为同素异形体的是_________ 。
(2)已知拆开1 mol H—H键、1 mol N≡N、1 mol N—H键分别需要吸收的能量为436kJ、946k J、391k J。则由氢气和氮气反应生成1 mol NH3需要__________ (填“放出”或“吸收”)___________ kJ能量。
(3)控制和治理SO2是减少酸雨的有效途径,有学者设想以如图所示装置用电化学原理将他们转化为重要化工原料。若A为SO2,B为O2,C为H2SO4。则负极是______ (填“A”或“B”),负极反应式为 ______________ 。

(4)已知由甲烷CH4和氧气构成的燃料电池,电解质溶液为KOH溶液时,负极通入的气体为_______ ,(填化学式),负极反应式为______________
 、
、 、
、 ;②H2、D2、T2;③石墨、金刚石;④
;②H2、D2、T2;③石墨、金刚石;④ 、
、 、
、 ;四组微粒或物质。互为同位素的是
;四组微粒或物质。互为同位素的是(2)已知拆开1 mol H—H键、1 mol N≡N、1 mol N—H键分别需要吸收的能量为436kJ、946k J、391k J。则由氢气和氮气反应生成1 mol NH3需要
(3)控制和治理SO2是减少酸雨的有效途径,有学者设想以如图所示装置用电化学原理将他们转化为重要化工原料。若A为SO2,B为O2,C为H2SO4。则负极是

(4)已知由甲烷CH4和氧气构成的燃料电池,电解质溶液为KOH溶液时,负极通入的气体为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在25℃、101kPa的条件下,断裂1 molH—H键吸收436 kJ能量,断裂1mol Cl—Cl键吸收243kJ能量,形成1 molH—Cl键放出431 kJ能量。
H2+Cl2===2HCl的化学反应可用如图表示:

请回答下列有关问题:
(1)反应物断键吸收的总能量为____ 。
(2)生成物成键放出的总能量为____ 。
(3)1molH2和1molCl2反应生成2molHCl是_____ (填“吸收”或“放出”)能量的反应,其能量值为____ 。
(4)反应物总能量___ (填“>”或“<”)生成物总能量。
H2+Cl2===2HCl的化学反应可用如图表示:

请回答下列有关问题:
(1)反应物断键吸收的总能量为
(2)生成物成键放出的总能量为
(3)1molH2和1molCl2反应生成2molHCl是
(4)反应物总能量
您最近一年使用:0次