ClO2是一种消毒、杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O,试回答下列问题。
(1)该反应中氧化产物是_______ ,被还原的元素是________ 。
(2)若反应共产生了0.2mol气体,则反应转移电子的物质的量为________ mol,消耗还原剂的质量为________ g。ClO2的有效氯含______ (有效氯含量指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力)。
(3)用ClO2气体可去除地下水中Mn2+,生成难溶于水的MnO2,该反应的离子方程式为___________ 。
(1)该反应中氧化产物是
(2)若反应共产生了0.2mol气体,则反应转移电子的物质的量为
(3)用ClO2气体可去除地下水中Mn2+,生成难溶于水的MnO2,该反应的离子方程式为
更新时间:2020-11-18 16:32:49
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】司机酒后驾车时可检测他呼出的气体,所利用的化学反应如下:2CrO3 + 3C2H5OH + 3 H2SO4 = Cr2(SO4)3 + 3 CH3CHO + 6H2O。被检测的气体成分是______ ,上述反应中的氧化剂是______ 。还原剂是______ ,氧化产物是:______ 还原产物是:______ 。
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求回答下列问题
(1)写出钠离子的结构示意图:___________
(2)对于反应C+2CuO 2Cu+CO2↑,C得到氧,发生了
2Cu+CO2↑,C得到氧,发生了___________ 反应;CuO失去氧,发生了___________ 反应。
(3)在反应8NH3+3Cl2=6NH4Cl+N2中,NH3中氮元素的化合价是___________ ,氧化剂是___________ (填化学式,下同),氧化产物是___________ ,被氧化的氨和未被氧化的氨的质量之比为___________ 。
(1)写出钠离子的结构示意图:
(2)对于反应C+2CuO
 2Cu+CO2↑,C得到氧,发生了
2Cu+CO2↑,C得到氧,发生了(3)在反应8NH3+3Cl2=6NH4Cl+N2中,NH3中氮元素的化合价是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】钠和铝是两种重要的金属。请回答下列问题:
(1)一小块金属钠长时间放置在空气中,可能有下列现象,这些现象出现的先后顺序是______________________ (填序号);
①变成白色粉末 ②变暗 ③变成白色固体 ④变成液体
若金属钠长时间在潮湿的空气中放置,最后生成的物质是_________ (填名称)。
(2)将一小块金属钠投入水中,观察到的实验现象是________ (填序号),发生反应的离子方程式为:__________________ 。
A.钠沉到水底 B.钠熔成小球 C.小球四处游动
(3)铝与稀硝酸反应的化学方程式为:Al+4HNO3=Al(NO3)3+NO↑+2H2O,该反应的氧化剂是_______ (填化学式),还原剂与氧化剂的物质的量之比是________ ,当有5.4gAl发生反应时,转移的电子数为________ 。
(1)一小块金属钠长时间放置在空气中,可能有下列现象,这些现象出现的先后顺序是
①变成白色粉末 ②变暗 ③变成白色固体 ④变成液体
若金属钠长时间在潮湿的空气中放置,最后生成的物质是
(2)将一小块金属钠投入水中,观察到的实验现象是
A.钠沉到水底 B.钠熔成小球 C.小球四处游动
(3)铝与稀硝酸反应的化学方程式为:Al+4HNO3=Al(NO3)3+NO↑+2H2O,该反应的氧化剂是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】将1.92 g铜与150 mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为672mL。请回答:
(1)NO 的物质的量_______ mol,NO2 的物质的量______ mol ;
(2)根据(1)计算结果,写出该反应的离子方程式_____________ ;
(3)如果产生的气体全部释放后,向溶液加入200mL0.45mol/L 的NaOH 溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为___ mol /L。
(4)如果将生成的混合气体672mL 收集在容器里,将容器倒扣在水槽中,同时向容器中通入一定体积的O2,恰好使容器中充满液体,则通入O2的体积在标准状况下为______ mL。
(1)NO 的物质的量
(2)根据(1)计算结果,写出该反应的离子方程式
(3)如果产生的气体全部释放后,向溶液加入200mL0.45mol/L 的NaOH 溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为
(4)如果将生成的混合气体672mL 收集在容器里,将容器倒扣在水槽中,同时向容器中通入一定体积的O2,恰好使容器中充满液体,则通入O2的体积在标准状况下为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3= Cu(NO3)2+NO2↑+ NO↑+H2O(方程式未配平)
(1)硝酸在该反应中表现出的性质是___________ 。
(2)0.3mol Cu被一定浓度的硝酸完全溶解后,如果此时产生的的NO和NO2气体总体积在标准状况下8.96L,则被还原的硝酸的物质的量是______ mol,参加反应的硝酸的物质的量是_____ mol,产生混合气体中NO和NO2体积比为______________ 。
(1)硝酸在该反应中表现出的性质是
(2)0.3mol Cu被一定浓度的硝酸完全溶解后,如果此时产生的的NO和NO2气体总体积在标准状况下8.96L,则被还原的硝酸的物质的量是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】根据下列各组信息,完成有关问题:
(1)根据反应Cu+4HNO3 (浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①还原产物是_______ 。
②未被还原的硝酸与参加反应的总硝酸的质量之比为_______ 。
(2)氢能是一种极具发展潜力的清洁能源,以太阳能为热源,热化学硫碳循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:
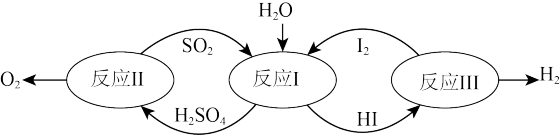
反应Ⅰ的化学方程式:_______
(3)KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,配平该反应的化学方程式,并在方程式上用单线桥标出电子转移:_______
_______KClO3+_______HCl(浓)=_______KCl+_______ClO2↑+_______Cl2↑+_______H2O
(4)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O
、Cl-、H2O
①写出并配平湿法制高铁酸钾反应的离子程式_______ 。
②每生成1个FeO 转移
转移_______ 个电子,若反应过程中转移了3个电子,则生产_______ 个还原产物。
(1)根据反应Cu+4HNO3 (浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①还原产物是
②未被还原的硝酸与参加反应的总硝酸的质量之比为
(2)氢能是一种极具发展潜力的清洁能源,以太阳能为热源,热化学硫碳循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:

反应Ⅰ的化学方程式:
(3)KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,配平该反应的化学方程式,并在方程式上用单线桥标出电子转移:
_______KClO3+_______HCl(浓)=_______KCl+_______ClO2↑+_______Cl2↑+_______H2O
(4)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO-、OH-、FeO
 、Cl-、H2O
、Cl-、H2O①写出并配平湿法制高铁酸钾反应的离子程式
②每生成1个FeO
 转移
转移
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】高锰酸钾(KMnO4)和双氧水(H2O2)都是常见物质。
(1)写出二者共同元素的原子最外层轨道表示式:___________ K在周期表的位置是 ___________ ;25Mn属于_____________ 族元素。
(2)双氧水(H2O2)和水都是极弱电解质,但H2O2比H2O更显酸性。若把H2O2看成是二元弱酸,请写出它在水中的电离方程式:_____________
(3)2g高锰酸钾溶于10ml水时溶液没有明显的温度变化,请解释理由__________________________________ ,氧化剂一般来说,酸性越强其氧化性也越强,因此常用酸化的高锰酸钾作氧化剂。用高锰酸钾法测定H2O2时,不能用HCl来酸化原因是_________________ ;
(4)往H2O2水溶液中滴入一滴酸性KMnO4溶液,从溶液内部析出大量无色气泡。写出可能的化学反应方程式。_____________________________________
(5)往H2O2水溶液中滴入酸性KMnO4溶液,下列方程式错误的是__________
A 3H2O2+2KMnO4+3H2SO4→K2SO4+2MnSO4+6H2O+4O2↑
B 5H2O2+2KMnO4+3H2SO4→K2SO4+2MnSO4+8H2O+5O2↑
C 7H2O2+2KMnO4+3H2SO4→K2SO4+2MnSO4+10H2O+6O2↑
D 9H2O2+2KMnO4+3H2SO4→K2SO4+2MnSO4+12H2O+7O2↑
(1)写出二者共同元素的原子最外层轨道表示式:
(2)双氧水(H2O2)和水都是极弱电解质,但H2O2比H2O更显酸性。若把H2O2看成是二元弱酸,请写出它在水中的电离方程式:
(3)2g高锰酸钾溶于10ml水时溶液没有明显的温度变化,请解释理由
(4)往H2O2水溶液中滴入一滴酸性KMnO4溶液,从溶液内部析出大量无色气泡。写出可能的化学反应方程式。
(5)往H2O2水溶液中滴入酸性KMnO4溶液,下列方程式错误的是
A 3H2O2+2KMnO4+3H2SO4→K2SO4+2MnSO4+6H2O+4O2↑
B 5H2O2+2KMnO4+3H2SO4→K2SO4+2MnSO4+8H2O+5O2↑
C 7H2O2+2KMnO4+3H2SO4→K2SO4+2MnSO4+10H2O+6O2↑
D 9H2O2+2KMnO4+3H2SO4→K2SO4+2MnSO4+12H2O+7O2↑
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氯酸钾和浓盐酸之间有下列反应:
 KClO3+
KClO3+ HCl(浓)=
HCl(浓)=  KCl +
KCl +  Cl2↑+
Cl2↑+ ClO2 +
ClO2 + H2O。
H2O。
(1)配平上述方程式_____________________ 。
(2)该反应氧化剂是__________ ,氧化产物是___________ 。
(3)当有0.4mol电子发生转移时,生成的氯气的体积为_____ L(标准状况)。被氧化的HCl的物质的量为____ mol。
(4)若分别用①KMnO4(还原产物是Mn2+)②MnO2(还原产物是Mn2+)③Ca(ClO)2(还原产物是Cl2)与浓盐酸反应制备氯气,当浓盐酸足量且这三种氧化剂的物质的量相同时,生成氯气的物质的量最少的是________ 。
 KClO3+
KClO3+ HCl(浓)=
HCl(浓)=  KCl +
KCl +  Cl2↑+
Cl2↑+ ClO2 +
ClO2 + H2O。
H2O。(1)配平上述方程式
(2)该反应氧化剂是
(3)当有0.4mol电子发生转移时,生成的氯气的体积为
(4)若分别用①KMnO4(还原产物是Mn2+)②MnO2(还原产物是Mn2+)③Ca(ClO)2(还原产物是Cl2)与浓盐酸反应制备氯气,当浓盐酸足量且这三种氧化剂的物质的量相同时,生成氯气的物质的量最少的是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】用化学方程式或离子方程式表示相应的化学反应.
(1)工业生产上将氯气通入石灰乳,在一定条件下蒸干可制漂白粉.写出该过程的化学方程式:_____________________ .
(2)侯氏制碱法中最后利用小苏打固体可以制得纯碱,写出该过程的化学方程式:_____________________ .
(3)向水玻璃溶液(Na2SiO3溶液)中,加入稀盐酸可用于生产硅酸胶体.用离子方程式表示该生产原理:_____________________ .
(4)硫酸工业中用氨水吸收二氧化硫,写出氨水吸收过量二氧化硫的离子方程式_______________________ .
(5)NO是大气污染物之一,目前一种治理方法是在400℃左右、在催化剂的作用下用氨气还原,写出化学方程式_____________________ .
(1)工业生产上将氯气通入石灰乳,在一定条件下蒸干可制漂白粉.写出该过程的化学方程式:
(2)侯氏制碱法中最后利用小苏打固体可以制得纯碱,写出该过程的化学方程式:
(3)向水玻璃溶液(Na2SiO3溶液)中,加入稀盐酸可用于生产硅酸胶体.用离子方程式表示该生产原理:
(4)硫酸工业中用氨水吸收二氧化硫,写出氨水吸收过量二氧化硫的离子方程式
(5)NO是大气污染物之一,目前一种治理方法是在400℃左右、在催化剂的作用下用氨气还原,写出化学方程式
您最近半年使用:0次
【推荐1】化学与我们的生活、生产、环境等息息相关。回答下列问题:
(1)维生素C能帮助人体将从食物中摄取的、不易吸收的 转变为易吸收的
转变为易吸收的 ,这说明维生素C具有
,这说明维生素C具有___________ 性,该转化反应中 作
作___________ 剂。
(2)ClO2是一种消毒效率高、污染小的水处理剂,实验室可通过以下反应制得: (未配平),在相同条件下,反应中产生的
(未配平),在相同条件下,反应中产生的 与
与 的分子个数比是
的分子个数比是___________ 。
(3)在鲜活鱼的长途运输中,需在水中加入供氧剂。 (易溶于水)、
(易溶于水)、 (微溶于水)都可与水发生反应生成碱和氧气,这两种物质中选
(微溶于水)都可与水发生反应生成碱和氧气,这两种物质中选___________ 作为供氧剂更好,理由是___________ 。
(4)氢化钙(CaH2)固体是登山运动员常用的能源提供剂,写出CaH2与水反应的化学方程式:___________ ,当有2.1gCaH2完全反应时转移电子的数目为___________  。
。
(1)维生素C能帮助人体将从食物中摄取的、不易吸收的
 转变为易吸收的
转变为易吸收的 ,这说明维生素C具有
,这说明维生素C具有 作
作(2)ClO2是一种消毒效率高、污染小的水处理剂,实验室可通过以下反应制得:
 (未配平),在相同条件下,反应中产生的
(未配平),在相同条件下,反应中产生的 与
与 的分子个数比是
的分子个数比是(3)在鲜活鱼的长途运输中,需在水中加入供氧剂。
 (易溶于水)、
(易溶于水)、 (微溶于水)都可与水发生反应生成碱和氧气,这两种物质中选
(微溶于水)都可与水发生反应生成碱和氧气,这两种物质中选(4)氢化钙(CaH2)固体是登山运动员常用的能源提供剂,写出CaH2与水反应的化学方程式:
 。
。
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】科学家在研究化学物质时,常常对物质进行分类,以便对同类物质的组成和性能进行深入的研究。物质分类及转化思想贯穿整个化学科学习的始终。
(1)有下列十种物质:
A.空气
B.O2
C.NaHSO4
D.氨水
E.CuSO4
F.NaOH
G.CO2
H.Fe2O3
I.金刚石
J.H2SO4
其中属于非电解质的有____________ ;属于盐的有____________ 。(填字母)
(2)有下列六个反应:
A.Cl2+H2O=HCl+HClO
B.Zn+H2SO4=ZnSO4+H2↑
C.2Cu2O+Cu2S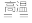 6Cu+SO2↑
6Cu+SO2↑
D.Cl2+2KI=2KCl+I2
E.H2+Cl2===2HCl
F.2KClO3 2KCl+3O2↑
2KCl+3O2↑
其中既属于分解反应又属于氧化还原反应的是____________ (填字母)。
(3)K2FeO4是一种重要的净水剂,可用下列方法制得:
2Fe(OH)3+3Cl2+10KOH 2K2FeO4+6KCl+8H2O
2K2FeO4+6KCl+8H2O
在该反应中,还原剂是____________ (填化学式),当反应中有1mol K2FeO4生成时,转移电子的数目为____________ 。
(1)有下列十种物质:
A.空气
B.O2
C.NaHSO4
D.氨水
E.CuSO4
F.NaOH
G.CO2
H.Fe2O3
I.金刚石
J.H2SO4
其中属于非电解质的有
(2)有下列六个反应:
A.Cl2+H2O=HCl+HClO
B.Zn+H2SO4=ZnSO4+H2↑
C.2Cu2O+Cu2S
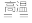 6Cu+SO2↑
6Cu+SO2↑D.Cl2+2KI=2KCl+I2
E.H2+Cl2===2HCl
F.2KClO3
 2KCl+3O2↑
2KCl+3O2↑其中既属于分解反应又属于氧化还原反应的是
(3)K2FeO4是一种重要的净水剂,可用下列方法制得:
2Fe(OH)3+3Cl2+10KOH
 2K2FeO4+6KCl+8H2O
2K2FeO4+6KCl+8H2O在该反应中,还原剂是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反应体系,共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质。
(1)该反应中,化合价升高的反应物是__ ,化合价没有发生变化的反应物是__ 。
(2)写出一个包含上述七种物质的氧化还原反应方程式(需配平)__ 。
(3)上述反应中,氧化剂是__ ,1mol氧化剂在反应中__ (填“得到”或“失去”)__ mol电子。
(4)如果在反应后的溶液中加入NaBiO3,溶液又显紫红色。此现象说明NaBiO3具有__ (填“氧化性”或“还原性”)。写出该反应的离子方程式:__ 。
(提示:NaBiO3为黄色或棕色粉末,不溶于冷水,在该反应中转化为Bi3+)
(1)该反应中,化合价升高的反应物是
(2)写出一个包含上述七种物质的氧化还原反应方程式(需配平)
(3)上述反应中,氧化剂是
(4)如果在反应后的溶液中加入NaBiO3,溶液又显紫红色。此现象说明NaBiO3具有
(提示:NaBiO3为黄色或棕色粉末,不溶于冷水,在该反应中转化为Bi3+)
您最近半年使用:0次



