蛋白质中含有C、H、O、N、S等元素,食物中的铁主要以三价铁与蛋白质和羧酸钴结合成络台物的形式存在。
(1)在蛋白质中涉及的氮、氧元素电负性由小到大的顺序是______ ,基态硫原子的价电子排布式为_______ 。
(2)KSCN是检验Fe3+的试剂之一,与SCN-互为等电子体的一种分子为_______ (填化学式),1mol/LCN-中含有的π键的数目为_________ 。
(3)血液中有一种含铜的呈蓝色的蛋白质分子,与Cu同周期且最外层电子数相等的元素还有______ (填元素符号)
(1)在蛋白质中涉及的氮、氧元素电负性由小到大的顺序是
(2)KSCN是检验Fe3+的试剂之一,与SCN-互为等电子体的一种分子为
(3)血液中有一种含铜的呈蓝色的蛋白质分子,与Cu同周期且最外层电子数相等的元素还有
更新时间:2020-11-14 03:18:10
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按要求完成下列各小题
(1)写出钙的核外电子排布式_________________________________________
(2)画出氟的价电子轨道表示式_______________________________________
(3)写出含有一个手性碳原子的分子__________________________________
(4)写出甲烷中σ键的具体类型(即参与成键的原子轨道)_______________
(1)写出钙的核外电子排布式
(2)画出氟的价电子轨道表示式
(3)写出含有一个手性碳原子的分子
(4)写出甲烷中σ键的具体类型(即参与成键的原子轨道)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】生活离不开化学,生活中有许多中学化学常见的物质,它们的主要成分如下表:
回答下列问题:
(1) 中所含化学键类型为
中所含化学键类型为___________ (填“离子键”或“共价键”)。
(2)明矾可用来制备氢氧化铝,请选择与之反应的最佳试剂:___________ (填“氨水”或“氢氧化钠溶液”)。
(3) 的电离方程式为
的电离方程式为___________ 。
(4) 溶液中混有少量
溶液中混有少量 ,可加适量的
,可加适量的 溶液除杂,离子方程式为
溶液除杂,离子方程式为___________ , 固体中若含有少量
固体中若含有少量 固体,可采取的除杂方法为
固体,可采取的除杂方法为___________ 。
(5)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:___________ 。
(6) 属于
属于___________ 电解质(填“强”、“弱”或“非”)。
| 商品 | 食盐 | 明矾 | 84消毒液 |
| 主要成分 | ① | ② | ③ |
| 商品 | 发酵粉 | 白醋 | 洁厕灵 |
| 主要成分 | ④ | ⑤ | ⑥ |
(1)
 中所含化学键类型为
中所含化学键类型为(2)明矾可用来制备氢氧化铝,请选择与之反应的最佳试剂:
(3)
 的电离方程式为
的电离方程式为(4)
 溶液中混有少量
溶液中混有少量 ,可加适量的
,可加适量的 溶液除杂,离子方程式为
溶液除杂,离子方程式为 固体中若含有少量
固体中若含有少量 固体,可采取的除杂方法为
固体,可采取的除杂方法为(5)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:
(6)
 属于
属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】乙醇俗称酒精,在生活中使用广泛。
资料1:乙醇分子有两个末端,一端是憎水(易溶于油)的—C2H5;一端是亲水(易溶于水)的—OH。
资料2:破坏蛋白质分子中形成蜷曲和螺旋的各种力,使长链舒展、松弛,可导致蛋白质变性。
资料3:水分子可以松弛蛋白质外部亲水基团之间的吸引力,而—OH不能;—C2H5可以破坏蛋白质内部憎水基团之间的吸引力。
(1)乙醇的结构及性质
①1mol乙醇分子中的极性共价键有___________ mol。
②从结构角度解释乙醇的沸点比乙烷高的原因____________________ 。
(2)乙醇的用途
①医用酒精(75%)制备过程与制酒的过程类似,不能饮用,但可接触人体医用。

结合题中资料,下列说法正确的是________________ (填字母)。
a.糖化、发酵的过程均含有化学变化
b.获得医用酒精常采用的分离提纯方法是蒸馏
c.浓度99%的酒精消毒杀菌效果一定大于75%的酒精
②乙醇是一种很好的溶剂,在油脂的皂化反应中,加入乙醇可加快反应速率,其原因是______________ 。
(3)乙醇的工业制取
乙醇的工业制取方法很多,由碳的氧化物直接合成乙醇燃料已进入大规模生产。下图是由二氧化碳合成乙
醇的工艺流程。
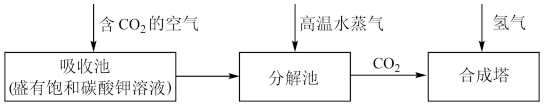
该流程中能循环使用的物质是_________________________ 。
资料1:乙醇分子有两个末端,一端是憎水(易溶于油)的—C2H5;一端是亲水(易溶于水)的—OH。
资料2:破坏蛋白质分子中形成蜷曲和螺旋的各种力,使长链舒展、松弛,可导致蛋白质变性。
资料3:水分子可以松弛蛋白质外部亲水基团之间的吸引力,而—OH不能;—C2H5可以破坏蛋白质内部憎水基团之间的吸引力。
(1)乙醇的结构及性质
①1mol乙醇分子中的极性共价键有
②从结构角度解释乙醇的沸点比乙烷高的原因
(2)乙醇的用途
①医用酒精(75%)制备过程与制酒的过程类似,不能饮用,但可接触人体医用。

结合题中资料,下列说法正确的是
a.糖化、发酵的过程均含有化学变化
b.获得医用酒精常采用的分离提纯方法是蒸馏
c.浓度99%的酒精消毒杀菌效果一定大于75%的酒精
②乙醇是一种很好的溶剂,在油脂的皂化反应中,加入乙醇可加快反应速率,其原因是
(3)乙醇的工业制取
乙醇的工业制取方法很多,由碳的氧化物直接合成乙醇燃料已进入大规模生产。下图是由二氧化碳合成乙
醇的工艺流程。

该流程中能循环使用的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题。
(1)Fe成为阳离子时首先失去___________ 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为___________ 。
(2)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为___________ 、___________ (填标号)。
A. B.
B.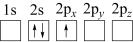
C. D.
D.
(3)基态Fe原子价层电子的电子排布图(轨道表达式)为___________ ,基态S原子电子占据最高能级的电子云轮廓图为___________ 形。
(1)Fe成为阳离子时首先失去
(2)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
 D.
D.
(3)基态Fe原子价层电子的电子排布图(轨道表达式)为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】中国炼丹家约在唐代或五代时期掌握了以炉甘石点化鍮石(即鍮石金)的技艺:将炉甘石(ZnCO3)、赤铜矿(主要成分Cu2O)和木炭粉混合加热至800℃左右可制得与黄金相似的鍮石金。回答下列问题:
(1)锌元素基态原子的价电子排布式为________________ ,铜元素基态原子中的未成对电子数为_________________ 。
(2)硫酸锌溶于过量氨水形成[ Zn(NH3)4]SO4溶液。
①[Zn(NH3)4]SO4中,阴离子的立体构型是__________________ ,[Zn(NH3)4]2+中含有的化学键有__________________ 。
②NH3分子中,中心原子的轨道杂化类型为________________ ,NH3在H2O中的溶解度____________ (填“大”或“小”),原因是_____________________ 。
(3)铜的第一电离能为I1Cu=745.5kJ·mol-1,第二电离能为I2Cu=1957.9kJ·mol-1,锌的第一电离能为I1Zn=906.4kJ·mol-1,第二电离能为I2Zn=1733.3kJ·mol-1,I2Cu>I2Zn的原因是___________________ 。
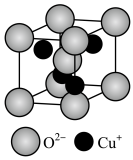
(4)Cu2O晶体的晶胞结构如图所示。O2-的配位数为_______________ ;若Cu2O的密度为dg·cm-3,则晶胞参数a=____________ nm。
(1)锌元素基态原子的价电子排布式为
(2)硫酸锌溶于过量氨水形成[ Zn(NH3)4]SO4溶液。
①[Zn(NH3)4]SO4中,阴离子的立体构型是
②NH3分子中,中心原子的轨道杂化类型为
(3)铜的第一电离能为I1Cu=745.5kJ·mol-1,第二电离能为I2Cu=1957.9kJ·mol-1,锌的第一电离能为I1Zn=906.4kJ·mol-1,第二电离能为I2Zn=1733.3kJ·mol-1,I2Cu>I2Zn的原因是
(4)Cu2O晶体的晶胞结构如图所示。O2-的配位数为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)根据Mn原子的核外电子排布情况,回答下列问题:
①价层电子排布图为_______ 。
②在Mn原子的核外电子中,有_______ 种运动状态不同的电子,最高化合价为_______ 。
(2)基态Fe2+与Fe3+离子中未成对的电子数之比为_______ ,Sm的价层电子排布式4f66s2,Sm3+的价层电子排布式为_______ 。
(3)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为_______ ,该能层具有的原子轨道数为_______ ,电子占据最高能级的电子云轮廓图为_______ 形。
②Li、B、H元素的电负性由大到小的排列顺序为_______ 。离子半径Li+_______ H-(填“>”“=”或“<”)。
(4)查表得知,元素X的电负性是1.5,元素Y的电负性是3.0,请判断X是_______ (填“金属”或“非金属”),元素X与元素Y形成的化合物属于_______ (填“离子化合物”或“共价化合物”),该化合物中显负价的是_______ (填“X”或“Y”)。
(1)根据Mn原子的核外电子排布情况,回答下列问题:
①价层电子排布图为
②在Mn原子的核外电子中,有
(2)基态Fe2+与Fe3+离子中未成对的电子数之比为
(3)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为
②Li、B、H元素的电负性由大到小的排列顺序为
(4)查表得知,元素X的电负性是1.5,元素Y的电负性是3.0,请判断X是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】黑火药的爆炸反应为2KNO3+3C+S A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)
(1)除S外,上列元素的电负性从大到小依次为______________________ 。
(2)在生成物中,A的晶体类型为____________ 、其电子式为___________ 。
(3)含极性共价键的分子的中心原子轨道杂化类型为____________________ 。
(4)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为________ 。
 A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)(1)除S外,上列元素的电负性从大到小依次为
(2)在生成物中,A的晶体类型为
(3)含极性共价键的分子的中心原子轨道杂化类型为
(4)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】碳氢氟氮硅等非金属元素与人类的生产生活息息相关。回答下列问题:
(1)写出硅原子的电子排布式___________ 。C、Si、N的电负性由大到小的顺序是___________ 。
(2)氟化氢水溶液中存在氢键有___________ 种。
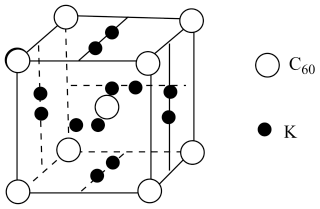
(3)科学家把C60和K掺杂在一起制造了一种富勒烯与钾的化合物,该物质在低温时是一种超导体,其晶胞如图所示,该物质中K原子和C60分子的个数比为___________ 。
(4)继C60后,科学家又合成了Si60、N60.请解释如下现象:熔点:Si60>N60>C60,而破坏分子所需要的能量:N60>C60>Si60,其原因是:___________ 。
(1)写出硅原子的电子排布式
(2)氟化氢水溶液中存在氢键有
(3)科学家把C60和K掺杂在一起制造了一种富勒烯与钾的化合物,该物质在低温时是一种超导体,其晶胞如图所示,该物质中K原子和C60分子的个数比为

(4)继C60后,科学家又合成了Si60、N60.请解释如下现象:熔点:Si60>N60>C60,而破坏分子所需要的能量:N60>C60>Si60,其原因是:
您最近一年使用:0次



