SiC纳米材料可望在电场发射材料、储氢、光催化和传感等领域都有广泛的应用前景。科学家用金属钠还原CCl4和SiCl4制得一种一维SiC纳米棒,相关反应的化学方程式为8Na+CCl4+ SiCl4=SiC+8NaCl。下列说法不正确的是.
| A.一维SiC纳米棒“比表面积”大,对微小粒子有较强的吸附能力 |
| B.上述反应中SiC既是氧化产物又是还原产物 |
| C.每生成l mol SiC转移8 mol电子 |
| D.CCl4、SiCl4分子中各原子都达到了8电子稳定结构 |
2020·全国·模拟预测 查看更多[2]
更新时间:2020-11-24 16:25:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】(Te)与氧元素同族,在元素周期表中与硒(Se)相邻,位于硒(Se)的下方。含元素碲(Te)的几种物质存在如图所示转化关系。下列说法错误的是
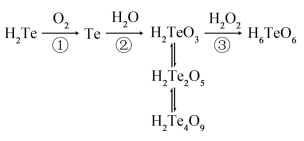

A.反应①利用了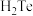 的还原性 的还原性 |
| B.碲(Te)位于元素周期表中第五周期第ⅥA族 |
C.反应③利用了 的氧化性 的氧化性 |
| D.H2Te2O5转化为H2Te4O9发生了氧化还原反应 |
您最近半年使用:0次
单选题
|
适中
(0.65)
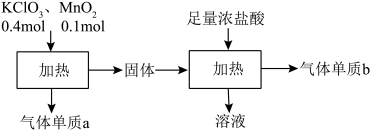
【推荐2】运动会上的发令枪所用“火药”的主要成分是氯酸钾和红磷,经撞击发出响声,同时产生白烟。撞击时发生反应的化学方程式: 。则下列有关叙述错误的是
。则下列有关叙述错误的是
 。则下列有关叙述错误的是
。则下列有关叙述错误的是A.该反应属于氧化还原反应, 为氧化反应的产物 为氧化反应的产物 |
B.该反应中n(氧化剂):n(还原剂) |
C.该反应中消耗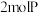 时,转移 时,转移 电子 电子 |
D.白烟是由于剧烈反应生成的白色固体小颗粒 和 和 |
您最近半年使用:0次
【推荐3】四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备Fe3O4纳米颗粒的反应是3Fe2++2 +O2+xOH-=Fe3O4↓+
+O2+xOH-=Fe3O4↓+ +2H2O。下列问题叙述不正确的是( )
+2H2O。下列问题叙述不正确的是( )
 +O2+xOH-=Fe3O4↓+
+O2+xOH-=Fe3O4↓+ +2H2O。下列问题叙述不正确的是( )
+2H2O。下列问题叙述不正确的是( )A.水热法制备Fe3O4纳米颗粒的反应中,还原剂是 |
| B.反应的离子方程式中x=4 |
| C.每生成1molFe3O4,反应转移的电子为4mol |
| D.被Fe2+还原的O2的物质的量为0.5mol |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子。N4分子结构如图所示,下列说法正确的是


| A.N4分子属于一种新型的化合物 |
| B.N4分子中只含有非极性键 |
| C.1 mol N4分子所含共价键数为4NA |
| D.N4分子中只含有极性键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法中正确的有
①金属晶体的导电性、导热性均与自由电子有关
②离子键是阴、阳离子间的相互吸引作用
③分子晶体的熔点一定比金属晶体低
④共价键的强弱决定分子晶体熔、沸点的高低
⑤共价晶体中一定含有共价键
⑥含有离子的晶体一定是离子晶体
⑦硬度由大到小:金刚石>碳化硅>晶体硅
⑧NaCl晶体中,阴离子周围紧邻的阳离子数为8
①金属晶体的导电性、导热性均与自由电子有关
②离子键是阴、阳离子间的相互吸引作用
③分子晶体的熔点一定比金属晶体低
④共价键的强弱决定分子晶体熔、沸点的高低
⑤共价晶体中一定含有共价键
⑥含有离子的晶体一定是离子晶体
⑦硬度由大到小:金刚石>碳化硅>晶体硅
⑧NaCl晶体中,阴离子周围紧邻的阳离子数为8
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】设NA为阿伏加德罗常数的值。下列说法正确的是
| A.向FeI2溶液中通入适量Cl2,当有1 mol Fe2+被氧化时,转移的电子数为NA |
| B.12g 金刚石中含碳碳单键的数目为2NA |
| C.一定条件下,丁烷催化裂解生成1mol乙烯时,消耗丁烷的数目一定为NA |
| D.1 mol CH2=CH-CH3分子中有NA个π键、2NA个σ键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】关于反应4CO2+SiH4 4CO+2H2O+SiO2,已知SiH4和SiO2中硅元素的化合价相同,下列说法正确的是
4CO+2H2O+SiO2,已知SiH4和SiO2中硅元素的化合价相同,下列说法正确的是
 4CO+2H2O+SiO2,已知SiH4和SiO2中硅元素的化合价相同,下列说法正确的是
4CO+2H2O+SiO2,已知SiH4和SiO2中硅元素的化合价相同,下列说法正确的是| A.H2O是氧化产物 | B.SiH4发生还原反应 |
| C.氧化剂与还原剂的分子个数之比为1∶4 | D.生成1个H2O时,转移2个电子 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温常压下,26.4gCO2和N2O的混合气体所含氧原子的数目为0.9NA |
B.200mL0.2 NaHCO3溶液,所含 NaHCO3溶液,所含 数目为0.04NA 数目为0.04NA |
| C.标准状况下,1.12LH2O所含质子的数目为0.5NA |
| D.将一定量Na2O2溶于足量盐酸,当产生1.6gO2时转移电子的数目为0.1NA |
您最近半年使用:0次