铜和稀硝酸发生反应的化学方程式为:3Cu +8HNO3(稀)=3Cu(NO3)2 + 2NO↑+ 4H2O
(1)请将上述反应改写为离子方程式,并标出电子转移方向和数目 :_____________ 。
(2)其中被还原元素是______ ,被还原与未被还原的HNO3的质量之比为_____ 。
(3)在该反应中,若生成NO气体(标准状况下)4.48 L,则消耗了________ g Cu,转移了_____ mol 电子 ,被还原的HNO3的物质的量是_______ 。
(1)请将上述反应改写为离子方程式,并
(2)其中被还原元素是
(3)在该反应中,若生成NO气体(标准状况下)4.48 L,则消耗了
更新时间:2020-12-09 14:16:54
|
相似题推荐
【推荐1】回答下列问题:
(1)现有以下物质:①NaOH溶液;②液氨;③BaCO3固体;④熔融NaHSO4;⑤Fe(OH)3胶体;⑥铜;⑦CO2;⑧CH3COOH;⑨蔗糖;
(i)以上物质中属于电解质的是_______ (填序号);以上纯净物中能导电的是_______ (填序号)。
(ii)写出制备物质⑤的方程式_______ 。
(iii)写出④的电离方程式_______ 。
(iV)上述物质中两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为_______
(V)在含40 g溶质的①溶液中缓缓通入标准状况下35.2 g CO2,则该过程的离子反应方程式为_______ 。
(2)已知一定条件可发生如下反应:NO+NH3=H2O+N2
①配平上述方程式,并用双线桥表示该反应中电子转移的方向和数目_______
②若有3.4 g氨气发生反应,则反应所得还原产物与氧化产物的质量差为_______
(1)现有以下物质:①NaOH溶液;②液氨;③BaCO3固体;④熔融NaHSO4;⑤Fe(OH)3胶体;⑥铜;⑦CO2;⑧CH3COOH;⑨蔗糖;
(i)以上物质中属于电解质的是
(ii)写出制备物质⑤的方程式
(iii)写出④的电离方程式
(iV)上述物质中两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为
(V)在含40 g溶质的①溶液中缓缓通入标准状况下35.2 g CO2,则该过程的离子反应方程式为
(2)已知一定条件可发生如下反应:NO+NH3=H2O+N2
①配平上述方程式,并用双线桥表示该反应中电子转移的方向和数目
②若有3.4 g氨气发生反应,则反应所得还原产物与氧化产物的质量差为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】3H2O2 + 2H2CrO4 =2 Cr(OH)3 + 3O2 ↑+ 2H2O
(1)其中Cr被___________ ,H2O2作____________ 剂。
(2)_____________ 是氧化产物,_______________ 发生还原反应。
(3)反应转移了0.3mol电子,则产生的气体在标准状态下体积约为__________ 。
(4)用单线桥标明电子转移的方向和数目。_______
(1)其中Cr被
(2)
(3)反应转移了0.3mol电子,则产生的气体在标准状态下体积约为
(4)用单线桥标明电子转移的方向和数目。
您最近半年使用:0次
【推荐3】按要求填空。
(1)配平氧化还原离子方程式:____Cu+_____NO +_____H+ =_____NO↑+____Cu2++_____H2O
+_____H+ =_____NO↑+____Cu2++_____H2O ___________
(2)已知KMnO4 与浓盐酸室温下可发生如下反应:2KMnO4 +16HCl浓=2KCl+2MnCl2 +5Cl2 +8H2O
①用“双线桥法”标出上述反应的电子转移情况。__________ 2KMnO4 +16HCl浓=2KCl+2MnCl2 +5Cl2 +8H2O
②该反应的离子反应方程式为___________ ,此反应体现 HCl的___________ 性和___________ 性,氧化剂与还原剂个数比为___________ , 生成 71gCl2 时消耗的还原剂的质量为___________ g
③若分别用①KMnO4(还原产物是 Mn2+);②MnO2+(还原产物是 Mn2+)氧化浓盐酸制备氯气,当浓盐酸足量且消耗 KMnO4 和 MnO2+这两种氧化剂的数目相同时,生成氯气分子的数目之比是___________ 。
(1)配平氧化还原离子方程式:____Cu+_____NO
 +_____H+ =_____NO↑+____Cu2++_____H2O
+_____H+ =_____NO↑+____Cu2++_____H2O (2)已知KMnO4 与浓盐酸室温下可发生如下反应:2KMnO4 +16HCl浓=2KCl+2MnCl2 +5Cl2 +8H2O
①用“双线桥法”标出上述反应的电子转移情况。
②该反应的离子反应方程式为
③若分别用①KMnO4(还原产物是 Mn2+);②MnO2+(还原产物是 Mn2+)氧化浓盐酸制备氯气,当浓盐酸足量且消耗 KMnO4 和 MnO2+这两种氧化剂的数目相同时,生成氯气分子的数目之比是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】含氯化合物的应用越来越广泛,请完成下列有关问题:
(1)亚氯酸钠( )是一种漂白织物的漂白剂,具有较强的氧化性。亚氯酸钠中氯元素的化合价为
)是一种漂白织物的漂白剂,具有较强的氧化性。亚氯酸钠中氯元素的化合价为_______ ,其水溶液显碱性的原因为_______ ,其水溶液中离子浓度由大到小的顺序为_______ 。
(2)亚氯酸钠在碱性溶液中稳定,在酸性溶液中生成 和氯元素的另一种稳定离子,写出亚氯酸钠在酸性条件下反应的离子方程式
和氯元素的另一种稳定离子,写出亚氯酸钠在酸性条件下反应的离子方程式_______ 。
(3) 是一种新型安全多功能型杀菌剂,其制备方法有多种,其中一种为
是一种新型安全多功能型杀菌剂,其制备方法有多种,其中一种为 通入
通入 中可得
中可得 ,其氧化剂与还原剂的物质的量之比为
,其氧化剂与还原剂的物质的量之比为_______ 。
(4)一定条件下, 与硫酸酸化的草酸(
与硫酸酸化的草酸( )溶液反应可制备
)溶液反应可制备 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
(5) 溶液可以用来检验水溶液中的
溶液可以用来检验水溶液中的 或
或 。若向
。若向 悬浊液中加入
悬浊液中加入 溶液,可把
溶液,可把 转化为
转化为 ,已知
,已知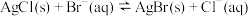 达到平衡时,
达到平衡时, ,已知
,已知 ,则
,则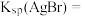
_______ 。(保留两位有效数字,不写单位)
(1)亚氯酸钠(
 )是一种漂白织物的漂白剂,具有较强的氧化性。亚氯酸钠中氯元素的化合价为
)是一种漂白织物的漂白剂,具有较强的氧化性。亚氯酸钠中氯元素的化合价为(2)亚氯酸钠在碱性溶液中稳定,在酸性溶液中生成
 和氯元素的另一种稳定离子,写出亚氯酸钠在酸性条件下反应的离子方程式
和氯元素的另一种稳定离子,写出亚氯酸钠在酸性条件下反应的离子方程式(3)
 是一种新型安全多功能型杀菌剂,其制备方法有多种,其中一种为
是一种新型安全多功能型杀菌剂,其制备方法有多种,其中一种为 通入
通入 中可得
中可得 ,其氧化剂与还原剂的物质的量之比为
,其氧化剂与还原剂的物质的量之比为(4)一定条件下,
 与硫酸酸化的草酸(
与硫酸酸化的草酸( )溶液反应可制备
)溶液反应可制备 ,该反应的离子方程式为
,该反应的离子方程式为(5)
 溶液可以用来检验水溶液中的
溶液可以用来检验水溶液中的 或
或 。若向
。若向 悬浊液中加入
悬浊液中加入 溶液,可把
溶液,可把 转化为
转化为 ,已知
,已知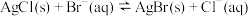 达到平衡时,
达到平衡时, ,已知
,已知 ,则
,则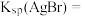
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】附加题
次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性。回答下列问题。
(1)H3PO2与足量的NaOH溶液反应,生成NaH2PO2,则H3PO2为________ 元酸。
(2)H3PO2是中强酸,写出其与NaHCO3溶液反应的离子方程式_______ 。
(3)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。
①H3PO2中,P元素的化合价为__________ ;
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为_______ (填化学式);
(4)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应,写出白磷与Ba(OH)2溶液反应的化学方程式______________________ 。
次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性。回答下列问题。
(1)H3PO2与足量的NaOH溶液反应,生成NaH2PO2,则H3PO2为
(2)H3PO2是中强酸,写出其与NaHCO3溶液反应的离子方程式
(3)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。
①H3PO2中,P元素的化合价为
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为
(4)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应,写出白磷与Ba(OH)2溶液反应的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】请按照要求用对应的化学术语回答下列问题。
(1) 是一种酸式盐,请写出
是一种酸式盐,请写出 在水中的电离方程式
在水中的电离方程式___________ 。
(2)将饱和 溶液滴入到沸水中,继续煮沸至液体变为红褐色,反应的离子方程式为
溶液滴入到沸水中,继续煮沸至液体变为红褐色,反应的离子方程式为___________ 。
(3) 可以作为供氧剂,其与
可以作为供氧剂,其与 反应时若生成标准状况下11.2L
反应时若生成标准状况下11.2L  ,则电子转移数目为
,则电子转移数目为___________ 。
(4) 溶于水可以产生具有漂白性的物质,
溶于水可以产生具有漂白性的物质, 与水反应的离子方程式为:
与水反应的离子方程式为:___________ 。
(5)某温度下将 通入KOH溶液里,反应后得到KCl、KClO、
通入KOH溶液里,反应后得到KCl、KClO、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为11∶1,则
的个数之比为11∶1,则 与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为___________ 。
(6)在标准状况下,将V L氨气溶于0.1L水中,所得溶液的密度为 ,则此氨水的物质的量浓度为
,则此氨水的物质的量浓度为___________  。
。
(1)
 是一种酸式盐,请写出
是一种酸式盐,请写出 在水中的电离方程式
在水中的电离方程式(2)将饱和
 溶液滴入到沸水中,继续煮沸至液体变为红褐色,反应的离子方程式为
溶液滴入到沸水中,继续煮沸至液体变为红褐色,反应的离子方程式为(3)
 可以作为供氧剂,其与
可以作为供氧剂,其与 反应时若生成标准状况下11.2L
反应时若生成标准状况下11.2L  ,则电子转移数目为
,则电子转移数目为(4)
 溶于水可以产生具有漂白性的物质,
溶于水可以产生具有漂白性的物质, 与水反应的离子方程式为:
与水反应的离子方程式为:(5)某温度下将
 通入KOH溶液里,反应后得到KCl、KClO、
通入KOH溶液里,反应后得到KCl、KClO、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为11∶1,则
的个数之比为11∶1,则 与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为(6)在标准状况下,将V L氨气溶于0.1L水中,所得溶液的密度为
 ,则此氨水的物质的量浓度为
,则此氨水的物质的量浓度为 。
。
您最近半年使用:0次



