附加题
次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性。回答下列问题。
(1)H3PO2与足量的NaOH溶液反应,生成NaH2PO2,则H3PO2为________ 元酸。
(2)H3PO2是中强酸,写出其与NaHCO3溶液反应的离子方程式_______ 。
(3)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。
①H3PO2中,P元素的化合价为__________ ;
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为_______ (填化学式);
(4)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应,写出白磷与Ba(OH)2溶液反应的化学方程式______________________ 。
次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性。回答下列问题。
(1)H3PO2与足量的NaOH溶液反应,生成NaH2PO2,则H3PO2为
(2)H3PO2是中强酸,写出其与NaHCO3溶液反应的离子方程式
(3)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。
①H3PO2中,P元素的化合价为
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为
(4)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应,写出白磷与Ba(OH)2溶液反应的化学方程式
更新时间:2019-01-30 18:14:09
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氯气和氯的化合物在生产、生活中具有广泛的用途。
(1)氯酸钾与浓盐酸在一定温度下反应会生成黄色的易爆物二氧化氯,反应的化学方程式为:KClO3 + HCl(浓)→KCl + ClO2↑+ Cl2↑+ H2O(未配平)
①配平该反应程式:______
②浓盐酸在该反应中表现的性质是______ (填序号)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸
③上述反应产生14.2 g Cl2时,转移的电子数目为______ 。
(2)下面三个方法都可以用来制氯气:
①2HCl(浓)+NaClO=NaCl+Cl2↑+H2O
②KClO3+6HCl=3Cl2↑+KCl+3H2O
③2KMnO4+16HCl(浓)=2 KCl+2MnCl2+5Cl2↑+8H2O
在反应③中,氧化剂与还原剂的物质的量之比为______ 。若要制得相同质量的氯气,三个反应中转移电子的数目之比(①:②:③)为______ 。
(1)氯酸钾与浓盐酸在一定温度下反应会生成黄色的易爆物二氧化氯,反应的化学方程式为:KClO3 + HCl(浓)→KCl + ClO2↑+ Cl2↑+ H2O(未配平)
①配平该反应程式:
②浓盐酸在该反应中表现的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸
③上述反应产生14.2 g Cl2时,转移的电子数目为
(2)下面三个方法都可以用来制氯气:
①2HCl(浓)+NaClO=NaCl+Cl2↑+H2O
②KClO3+6HCl=3Cl2↑+KCl+3H2O
③2KMnO4+16HCl(浓)=2 KCl+2MnCl2+5Cl2↑+8H2O
在反应③中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。实验室制取氯气除了用浓盐酸和二氧化锰反应外还可利用下列反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,该反应的优点是反应产生氯气速度快、不需加热。请你根据所学知识回答下列问题:
(1)上述反应中_______ 是氧化剂,该反应中氧化产物与还原产物的物质量之比为_________ 。
(2)把氯气通入紫色石蕊溶液中,可以观察到的现象是:__________ 。
(3)实验室配制好2.0 mol·L-1的NaOH溶液,需要这种溶液__________ mL才能与2.24 L氯气(标准状况)恰好完全反应。
(4)已知Br2的水溶液因浓度不同而呈现橙色或红棕色,NaBr溶液中缓缓通入Cl2时,可以看到无色溶液逐渐变为红棕色,请写出对应的离子方程式并用双线桥法表示出电子转移情况:_________________ 。
(5)现需490 mL 2.0 mol·L-1 NaOH溶液:
①所需称量的氢氧化钠固体的质量是__________ 。
②上述实验需要的仪器有天平(含砝码)、药匙、烧杯、量筒、玻璃棒、胶头滴管、__________ 。
③在配制溶液的过程中,下列操作可能造成结果偏高的是__________ 。
(1)上述反应中
(2)把氯气通入紫色石蕊溶液中,可以观察到的现象是:
(3)实验室配制好2.0 mol·L-1的NaOH溶液,需要这种溶液
(4)已知Br2的水溶液因浓度不同而呈现橙色或红棕色,NaBr溶液中缓缓通入Cl2时,可以看到无色溶液逐渐变为红棕色,请写出对应的离子方程式并用双线桥法表示出电子转移情况:
(5)现需490 mL 2.0 mol·L-1 NaOH溶液:
①所需称量的氢氧化钠固体的质量是
②上述实验需要的仪器有天平(含砝码)、药匙、烧杯、量筒、玻璃棒、胶头滴管、
③在配制溶液的过程中,下列操作可能造成结果偏高的是
| A.定容时俯视 |
| B.容量瓶不干燥,含有少量蒸馏水 |
| C.溶解所用烧杯未洗涤 |
| D.NaOH溶解后,未冷却即进行实验 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上常用SO2除去原料气中少量CO生成物为S和氧和CO2。
(1)写出该反应的化学方程式为__________________________________________
(2)上述反应中,每减少2.24L气体(标准状况下)转移电子数为________________ 。
(3)上述反应所涉及的三种元素中原子半径从大到小的排列顺序为______________ ;三种元素非金属性由强到弱的顺序为__________________ ;反应所涉及的化合物中仅有一种是非极性分子,其电子式为_______________ 。
(1)写出该反应的化学方程式为
(2)上述反应中,每减少2.24L气体(标准状况下)转移电子数为
(3)上述反应所涉及的三种元素中原子半径从大到小的排列顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】常温下,浓度均为0.1mol·L-1的下列4种溶液:
①NaCN溶液 ②NaOH溶液 ③CH3COONa溶液 ④NaHCO3溶液
(1)①中各离子浓度由大到小的顺序是___ 。
(2)④的水解平衡常数Kh=___ 。
(3)若向等体积的③和④中滴加盐酸至呈中性,则消耗盐酸的体积③___ ④(填“>”、“<"、“=”)
(4)向NaCN溶液中通入少量CO2,则发生反应的离子方程式为:__ 。
①NaCN溶液 ②NaOH溶液 ③CH3COONa溶液 ④NaHCO3溶液
| HCN | H2CO3 | CH3COOH |
| Ka=4.9×10-10 | Ka1=4×10-7;Ka2=5.6×10-11 | Ka=1.7×10-5 |
(1)①中各离子浓度由大到小的顺序是
(2)④的水解平衡常数Kh=
(3)若向等体积的③和④中滴加盐酸至呈中性,则消耗盐酸的体积③
(4)向NaCN溶液中通入少量CO2,则发生反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】常温下 、
、 、
、 在水中的电离常数如下表:
在水中的电离常数如下表:
(1)下列能证明 是弱酸的事实是
是弱酸的事实是__________ (填标号)。
A 易挥发
易挥发
B 常温下, 溶液的pH约为3
溶液的pH约为3
C.将 的
的 溶液加水稀释10倍,溶液的
溶液加水稀释10倍,溶液的
D 等体积、等浓度的 溶液和盐酸分别与足量镁粉反应,产生氢气一样多
溶液和盐酸分别与足量镁粉反应,产生氢气一样多
(2)煤气化过程中产生的 可用足量
可用足量 溶液吸收,该反应的离子方程式为
溶液吸收,该反应的离子方程式为__________ 。
 、
、 、
、 在水中的电离常数如下表:
在水中的电离常数如下表:| 弱酸 | 电离常数/( ) ) |
 | 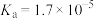 |
 |  |
 |  |
(1)下列能证明
 是弱酸的事实是
是弱酸的事实是A
 易挥发
易挥发B 常温下,
 溶液的pH约为3
溶液的pH约为3C.将
 的
的 溶液加水稀释10倍,溶液的
溶液加水稀释10倍,溶液的
D 等体积、等浓度的
 溶液和盐酸分别与足量镁粉反应,产生氢气一样多
溶液和盐酸分别与足量镁粉反应,产生氢气一样多(2)煤气化过程中产生的
 可用足量
可用足量 溶液吸收,该反应的离子方程式为
溶液吸收,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在一定温度下,有a.亚硫酸b.硝酸c.盐酸三种酸:
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是___________ (用字母表示,下同)。
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是___________ 。
(3)若三者pH相同时,物质的量浓度由大到小的顺序是___________ 。
(4)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是___________ 。
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是
(3)若三者pH相同时,物质的量浓度由大到小的顺序是
(4)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知硫化氢的水溶液为氢硫酸,它是一种二元弱酸,CuS为沉淀。
(1)H2S溶于水的电离方程式为_______ 。
(2)向H2S溶液中加入少量CuSO4溶液时,电离平衡向_______ (填“左”或“右”)移动,c(H+)_______ ,c(S2-)_______ (填“增大”或“减小”)。
(3)向H2S溶液中加入NaOH固体时,电离平衡向_______ (填“左”或“右”)移动,c(H+)_______ ,c(S2-)_______ (填“增大”或“减小”)。
(4)若要增大H2S溶液中c(S2-),最好加入_______ 。
(1)H2S溶于水的电离方程式为
(2)向H2S溶液中加入少量CuSO4溶液时,电离平衡向
(3)向H2S溶液中加入NaOH固体时,电离平衡向
(4)若要增大H2S溶液中c(S2-),最好加入
您最近一年使用:0次
【推荐2】气态亚硝酸(HNO2或HONO)是大气中的一种污染物。
(1)亚硝酸的电离平衡常数Ka=6.0×10﹣6,其电离方程式为________ 。
(2)亚硝酸分子中各原子最外层电子均达到稳定结构,其电子式为________ 。
(3)亚硝酸进入人体可以与二甲胺[(CH3)2NH]迅速反应生成亚硝酸胺[CH3)2N-N=O],亚硝酸胺是最重要的化学致癌物之一。
① 亚硝酸与二甲胺反应生成亚硝酸胺的一种反应机理如下:
HONO+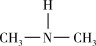

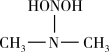

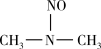
过程ⅰ和过程ⅱ的反应类型分别为:________ 、消去反应。
② 上述反应机理的反应过程与能量变化的关系如图:
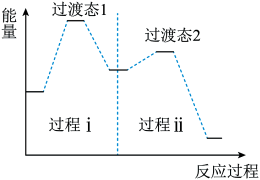
亚硝酸与二甲胺反应生成亚硝酸胺的反应ΔH________ 0(填“>”或“<”)。反应难度更大的是过程________ (填“ⅰ”或“ⅱ”)。
(1)亚硝酸的电离平衡常数Ka=6.0×10﹣6,其电离方程式为
(2)亚硝酸分子中各原子最外层电子均达到稳定结构,其电子式为
(3)亚硝酸进入人体可以与二甲胺[(CH3)2NH]迅速反应生成亚硝酸胺[CH3)2N-N=O],亚硝酸胺是最重要的化学致癌物之一。
① 亚硝酸与二甲胺反应生成亚硝酸胺的一种反应机理如下:
HONO+
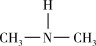



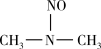
过程ⅰ和过程ⅱ的反应类型分别为:
② 上述反应机理的反应过程与能量变化的关系如图:

亚硝酸与二甲胺反应生成亚硝酸胺的反应ΔH
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知:草酸(H2C2O4)是一种常见的二元弱酸。请回答下列问题。
(1)草酸(H2C2O4)中碳元素的化合价为_______ 。
(2)依据氧化还原反应规律之价态规律可知草酸可能具有_______
A.只有氧化性 B.只有还原性 C.既有氧化性又有还原性
(3)请写出草酸(H2C2O4)在水溶液中的电离方程式_______ 。
(4)请写出草酸(H2C2O4)和氢氧化钠溶液反应的离子方程式_______ 。
(5)请配平草酸溶液和酸性高锰酸钾溶液发生反应的离子方程式 :_____
H2C2O4+ H ++ MnO = Mn2+ + H2O+ CO2↑
= Mn2+ + H2O+ CO2↑
(1)草酸(H2C2O4)中碳元素的化合价为
(2)依据氧化还原反应规律之价态规律可知草酸可能具有
A.只有氧化性 B.只有还原性 C.既有氧化性又有还原性
(3)请写出草酸(H2C2O4)在水溶液中的电离方程式
(4)请写出草酸(H2C2O4)和氢氧化钠溶液反应的离子方程式
(5)请配平草酸溶液和酸性高锰酸钾溶液发生反应的离子方程式 :
H2C2O4+ H ++ MnO
 = Mn2+ + H2O+ CO2↑
= Mn2+ + H2O+ CO2↑
您最近一年使用:0次



