已知2Na2O2+2H2O=4NaOH+O2↑回答下列问题:
(1)该反应中,氧化剂是____ ,还原剂是____ ,被氧化的元素是___ ,还原产物是____ ,氧化剂和还原剂的物质的量之比为____ ;
(2)该反应中,每生成标况下22.4 L O2转移电子的物质的量为___ ,反应的Na2O2的质量为__ 。
(1)该反应中,氧化剂是
(2)该反应中,每生成标况下22.4 L O2转移电子的物质的量为
更新时间:2020-12-31 16:43:38
|
相似题推荐
填空题
|
容易
(0.94)
解题方法
【推荐1】Kistiakowsky曾研究了NOCl光化学分解反应,在一定频率(ν)光的照射下机理为:NOCl+hν→NOCl*,NOCl+NOCl*→2NO+Cl2;其中hν表示一个光子能量,NOCl*表示NOCl的激发态。可知,分解1 mol的NOCl需要吸收_______ mol的光子
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】硅是重要的无机非金属材料。工业上用石英砂、焦炭为原料制粗硅,反应的化学高温方程式为SiO2+ 2C  Si+ 2CO↑。
Si+ 2CO↑。
(1)作还原剂的物质是___________ , 碳元素的化合价___________ (填 “升高”或“降低”)。
(2)反应中每生成1 mol Si,消耗SiO2的物质的量是___________ mol, 转移电子的物质的量是___________ mol。
 Si+ 2CO↑。
Si+ 2CO↑。(1)作还原剂的物质是
(2)反应中每生成1 mol Si,消耗SiO2的物质的量是
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐3】1774年,瑞典化学家舍勒发现软锰矿(主要成分是MnO2)和浓盐酸在一定条件下能反应产生一种黄绿色气体,命名为氯气。 实验室也可以用高锰酸钾和盐酸反应制氯气。
(1)写出该反应的离子方程式:______________________ 。
(2)当质量分数80%的高锰酸钾7.9g完全反应时,计算理论上生成标准状况下氯气体积___________ (假设杂质不参与反应)。
(1)写出该反应的离子方程式:
(2)当质量分数80%的高锰酸钾7.9g完全反应时,计算理论上生成标准状况下氯气体积
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐1】铜和浓硫酸发生反应的化学方程式为 Cu+2H2SO4(浓) CuSO4+ SO2↑+ 2H2O
CuSO4+ SO2↑+ 2H2O
(1)用双线桥标出电子转移的方向和数目___________ 。
(2)Cu作________ 剂,硫元素被_________ (填“氧化”或“还原”)。
 CuSO4+ SO2↑+ 2H2O
CuSO4+ SO2↑+ 2H2O(1)用双线桥标出电子转移的方向和数目
(2)Cu作
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐2】某校化学兴趣小组根据反应:H2O2+2HI=2H2O+I2探究影响化学反应速率的因素。实验数据如下:
回答下列问题:
(1)反应:H2O2+2HI=2H2O+I2中,氧化剂是___ 。
(2)25℃时,表明增大反应物浓度,化学反应速率___ (填“增大”或“减小”)。
(3)能表明温度对化学反应速率影响的实验编号是①和___ 。
(4)H2O2不稳定,写出H2O2发生分解反应的化学方程式:___ 。
| 实验 编号 | H2O2溶液浓度/(mol·L-1) | HI溶液浓度/(mol·L-1) | 温度/℃ | 反应速率/(mol·L-1·s-1) |
| ① | 0.1 | 0.1 | 25 | 0.0076 |
| ② | 0.1 | 0.2 | 25 | 0.0153 |
| ③ | 0.1 | 0.3 | 25 | 0.0227 |
| ④ | 0.1 | 0.1 | 35 | 0.0304 |
回答下列问题:
(1)反应:H2O2+2HI=2H2O+I2中,氧化剂是
(2)25℃时,表明增大反应物浓度,化学反应速率
(3)能表明温度对化学反应速率影响的实验编号是①和
(4)H2O2不稳定,写出H2O2发生分解反应的化学方程式:
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐1】氢化钠(NaH)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂为___________ 。(写化学式)
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】实验室可以用高锰酸钾和浓盐酸反应来制备氯气,反应的化学方程式为:2KMnO4 +16HCl→2KCl+2MnCl2+5Cl2↑+8H2O
(1)用单线桥标出上述反应电子转移的方向和数目。____
(2)该反应中氧化剂是___ ,被氧化的元素是___ ,若有1mol的KMnO4参加反应,则可以氧化___ mol的HCl,转移的电子数目为____ mol,得到的氯气的体积为___ L(标准状况下)。
(1)用单线桥标出上述反应电子转移的方向和数目。
(2)该反应中氧化剂是
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
【推荐1】高铁酸钾是一种新型水处理剂,使用说明书如下。
回答下列问题:
(1) 中铁元素的化合价为
中铁元素的化合价为___________ 。
(2)制备 需要在
需要在___________ (填“酸性”“碱性”或“中性”)环境中进行。
(3)下列关于 的说法中,错误的是
的说法中,错误的是___________ (填字母)。
a.是具有强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4) 与水反应生成
与水反应生成 胶体、
胶体、 和
和 反应的化学方程式为
反应的化学方程式为___________ ;该反应消耗 转移的电子数为
转移的电子数为___________  (
( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(5)消毒净化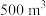 水,至少需要
水,至少需要 的质量为
的质量为___________  。
。
(6)产生 胶体时,该分散系区别于其他分散系的本质特征是
胶体时,该分散系区别于其他分散系的本质特征是___________ 。
| 高铁酸钾使用说明书 【化学式】  【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着  减小,稳定性下降。 减小,稳定性下降。 能与水反应放出氧气并通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 能与水反应放出氧气并通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 与水反应还能产生具有强吸附性的 与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用。 胶体,可除去水中细微的悬浮物,有净水作用。【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放 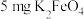 即可达到卫生标准 即可达到卫生标准 |
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)制备
 需要在
需要在(3)下列关于
 的说法中,错误的是
的说法中,错误的是a.是具有强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)
 与水反应生成
与水反应生成 胶体、
胶体、 和
和 反应的化学方程式为
反应的化学方程式为 转移的电子数为
转移的电子数为 (
( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(5)消毒净化
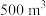 水,至少需要
水,至少需要 的质量为
的质量为 。
。(6)产生
 胶体时,该分散系区别于其他分散系的本质特征是
胶体时,该分散系区别于其他分散系的本质特征是
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】硅是重要的无机非金属材料。工业上用石英砂、焦炭为原料制粗硅,反应的化学高温方程式为SiO2+ 2C  Si+ 2CO↑。
Si+ 2CO↑。
(1)作还原剂的物质是___________ , 碳元素的化合价___________ (填 “升高”或“降低”)。
(2)反应中每生成1 mol Si,消耗SiO2的物质的量是___________ mol, 转移电子的物质的量是___________ mol。
 Si+ 2CO↑。
Si+ 2CO↑。(1)作还原剂的物质是
(2)反应中每生成1 mol Si,消耗SiO2的物质的量是
您最近一年使用:0次

 ______。
______。

