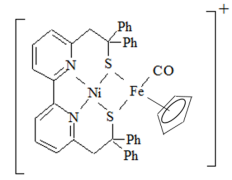
(1)Ni2+和Fe2+可形成如图所示的配合物离子,其中铁的一个配体为茂环阴离子( ),该配体以π电子参与配位,其中Ni2+的价电子排布式为
),该配体以π电子参与配位,其中Ni2+的价电子排布式为______ ,配合物离子中铁周围的价电子数共有______ 个,S元素的杂化方式为______ ,该配合物离子中的 (Ⅰ)和气态
(Ⅰ)和气态 分子(Ⅱ)的三键相比,键长较长的为
分子(Ⅱ)的三键相比,键长较长的为______ (用Ⅰ或Ⅱ表示)。
(2)CsAuCl3的结构不能表示为CsCl·AuCl2,实际上可看作一种阳离子和两种阴离子按照个数比为2∶1∶1形成的,这两种阴离子形状分别是直线型和平面正方形,在平面正方形离子中Au的化合价为______ 。基态Cs原子中电子占据的能量最高的轨道是______ ,能量最低的空轨道是______ 。
(3)如果m个原子有相互平行的p轨道,这些p轨道中共有n个电子(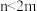 ),则可以形成大π键,表示为
),则可以形成大π键,表示为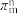 ,则SO2分子中的大π键可以表示为
,则SO2分子中的大π键可以表示为______ 。
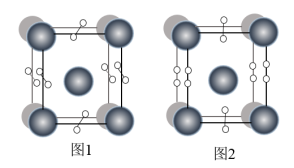
(4)如图表示的是某物质的两种结构的晶胞(大球表示的是K原子,小球表示O原子)图1中的O2单元空间取向有______ 种。若K之间底面上的最近距离为a pm,竖直方向上为c pm,图2表示的晶体密度为______  ,(NA表示阿伏加德罗常数)
,(NA表示阿伏加德罗常数)
 ),该配体以π电子参与配位,其中Ni2+的价电子排布式为
),该配体以π电子参与配位,其中Ni2+的价电子排布式为 (Ⅰ)和气态
(Ⅰ)和气态 分子(Ⅱ)的三键相比,键长较长的为
分子(Ⅱ)的三键相比,键长较长的为
(2)CsAuCl3的结构不能表示为CsCl·AuCl2,实际上可看作一种阳离子和两种阴离子按照个数比为2∶1∶1形成的,这两种阴离子形状分别是直线型和平面正方形,在平面正方形离子中Au的化合价为
(3)如果m个原子有相互平行的p轨道,这些p轨道中共有n个电子(
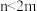 ),则可以形成大π键,表示为
),则可以形成大π键,表示为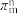 ,则SO2分子中的大π键可以表示为
,则SO2分子中的大π键可以表示为(4)如图表示的是某物质的两种结构的晶胞(大球表示的是K原子,小球表示O原子)图1中的O2单元空间取向有
 ,(NA表示阿伏加德罗常数)
,(NA表示阿伏加德罗常数)
20-21高三上·湖北武汉·阶段练习 查看更多[4]
八省八校(T8联考)2020-2021学年高三上学期第一次联考化学试题(华中师大一附中)(已下线)大题08 物质结构与性质(一)(选修)-【考前抓大题】备战2021年高考化学(全国通用)湖南省常德市汉寿县第一中学2022届高三下学期第三次模考化学试题山东省菏泽市单县第二中学2023届高三第一次模拟考试化学试题
更新时间:2021-01-03 09:52:09
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】含硼、氮、磷的化合物有许多重要用途,如:(CH3)3N、Cu3P、磷化硼等。回答下列问题:
(1)基态B原子电子占据最高能级的电子云轮廓图为_____ ;基态Cu+的核外电子排布式为_____ 。
(2)化合物(CH3)3N分子中N原子杂化方式为_____ ,该物质能溶于水的原因是_____ 。
(3)PH3分子的键角小于NH3分子的原因是_____ ;亚磷酸(H3PO3)是磷元素的一种含氧酸,与NaOH反应只生成NaH2PO3和Na2HPO3两种盐,则H3PO3分子的结构式为_____ 。
(4)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图1所示:
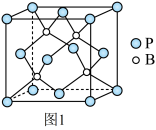
①在一个晶胞中磷原子的配位数为_____ 。
②已知磷化硼晶体的密度为ρg/cm3,阿伏加 德罗常数为NA,则B-P键长为_____ 。
(1)基态B原子电子占据最高能级的电子云轮廓图为
(2)化合物(CH3)3N分子中N原子杂化方式为
(3)PH3分子的键角小于NH3分子的原因是
(4)磷化硼是一种耐磨涂料,它可用作金属的表面保护层。磷化硼晶体晶胞如图1所示:

①在一个晶胞中磷原子的配位数为
②已知磷化硼晶体的密度为ρg/cm3,阿伏加 德罗常数为NA,则B-P键长为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知:V、W、R、T四种元素均位于元素周期表前四周期,它们的原子序数逐渐增大。其相关信息如表:
请回答下列问题:
(1)T元素的名称为______ ,在元素周期表中的位置是_____ 。
(2)基态W原子中能量最高的电子所占据能级的电子云在空间有_____ 个方向,原子轨道呈_____ 形。
(3)W的单质易溶于V、W形成的化合物中,其原因是_____ 。
(4)V、W、R三种元素最高价氧化物对应水化物的酸性从强到弱的顺序是______ (用化学式表示),原因是_____ 。
(5)写出W、T元素的单质加热时发生化合的化学方程式:______ 。
| V元素是形成有机物的必备元素 |
| W元素基态原子最外层p轨道电子数是最外层s轨道电子数的2倍,其单质常温下为固体 |
| R元素与W元素位于同一周期并相邻 |
| T元素原子中p轨道电子数与d轨道电子数之比为6:5;其盐溶液通常呈蓝色 |
(1)T元素的名称为
(2)基态W原子中能量最高的电子所占据能级的电子云在空间有
(3)W的单质易溶于V、W形成的化合物中,其原因是
(4)V、W、R三种元素最高价氧化物对应水化物的酸性从强到弱的顺序是
(5)写出W、T元素的单质加热时发生化合的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】近年来,我国以风电、光伏发电为代表的新能源发展成效显著,推动了绿色生态文明的建设。回答下列问题:
(1)光伏发电的传统材料是硅,基态硅原子核外电子有______ 种空间运动状态,与硅同主族的第四周期元素基态原子的价层电子排布式为______ 。
(2) 与N—甲基咪唑
与N—甲基咪唑 反应可以得到
反应可以得到 ,其结构如图1所示。
,其结构如图1所示。
①已知 —甲基咪唑分子具有类似苯环的结构,则该分子中存在的大
—甲基咪唑分子具有类似苯环的结构,则该分子中存在的大 键应表示为
键应表示为______ ,连甲基的 原子的价层孤电子对占据
原子的价层孤电子对占据______ 轨道。
②每个 含有个
含有个 键;除
键;除 键外,
键外, 中还存在的化学键有
中还存在的化学键有______ (填标号)。
A.极性键B.非极性键C.离子键D.范德华力E.配位键
(3)武汉大学闵杰课题组研究出一种小分子有机光伏材料,结构如图2所示。 由大到小的顺序为
由大到小的顺序为______ (用元素符号表示)。
② 是微电子工业中一种优良的等离子蚀刻气体,其分子空间构型与
是微电子工业中一种优良的等离子蚀刻气体,其分子空间构型与 相似,键角
相似,键角
______  (填“大于”“等于”或“小于”),原因是
(填“大于”“等于”或“小于”),原因是______ 。
(1)光伏发电的传统材料是硅,基态硅原子核外电子有
(2)
 与N—甲基咪唑
与N—甲基咪唑 反应可以得到
反应可以得到 ,其结构如图1所示。
,其结构如图1所示。
①已知
 —甲基咪唑分子具有类似苯环的结构,则该分子中存在的大
—甲基咪唑分子具有类似苯环的结构,则该分子中存在的大 键应表示为
键应表示为 原子的价层孤电子对占据
原子的价层孤电子对占据②每个
 含有个
含有个 键;除
键;除 键外,
键外, 中还存在的化学键有
中还存在的化学键有A.极性键B.非极性键C.离子键D.范德华力E.配位键
(3)武汉大学闵杰课题组研究出一种小分子有机光伏材料,结构如图2所示。
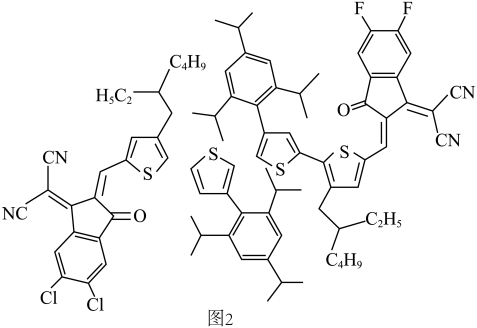
 由大到小的顺序为
由大到小的顺序为②
 是微电子工业中一种优良的等离子蚀刻气体,其分子空间构型与
是微电子工业中一种优良的等离子蚀刻气体,其分子空间构型与 相似,键角
相似,键角
 (填“大于”“等于”或“小于”),原因是
(填“大于”“等于”或“小于”),原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】因在航空、核能、电池等高技术领域的重要作用——锂被称为“21世纪的能源金属”。
(1)锂在元素周期表中的位置_______ 。锂的很多化学性质与镁相似,请依据元素周期律进行解释:_______ 。
(2)氢化锂(LiH)是离子化合物,写出其电子式_______ ,LiH中阴离子半径大于阳离子半径,其原因是_______ 。
工业上用 制取锂的化合物及金属锂。
制取锂的化合物及金属锂。
(3)碳原子核外电子有_______ 种不同能量的电子,其中有两个电子的能量最高且能量相等,这两个电子所处的轨道是_______ 。
(4)用 、氨水和液溴制备
、氨水和液溴制备 的流程如下:
的流程如下:

①合成时,除生成LiBr外,还产生了两种参与大气循环的气体,补全产物并配平该反应的化学方程式:_______ 。
_______ +_______
+_______ _______
_______
 _______
_______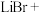 _______
_______
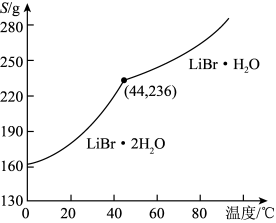
②溴化锂的溶解度随温度变化曲线如图所示,请补全从溶液中得到 晶体的实验步骤:
晶体的实验步骤:_______ 、过滤、用乙醇洗涤,干燥。
(1)锂在元素周期表中的位置
(2)氢化锂(LiH)是离子化合物,写出其电子式
工业上用
 制取锂的化合物及金属锂。
制取锂的化合物及金属锂。(3)碳原子核外电子有
(4)用
 、氨水和液溴制备
、氨水和液溴制备 的流程如下:
的流程如下:
①合成时,除生成LiBr外,还产生了两种参与大气循环的气体,补全产物并配平该反应的化学方程式:
_______
 +_______
+_______ _______
_______
 _______
_______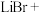 _______
_______②溴化锂的溶解度随温度变化曲线如图所示,请补全从溶液中得到
 晶体的实验步骤:
晶体的实验步骤:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表给出了五种元素的相关信息,其中X、Y、Z、W为短周期元素。
根据上述信息填空:
(1)Y元素的原子含有___________ 个能层,其中第二能层中的能级包括___________ ;画出W元素原子的结构示意图:___________ ;M元素是___________ (填元素符号)。
(2)Z与X形成的某种化合物能和Z与Y形成的另一种无色化合物(这两种化合物分子中Z与另一元素原子的个数比均为1:2)一起用作火箭推进剂,写出二者发生反应生成无毒物质的化学方程式:___________ 。
| 元素 | 相关信息 |
| X | 在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为备受青睐的清洁燃料 |
| Y | 工业上通过分离液态空气获得它的一种单质,含它的另一种单质的浓度相对较高的平流层是保护地球地表环境的重要屏障 |
| W | 植物生长所需的主要元素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂 |
| Z | 室温下其单质为粉末状固体,加热易熔化。该单质在氧气中燃烧发出明亮的蓝紫色火焰 |
| M | 它是人体不可缺少的微量元素,含该元素的合金是工业生产中不可缺少的金属材料,常用于建造桥梁楼房等 |
(1)Y元素的原子含有
(2)Z与X形成的某种化合物能和Z与Y形成的另一种无色化合物(这两种化合物分子中Z与另一元素原子的个数比均为1:2)一起用作火箭推进剂,写出二者发生反应生成无毒物质的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】a、b、c、d为四种由短周期元素构成的中性微粒,它们都有14个电子,且除a外都是共价型分子。回答下列问题:
(1)a是常见单原子微粒,a单质可用作半导体材料,a原子核外电子排布式为______ 。M层上的能级能量大小关系为_________ ,3p能级上的电子应满足_______ 。
(2)b是两原子化合物,常温下为无色无味气体。b的化学式为________ 。人一旦吸入b气体后,就易引起中毒,是因为________ 而中毒。
(3)c是两原子单质,写出其电子式___________ 。c分子中所含共价键的类型为_______ (填“极性键”或“非极性键”)。c单质常温下性质稳定,不易起反应,原因是____ 。
(4)d是四原子有机化合物,其结构式为______________ ;d分子内所含共价键有________ 个σ键,________ 个π键;σ键与π键的强度大小关系为σ___ π(填“>”、“<”或“=”),原因是:_______ 。
(1)a是常见单原子微粒,a单质可用作半导体材料,a原子核外电子排布式为
(2)b是两原子化合物,常温下为无色无味气体。b的化学式为
(3)c是两原子单质,写出其电子式
(4)d是四原子有机化合物,其结构式为
您最近一年使用:0次
【推荐1】新型储氢材料是氢能的重要研究方向。
(1)化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3通过如下反应制得:3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3。A在一定条件下通过多步去氢可最终转化为氮化硼(BN)。
①基态O原子的电子占据了_______ 个能层,最高能级有______ 种运动状态不同的电子。
②CH4、H2O、CO2分子键角从大到小的顺序是______ 。写出H3BNH3固体结构式,并标注出其中的配位键______ ,写出与H3BNH3互为等电子体的分子、离子的化学式______ 、______ 。(各举一例),。
(2)掺杂T基催化剂的NaAlH4是其中一种具有较好吸、放氢性能的可逆储氢材料。NaAlH4由Na+和AlH 构成,Al原子的杂化轨道类型是
构成,Al原子的杂化轨道类型是_______ 。Na、Al、H元素的电负性由大到小的顺序为______ 。
(3)Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在中国已实现了产业化。该合金的晶胞结构如图所示。

①该晶体的化学式为______ 。
②已知该晶胞的摩尔质量为Mg/mol,密度为dg/cm3。设NA为阿伏加 德罗常数的值,则该晶胞的体积是______ cm3(用含M、d、NA的代数式表示)。
③已知晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子比较稳定,晶胞参数分别为apm、apm、cpm。标准状况下氢气的密度为Mg/cm3;若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为________ 。(用相关字母表示已知储氢能力=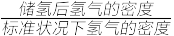 )。
)。
(1)化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3通过如下反应制得:3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3。A在一定条件下通过多步去氢可最终转化为氮化硼(BN)。
①基态O原子的电子占据了
②CH4、H2O、CO2分子键角从大到小的顺序是
(2)掺杂T基催化剂的NaAlH4是其中一种具有较好吸、放氢性能的可逆储氢材料。NaAlH4由Na+和AlH
 构成,Al原子的杂化轨道类型是
构成,Al原子的杂化轨道类型是(3)Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在中国已实现了产业化。该合金的晶胞结构如图所示。

①该晶体的化学式为
②已知该晶胞的摩尔质量为Mg/mol,密度为dg/cm3。设NA为阿伏加 德罗常数的值,则该晶胞的体积是
③已知晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子比较稳定,晶胞参数分别为apm、apm、cpm。标准状况下氢气的密度为Mg/cm3;若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为
 )。
)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
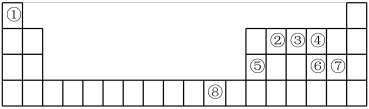
(1)元素⑧的基态原子价电子排布式为_______ 。
(2)元素②③④的第一电离能由大到小的顺序是_______ (填元素符号)。
(3)元素③④⑤形成的简单离子半径由大到小的顺序为_______ (用离子符号表示)。
(4)元素④⑥的简单气态氢化物更稳定的是_______ ,键角更大的是_______ (填化学式)。
(5)元素③的最高价含氧酸根的中心原子杂化方式为_______ ,其空间结构为_______ 。
(6)由元素⑦⑧组成的化合物溶于水后溶液呈蓝色,滴加稀盐酸变成黄绿色,从平衡移动角度解释上述颜色变化过程:_______ (用离子方程式表示)。

(1)元素⑧的基态原子价电子排布式为
(2)元素②③④的第一电离能由大到小的顺序是
(3)元素③④⑤形成的简单离子半径由大到小的顺序为
(4)元素④⑥的简单气态氢化物更稳定的是
(5)元素③的最高价含氧酸根的中心原子杂化方式为
(6)由元素⑦⑧组成的化合物溶于水后溶液呈蓝色,滴加稀盐酸变成黄绿色,从平衡移动角度解释上述颜色变化过程:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)铁的一种配合物的化学式为[Fe(Htrz)3](ClO4)2,其中Htrz为1,2,4-三氮唑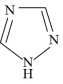 ,配合物中阴离子空间构型为
,配合物中阴离子空间构型为_______ ,阴离子的中心原子的杂化方式是_______ 。
(2)下图表示一些晶体中的某些结构,请回答下列问题:
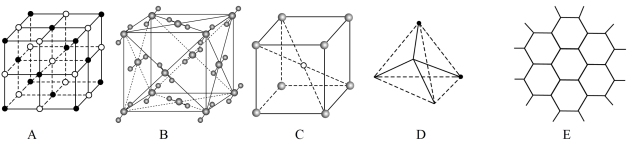
①代表金刚石的是_______ (填编号字母,下同),其中每个碳原子与_______ 个碳原子最近且距离相等,金刚石属于_______ 晶体。
②代表石墨的是_______ ,每个正六边形占有的碳原子数平均为_______ 个。
(3)苏丹红颜色鲜艳、价格低廉,常被一些企业非法作为食品和化妆品等的染色剂,严重危害人们健康。苏丹红常见有I、II、III、IV4种类型,苏丹红I的分子结构如图1所示。
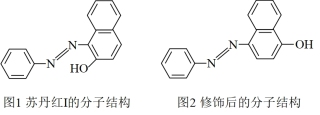
苏丹红I在水中溶解度很小,微溶于乙醇,有人把羟基取代在对位形成图2所示的结构,则其在水中的溶解度会_______ (填“增大”或“减小”),原因是_______ 。
(1)铁的一种配合物的化学式为[Fe(Htrz)3](ClO4)2,其中Htrz为1,2,4-三氮唑
 ,配合物中阴离子空间构型为
,配合物中阴离子空间构型为(2)下图表示一些晶体中的某些结构,请回答下列问题:

①代表金刚石的是
②代表石墨的是
(3)苏丹红颜色鲜艳、价格低廉,常被一些企业非法作为食品和化妆品等的染色剂,严重危害人们健康。苏丹红常见有I、II、III、IV4种类型,苏丹红I的分子结构如图1所示。

苏丹红I在水中溶解度很小,微溶于乙醇,有人把羟基取代在对位形成图2所示的结构,则其在水中的溶解度会
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】(1)基态N原子价层电子的排布图(轨道表达式)为___ ;基态N原子占据最高能级的电子云轮廓图为___ 形。
(2)CO(NH2)2分子中含有σ键的个数为___ ;CaCN2中阴离子为CN ,与CN
,与CN 离子互为等电子体的分子的化学式为
离子互为等电子体的分子的化学式为___ ;可推知CN 的空间构型为
的空间构型为___ 。
(3)三聚氰胺(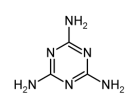 )在动物可转化为三聚氰酸(
)在动物可转化为三聚氰酸(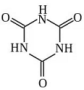 ),三聚氰酸分子中N原子采取
),三聚氰酸分子中N原子采取___ 杂化;三聚氰胺与三聚氰酸的分子相互之间通过___ 结合;在肾脏内易形成结石。
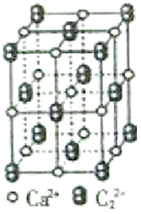
(4)如图是电石的晶胞示意图,则一个晶胞中含有___ 个Ca2+离子;研究表明,C 的存在使晶胞呈长方体,该晶胞中一个Ca2+周围距离相等且最近的C
的存在使晶胞呈长方体,该晶胞中一个Ca2+周围距离相等且最近的C 有
有___ 个。
(2)CO(NH2)2分子中含有σ键的个数为
 ,与CN
,与CN 离子互为等电子体的分子的化学式为
离子互为等电子体的分子的化学式为 的空间构型为
的空间构型为(3)三聚氰胺(
 )在动物可转化为三聚氰酸(
)在动物可转化为三聚氰酸( ),三聚氰酸分子中N原子采取
),三聚氰酸分子中N原子采取(4)如图是电石的晶胞示意图,则一个晶胞中含有
 的存在使晶胞呈长方体,该晶胞中一个Ca2+周围距离相等且最近的C
的存在使晶胞呈长方体,该晶胞中一个Ca2+周围距离相等且最近的C 有
有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】钠的化合物用途广泛,回答下列问题:
(1)多硫化钠(Na2Sx)用作聚合的终止剂。钠原子价层电子的轨道表达式(电子排布图)为___________ ,基态S原子电子占据最高能级的电子云轮廓图为___________ ,其中Na2S4中存在的化学键有:___________ 。
A.离子键 B.极性共价键 C.π键 D.非极性共价键
(2)r(S2-)>r(Na+)的原因是___________ 。
(3)Na2SO3常用作工业的脱氧剂和漂白剂,其阴离子的中心原子的杂化形式是___________ ,空间构型是______________________ 。
(4)下表列出了钠的卤化物的熔点:
①NaF的熔点比NaI的熔点高的原因是_________________________________ ;
②NaCl晶格能是786 kJ/mol,则NaF的晶格能可能是___________ 。
A. 704 kJ/mol B. 747kJ/mol C 928 kJ/mol
(5)NaH具有NaCl型的立方晶体结构,已知NaH晶体的晶胞参数a=488pm,Na+半径为102pm,则H-的半径为___________ pm;NaH的理论密度是___________ g·cm-3(保留三位有效数字)。[H—1、Na—23]
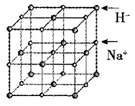
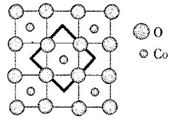
(6)首例被发现的带结晶水的超导材料晶体化学式为Na0.35CoOx·1.3H2O,具有……-CoO2-H2O-Na-H2O-CoO2-H2O-Na-H2O-……层状结构,已知CoOx层的构型部分如图,其中粗线画出的是其二维晶胞,则x=___________ 。
(1)多硫化钠(Na2Sx)用作聚合的终止剂。钠原子价层电子的轨道表达式(电子排布图)为
A.离子键 B.极性共价键 C.π键 D.非极性共价键
(2)r(S2-)>r(Na+)的原因是
(3)Na2SO3常用作工业的脱氧剂和漂白剂,其阴离子的中心原子的杂化形式是
(4)下表列出了钠的卤化物的熔点:
| 化学式 | NaF | NaCl | NaBr | NaI |
| 熔点/℃ | 995 | 801 | 775 | 651 |
①NaF的熔点比NaI的熔点高的原因是
②NaCl晶格能是786 kJ/mol,则NaF的晶格能可能是
A. 704 kJ/mol B. 747kJ/mol C 928 kJ/mol
(5)NaH具有NaCl型的立方晶体结构,已知NaH晶体的晶胞参数a=488pm,Na+半径为102pm,则H-的半径为

(6)首例被发现的带结晶水的超导材料晶体化学式为Na0.35CoOx·1.3H2O,具有……-CoO2-H2O-Na-H2O-CoO2-H2O-Na-H2O-……层状结构,已知CoOx层的构型部分如图,其中粗线画出的是其二维晶胞,则x=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】铁是一种重要的材料金属,与氨形成的化合物可用于制备催化剂、磁流体、吸波剂等,与镧、锑形成的合金具有热电效应。回答下列问题:
(1)Sb是与N同主族的第五周期元素,基态Sb原子的价电子排布图为_______ ;基态 核外占据最高能级电子的电子云有
核外占据最高能级电子的电子云有_______ 个伸展方向。
(2)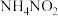 能为制备氮化铁提供氨源。
能为制备氮化铁提供氨源。
①1 molNH4NO2中含有配位键的数目为_______ 。
② 的立体构型为
的立体构型为_______ ,其中氮原子的杂化方式为_______ 。
③氮及其同周期相邻元素原子的第一电离能由大到小的顺序为_______ (用元素符号表示),其原因为_______ 。
④分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数,则
键的电子数,则 中的大
中的大 键可表示为
键可表示为_______ 。
(3)La、Sb、Fe形成合金的立方晶胞中,Fe原子填入Sb原子形成的正八面体空隙;La和Fe的位置如图1所示;沿x、y、z轴的投影图中Sb的位置相同,如图2所示。
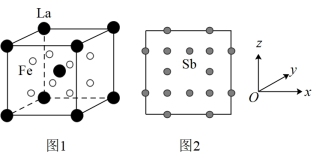
①La原子周围距离最近的Sb原子数目为_______ 。
②若晶胞参数为a pm,阿伏加德罗常数的值为NA,则晶体密度为_______  (用含a、NA的代数式表示)。
(用含a、NA的代数式表示)。
(1)Sb是与N同主族的第五周期元素,基态Sb原子的价电子排布图为
 核外占据最高能级电子的电子云有
核外占据最高能级电子的电子云有(2)
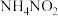 能为制备氮化铁提供氨源。
能为制备氮化铁提供氨源。①1 molNH4NO2中含有配位键的数目为
②
 的立体构型为
的立体构型为③氮及其同周期相邻元素原子的第一电离能由大到小的顺序为
④分子中的大
 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数,则
键的电子数,则 中的大
中的大 键可表示为
键可表示为(3)La、Sb、Fe形成合金的立方晶胞中,Fe原子填入Sb原子形成的正八面体空隙;La和Fe的位置如图1所示;沿x、y、z轴的投影图中Sb的位置相同,如图2所示。

①La原子周围距离最近的Sb原子数目为
②若晶胞参数为a pm,阿伏加德罗常数的值为NA,则晶体密度为
 (用含a、NA的代数式表示)。
(用含a、NA的代数式表示)。
您最近一年使用:0次



