工业上常用水钴矿(主要成分为Co2O3,还含少量Fe2O3、Al2O3、MgO、CaO等杂质)制备钴的氧化物,其制备工艺流程如下:
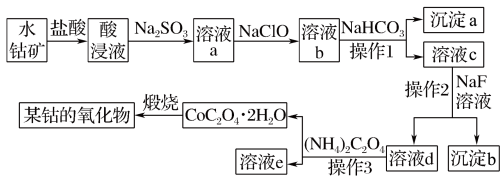
已知:CoC2O4∙2H2O微溶于水,它的溶解度随温度升高而逐渐增大。回答下列问题:
(1)进行“酸浸”时,能提高“酸浸”速率的方法有_______ (任写2种)。
(2)“酸浸”后加入Na2SO3生成Co2+的离子方程式为_______ 。
(3)沉淀a所含有的主要物质是_______ ;溶液d中的金属离子只有Co2+和Na+两种,则溶液c中加入NaF溶液的作用是_______ 。
(4)“沉钴”过程中,加入(NH4)2C2O4使得n(C2O )∶n(Co2+)初始比值为1.15,沉淀反应时间为10 min,沉淀反应的温度与钴的沉淀率关系如图所示:
)∶n(Co2+)初始比值为1.15,沉淀反应时间为10 min,沉淀反应的温度与钴的沉淀率关系如图所示:

该过程需控制温度在46℃~50℃的原因是_______ 。
(5)在空气中煅烧CoC2O4生成钴的某种氧化物和CO2,测得充分煅烧后固体质量为12.05 g,CO2的体积为6.72 L(标准状况),则此反应的化学方程式为_______ 。

已知:CoC2O4∙2H2O微溶于水,它的溶解度随温度升高而逐渐增大。回答下列问题:
(1)进行“酸浸”时,能提高“酸浸”速率的方法有
(2)“酸浸”后加入Na2SO3生成Co2+的离子方程式为
(3)沉淀a所含有的主要物质是
(4)“沉钴”过程中,加入(NH4)2C2O4使得n(C2O
 )∶n(Co2+)初始比值为1.15,沉淀反应时间为10 min,沉淀反应的温度与钴的沉淀率关系如图所示:
)∶n(Co2+)初始比值为1.15,沉淀反应时间为10 min,沉淀反应的温度与钴的沉淀率关系如图所示:
该过程需控制温度在46℃~50℃的原因是
(5)在空气中煅烧CoC2O4生成钴的某种氧化物和CO2,测得充分煅烧后固体质量为12.05 g,CO2的体积为6.72 L(标准状况),则此反应的化学方程式为
2021·福建漳州·一模 查看更多[2]
更新时间:2021-01-07 14:24:09
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】铁红(Fe2O3)是一种常见颜料,用废铁屑制取铁红的工艺如图:
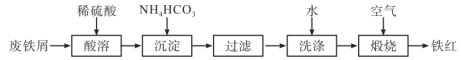
(1)为了加快“酸溶”时的反应速率,可以采取的措施有:___________ (任写两条)。
(2)FeSO4溶液放置时间久了会变黄,可用___________ (填写试剂的化学式)加以检验,变质的原因是(用离子方程式表示)___________ ,可以加入___________ 以避免该现象的发生。
(3)“沉淀”反应中除生成FeCO3外,还生成一种气体,写出该反应的离子方程式___________ 。
(4)”洗涤”步骤操作的方法是___________ 。
(5)“煅烧”时FeCO3与O2反应的化学方程式为___________ 。

(1)为了加快“酸溶”时的反应速率,可以采取的措施有:
(2)FeSO4溶液放置时间久了会变黄,可用
(3)“沉淀”反应中除生成FeCO3外,还生成一种气体,写出该反应的离子方程式
(4)”洗涤”步骤操作的方法是
(5)“煅烧”时FeCO3与O2反应的化学方程式为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】汽车尾气中含有CO、NOx等有害气体。
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:___________ 。
(2)汽车尾气中NO生成过程的能量变化示意图如下:
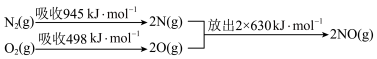
该条件下,N2和O2完全反应生成2molNO时需要_______ (吸收或释放)________ kJ的能量。
(3)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:

①NiO电极上发生的是___________ 反应(填“氧化”或“还原”)。
②外电路中,电子的流动方向是从___________ 电极流出(填NiO或Pt);Pt电极上的电极反应式为___________ 。
(4)一种新型催化剂能使NO和CO发生反应:2NO+2CO⇌2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
①请将表中数据补充完整:A___________ ;B___________ 。
②能验证温度对化学反应速率影响规律的实验是___________ (填实验编号)。
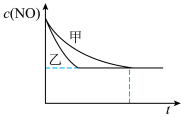
③实验Ⅰ和实验Ⅱ中,c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的曲线是___________ (填“甲”或“乙”)。
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:
(2)汽车尾气中NO生成过程的能量变化示意图如下:

该条件下,N2和O2完全反应生成2molNO时需要
(3)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:

①NiO电极上发生的是
②外电路中,电子的流动方向是从
(4)一种新型催化剂能使NO和CO发生反应:2NO+2CO⇌2CO2+N2。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下表中。
| 实验 编号 | t(℃) | NO初始浓度 (mol/L) | CO初始浓度 (mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | 1.20×10-3 | B | 124 |
| Ⅲ | 350 | A | 5.80×10-3 | 82 |
②能验证温度对化学反应速率影响规律的实验是
③实验Ⅰ和实验Ⅱ中,c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的曲线是

您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】工业上以铬铁矿(主要成分为FeO和Cr2O3,含有Al2O3、SiO2等杂质)为主要原料生产化工原料红矾钠(主要成分为:Na2Cr2O7·2H2O),其主要工艺流程如下:
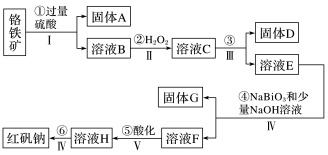
查阅相关资料得知:
i.常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下能将Cr3+转化为CrO42—,自身被还原为Bi(OH)3固体。
ii.
回答下列问题:
(1)将铬铁矿矿石粉碎的目的是___________ 。
(2)操作I、III、IV用到的主要玻璃仪器有玻璃棒和___________ (填仪器名称)。
(3)写出④反应的化学方程式________________ 。
(4)⑤中酸化是使CrO42—转化为Cr2O72—。写出该反应的离子方程式______ 。
(5)将溶液H经下列操作:蒸发浓缩,__________ ,过滤,洗涤,干燥即得红矾钠。
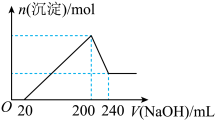
(6)取一定质量的固体D溶解于200mL的稀硫酸中,向所得溶液中加入5.0mol/L的NaOH溶液,生成沉淀的物质的量(n)与加入NaOH溶液的体积(V)关系如图所示,则稀硫酸的浓度为_________ ,固体D中含Fe化合物的物质的量为___________ 。

查阅相关资料得知:
i.常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下能将Cr3+转化为CrO42—,自身被还原为Bi(OH)3固体。
ii.
| 物质 | Fe(OH)3 | Al(OH)3 | Cr(OH)3 | Fe(OH)2 | Bi(OH)3 |
| 开始沉淀的PH | 2.7 | 3.4 | 4.6 | 7.5 | 0.7 |
| 完全沉淀的PH | 3.7 | 4.4 | 5.9 | 9.7 | 4.5 |
回答下列问题:
(1)将铬铁矿矿石粉碎的目的是
(2)操作I、III、IV用到的主要玻璃仪器有玻璃棒和
(3)写出④反应的化学方程式
(4)⑤中酸化是使CrO42—转化为Cr2O72—。写出该反应的离子方程式
(5)将溶液H经下列操作:蒸发浓缩,
(6)取一定质量的固体D溶解于200mL的稀硫酸中,向所得溶液中加入5.0mol/L的NaOH溶液,生成沉淀的物质的量(n)与加入NaOH溶液的体积(V)关系如图所示,则稀硫酸的浓度为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】以银锰精矿(主要含 、
、 、
、 )和氧化锰矿(主要含
)和氧化锰矿(主要含 )为原料联合提取银和锰的一种流程示意图如下。
)为原料联合提取银和锰的一种流程示意图如下。
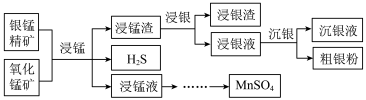
已知:酸性条件下, 的氧化性强于
的氧化性强于 。
。
(1)“浸锰”过程是在 溶液中使矿石中的锰元素浸出,同时去除
溶液中使矿石中的锰元素浸出,同时去除 ,有利于后续银的浸出:矿石中的银以
,有利于后续银的浸出:矿石中的银以 的形式残留于浸锰渣中。
的形式残留于浸锰渣中。
①“浸锰”过程中,发生反应 ,则可推断:
,则可推断: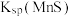
___________ (填“>”或“<”) 。
。
②在 溶液中,银锰精矿中的
溶液中,银锰精矿中的 和氧化锰矿中的
和氧化锰矿中的 发生反应,则浸锰液中主要的金属阳离子有
发生反应,则浸锰液中主要的金属阳离子有___________ 。
(2)“沉银”过程中需要过量的铁粉作为还原剂。
①该步反应的离子方程式有___________ 。
②一定温度下, 的沉淀率随反应时间的变化如图所示。解释t分钟后
的沉淀率随反应时间的变化如图所示。解释t分钟后 的沉淀率逐渐减小的原因:
的沉淀率逐渐减小的原因:___________ 。

(3)结合“浸锰”过程,从两种矿石中各物质利用的角度,分析联合提取银和锰的优势:___________ 。
 、
、 、
、 )和氧化锰矿(主要含
)和氧化锰矿(主要含 )为原料联合提取银和锰的一种流程示意图如下。
)为原料联合提取银和锰的一种流程示意图如下。
已知:酸性条件下,
 的氧化性强于
的氧化性强于 。
。(1)“浸锰”过程是在
 溶液中使矿石中的锰元素浸出,同时去除
溶液中使矿石中的锰元素浸出,同时去除 ,有利于后续银的浸出:矿石中的银以
,有利于后续银的浸出:矿石中的银以 的形式残留于浸锰渣中。
的形式残留于浸锰渣中。①“浸锰”过程中,发生反应
 ,则可推断:
,则可推断: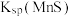
 。
。②在
 溶液中,银锰精矿中的
溶液中,银锰精矿中的 和氧化锰矿中的
和氧化锰矿中的 发生反应,则浸锰液中主要的金属阳离子有
发生反应,则浸锰液中主要的金属阳离子有(2)“沉银”过程中需要过量的铁粉作为还原剂。
①该步反应的离子方程式有
②一定温度下,
 的沉淀率随反应时间的变化如图所示。解释t分钟后
的沉淀率随反应时间的变化如图所示。解释t分钟后 的沉淀率逐渐减小的原因:
的沉淀率逐渐减小的原因:
(3)结合“浸锰”过程,从两种矿石中各物质利用的角度,分析联合提取银和锰的优势:
您最近半年使用:0次
【推荐2】蛇纹石矿由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁实验步骤如下:
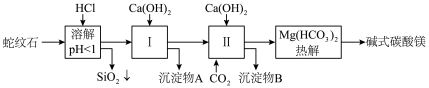
已知:
(1)蛇纹石加盐酸溶解后,溶液里除了Mg2+外,还含有的阳离子有________________ 。
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见上表),Ca(OH)2不能过量,若Ca(OH)2过量可能会导致________ 溶解、________ 沉淀。
(3)物质循环使用,能节约资源,上述实验中,可以循环使用的物质是______________ 。
(4)高温煅烧碱式碳酸镁aMgCO3·bMg(OH)2·cH2O得到MgO。取碱式碳酸镁4.66 g,高温煅烧至恒重,得到固体2.00 g和标准状况下CO2 0.896 L,通过计算确定碱式碳酸镁的化学式为____________________ 。(写出计算过程,否则不得分)

已知:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见上表),Ca(OH)2不能过量,若Ca(OH)2过量可能会导致
(3)物质循环使用,能节约资源,上述实验中,可以循环使用的物质是
(4)高温煅烧碱式碳酸镁aMgCO3·bMg(OH)2·cH2O得到MgO。取碱式碳酸镁4.66 g,高温煅烧至恒重,得到固体2.00 g和标准状况下CO2 0.896 L,通过计算确定碱式碳酸镁的化学式为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如图:
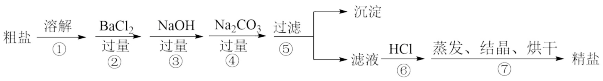
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是____ 。
(2)第②步操作加入过量的BaCl2目的是除去粗盐中的____ ;写出这个反应的化学方程____ 。
(3)第⑤步“过滤”操作中得到沉淀的成分有泥沙____ (多选)。
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是____ 。
(5)在利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是除去滤液中的NaOH和____ 。
(6)食盐水也可以通过电解得到更多种类的化工原料,写出电解饱和食盐水的化学方程式____ ;电解过程中,阳极有____ 色氯气产生,可用湿润的____ 试纸检验该气体。

(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是
(2)第②步操作加入过量的BaCl2目的是除去粗盐中的
(3)第⑤步“过滤”操作中得到沉淀的成分有泥沙
| A.BaSO4 | B.CaCO3 | C.BaCO3 | D.Mg(OH)2 |
(5)在利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是除去滤液中的NaOH和
(6)食盐水也可以通过电解得到更多种类的化工原料,写出电解饱和食盐水的化学方程式
您最近半年使用:0次



