过氧化氢的水溶液俗称双氧水,它的用途很广泛,常用于消毒、杀菌、漂白等。回答下列问题:
(1)过氧化氢的性质
①酸性条件下H2O2可将Fe2+转化成Fe3+,说明H2O2具有__ 性。
②常温下,H2O2显弱酸性(Ka1=2.40×10-12、Ka2=1.05×10-25),不能使甲基橙指示剂褪色,则向4.0mol•L-1的H2O2溶液中滴加甲基橙,溶液显__ 色。(甲基橙在pH小于3.1时显红色,3.1~4.4时显橙色,大于4.4时显黄色)
(2)过氧化氢含量的测定实验
某兴趣小组同学用0.1mol•L-1的酸性高锰酸钾标准溶液滴定试样中的过氧化氢,反应原理为2MnO +5H2O2+6H+=2Mn2++8H2O+5O2↑。
+5H2O2+6H+=2Mn2++8H2O+5O2↑。
①滴定达到终点的现象是__ 。
②用移液管移取25.00mL试样置于锥形瓶中,重复滴定四次,每次消耗酸性高锰酸钾标准溶液的体积如下表:
试样中过氧化氢的浓度为__ mol•L-1。
(3)甲酸钙[Ca(HCOO)2]广泛用于食品工业生产上。实验室制取甲酸钙的方法之一是将氢氧化钙和甲醛(HCHO)溶液依次加入质量分数为30%~70%的过氧化氢溶液中。该反应的化学方程式为__ 。
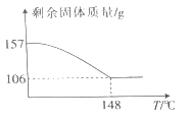
(4)过氧化氢与碳酸钠的加合物Na2CO3•xH2O2比较稳定,方便储存,可用于消毒、漂白。现称取157gNa2CO3•xH2O2晶体加热,实验结果如图所示,则该晶体的组成为__ (x精确到0.1)
(1)过氧化氢的性质
①酸性条件下H2O2可将Fe2+转化成Fe3+,说明H2O2具有
②常温下,H2O2显弱酸性(Ka1=2.40×10-12、Ka2=1.05×10-25),不能使甲基橙指示剂褪色,则向4.0mol•L-1的H2O2溶液中滴加甲基橙,溶液显
(2)过氧化氢含量的测定实验
某兴趣小组同学用0.1mol•L-1的酸性高锰酸钾标准溶液滴定试样中的过氧化氢,反应原理为2MnO
 +5H2O2+6H+=2Mn2++8H2O+5O2↑。
+5H2O2+6H+=2Mn2++8H2O+5O2↑。①滴定达到终点的现象是
②用移液管移取25.00mL试样置于锥形瓶中,重复滴定四次,每次消耗酸性高锰酸钾标准溶液的体积如下表:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| V(酸性KMnO4标准溶液)/mL | 17.10 | 18.10 | 18.00 | 17.90 |
试样中过氧化氢的浓度为
(3)甲酸钙[Ca(HCOO)2]广泛用于食品工业生产上。实验室制取甲酸钙的方法之一是将氢氧化钙和甲醛(HCHO)溶液依次加入质量分数为30%~70%的过氧化氢溶液中。该反应的化学方程式为
(4)过氧化氢与碳酸钠的加合物Na2CO3•xH2O2比较稳定,方便储存,可用于消毒、漂白。现称取157gNa2CO3•xH2O2晶体加热,实验结果如图所示,则该晶体的组成为

更新时间:2021-01-11 14:00:43
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】完成下列问题
Ⅰ.现有下列十种物质:①蔗糖②熔融NaCl③盐酸④铜丝⑤NaOH固体⑥氧气⑦ 固体⑧乙醇⑨
固体⑧乙醇⑨ 溶液⑩液态
溶液⑩液态
(1)上述状态下物质中可导电的是______ (填序号,下同);
(2)上述状态下物质中不能导电,但属于电解质的是______ ;
(3)上述物质中属于非电解质的是______ ;
(4)上述物质中既不属于电解质也不属于非电解质的是______ ;
Ⅱ.写出下列除杂的离子方程式,括号内的物质为杂质。
(5) 溶液(
溶液( ):
):__________________
(6) 溶液(
溶液( ):
):__________________ ;
(7)______ ____ ______
______ ______
______ ______
______ ______
______ ______
______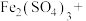 ______
______
Ⅰ.现有下列十种物质:①蔗糖②熔融NaCl③盐酸④铜丝⑤NaOH固体⑥氧气⑦
 固体⑧乙醇⑨
固体⑧乙醇⑨ 溶液⑩液态
溶液⑩液态
(1)上述状态下物质中可导电的是
(2)上述状态下物质中不能导电,但属于电解质的是
(3)上述物质中属于非电解质的是
(4)上述物质中既不属于电解质也不属于非电解质的是
Ⅱ.写出下列除杂的离子方程式,括号内的物质为杂质。
(5)
 溶液(
溶液( ):
):(6)
 溶液(
溶液( ):
):(7)
 ______
______ ______
______ ______
______ ______
______ ______
______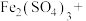 ______
______
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列各题
(1)现有下列物质:①冰水共存物 ②爆鸣气 ③铝热剂 ④普通玻璃 ⑤水玻璃⑥有机玻璃 ⑦漂白粉 ⑧TNT ⑨ ⑩含氧40%的氧化镁⑪花生油 ⑫福尔马林 ⑬密封保存的
⑩含氧40%的氧化镁⑪花生油 ⑫福尔马林 ⑬密封保存的 气体 ⑭
气体 ⑭ ⑮液氯⑯王水 ⑰
⑮液氯⑯王水 ⑰ ⑱分子式为
⑱分子式为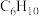 的烃 ⑲分子式为
的烃 ⑲分子式为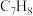 的芳香烃。其中一定为纯净物的是
的芳香烃。其中一定为纯净物的是___________ (填序号)。
(2)缺项配平:将 固体(黄色,微溶)加入
固体(黄色,微溶)加入 和
和 的混合溶液里,加热,溶液显紫色(
的混合溶液里,加热,溶液显紫色( 无色)。配平该反应的离子方程式:
无色)。配平该反应的离子方程式:___________ 。




 ______=
______=
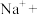


 ______+
______+ ________
________
(3)已知在酸性介质中 能将
能将 价铬还原成
价铬还原成 价铬。写出
价铬。写出 与
与 溶液在酸性条件下反应的离子方程式:
溶液在酸性条件下反应的离子方程式:___________ 。
(4)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。 的一种制备方法如下图所示:
的一种制备方法如下图所示:
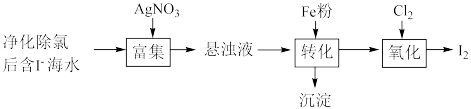
加入Fe粉进行转化反应的离子方程式为___________ 。
(1)现有下列物质:①冰水共存物 ②爆鸣气 ③铝热剂 ④普通玻璃 ⑤水玻璃⑥有机玻璃 ⑦漂白粉 ⑧TNT ⑨
 ⑩含氧40%的氧化镁⑪花生油 ⑫福尔马林 ⑬密封保存的
⑩含氧40%的氧化镁⑪花生油 ⑫福尔马林 ⑬密封保存的 气体 ⑭
气体 ⑭ ⑮液氯⑯王水 ⑰
⑮液氯⑯王水 ⑰ ⑱分子式为
⑱分子式为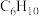 的烃 ⑲分子式为
的烃 ⑲分子式为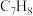 的芳香烃。其中一定为纯净物的是
的芳香烃。其中一定为纯净物的是(2)缺项配平:将
 固体(黄色,微溶)加入
固体(黄色,微溶)加入 和
和 的混合溶液里,加热,溶液显紫色(
的混合溶液里,加热,溶液显紫色( 无色)。配平该反应的离子方程式:
无色)。配平该反应的离子方程式:



 ______=
______=
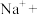


 ______+
______+ ________
________(3)已知在酸性介质中
 能将
能将 价铬还原成
价铬还原成 价铬。写出
价铬。写出 与
与 溶液在酸性条件下反应的离子方程式:
溶液在酸性条件下反应的离子方程式:(4)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。
 的一种制备方法如下图所示:
的一种制备方法如下图所示: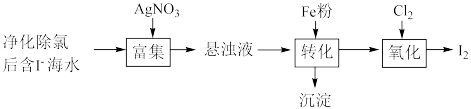
加入Fe粉进行转化反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】饮用水的质量关乎人类健康。回答下列问题:
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了HClO,写出HClO的电子式________ 。
(2)常温下,将氯气通入稀NaOH溶液中得到漂白液(主要成分为NaClO),该反应的离子方程式为________ 。
(3)ClO2是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备ClO2的一种方法为:在平底烧瓶中加入KClO3固体、足量草酸(H2C2O4)、稀硫酸,60℃~80℃水浴加热。该反应的化学方程式为________ 。
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了HClO,写出HClO的电子式
(2)常温下,将氯气通入稀NaOH溶液中得到漂白液(主要成分为NaClO),该反应的离子方程式为
(3)ClO2是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备ClO2的一种方法为:在平底烧瓶中加入KClO3固体、足量草酸(H2C2O4)、稀硫酸,60℃~80℃水浴加热。该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.甲酸(HCOOH)是一种弱酸,在水溶液中电离成氢离子和甲酸根离子( )。
)。
(1)请写出甲酸的电离方程式_______ 。
(2)某甲酸溶液中,HCOOH的初始浓度是 ,当其电离达到平衡时,溶液中的
,当其电离达到平衡时,溶液中的 浓度c的取值范围是_______。
浓度c的取值范围是_______。
Ⅱ.完成下列问题
(3)某种酱油的pH为5,则该酱油中的c(H+)=_______ 。
(4)在常温下,柠檬水的pH为3,其中的c(OH-)为_______ (填字母)。
a.0.1 mol∙L−1 b.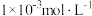 c.
c.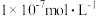 d.
d.
Ⅲ.在25℃时对氨水进行如下操作。请填写下列空白。
(5)若向氨水中加入少量硫酸铵固体,则溶液中 将
将_______ (填“增大”“减小”或“不变”)。
(6)若向氨水中加入稀硫酸,使氨水恰好被中和,写出反应的离子方程式:_______ ;所得溶液的pH_______ 7(填“>”“<”或“=”),用离子方程式表示其原因:_______ 。
(7)若向氨水中加入稀硫酸至溶液的pH=7,此时溶液中 ,则
,则
_______ 。
(8)用硫酸标准溶液滴定氨水,达滴定终点的标志是_______ 。
 )。
)。(1)请写出甲酸的电离方程式
(2)某甲酸溶液中,HCOOH的初始浓度是
 ,当其电离达到平衡时,溶液中的
,当其电离达到平衡时,溶液中的 浓度c的取值范围是_______。
浓度c的取值范围是_______。A. | B. |
C.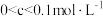 | D. 0 0 |
Ⅱ.完成下列问题
(3)某种酱油的pH为5,则该酱油中的c(H+)=
(4)在常温下,柠檬水的pH为3,其中的c(OH-)为
a.0.1 mol∙L−1 b.
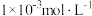 c.
c.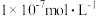 d.
d.
Ⅲ.在25℃时对氨水进行如下操作。请填写下列空白。
(5)若向氨水中加入少量硫酸铵固体,则溶液中
 将
将(6)若向氨水中加入稀硫酸,使氨水恰好被中和,写出反应的离子方程式:
(7)若向氨水中加入稀硫酸至溶液的pH=7,此时溶液中
 ,则
,则
(8)用硫酸标准溶液滴定氨水,达滴定终点的标志是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】镀镍废水是重金属污染源之一,常见处理含镍废水的一种离子交换和沉淀法工艺如下:
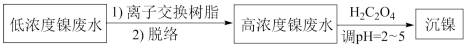
已知该交换树脂为阳离子型树脂HR,HR R-+H+;NiR2(aq)
R-+H+;NiR2(aq) Ni2+(aq)+2R-(aq)。
Ni2+(aq)+2R-(aq)。
(1)Ni2+的核外电子排布式为___________ 。
(2)已知在pH=2时,离子交换过程Ni2+去除率很低,其原因为_______ 。
(3)“脱络”(指镍元素由络合物NiR2转化成游离的Ni2+)过程中,R-与中间产物·OH(羟基自由基)反应生成难以与Ni2+络合的·R(有机物自由基),但·OH也能与H2O2发生反应。反应的方程式如下:
Ⅰ.Fe2++H2O2=Fe3++OH-+·OH
Ⅱ.R-+·OH=OH-+·R
平衡移动的角度解释加入FeSO4和H2O2能够实现“脱络”的原因是___________ 。
(4)NiC2O4隔绝空气高温煅烧可制得Ni2O3,NiC2O4受热分解的化学方程式为___________ 。
(5)硫酸镍铵(NH4)xNiy(SO4)m·nH2O可用于电镀等领域,为测定其组成,进行如下实验:
①称取4.670样品,配成250mL溶液A。
②取25.00mL溶液A,加足量浓NaOH溶液并加热,生成NH3 44.80mL (标准状况)。
③另取25.00mL溶液A,用0.05000mol/L的EDTA(Na2H2Y)标准溶液滴定其中的Ni2+(离子方程式为Ni2++H2Y2-=NiY2-+2H+),平行测定三次,平均消耗标准EDTA溶液20.00mL。
则硫酸镍铵的化学式为___________ (写出计算过程)。

已知该交换树脂为阳离子型树脂HR,HR
 R-+H+;NiR2(aq)
R-+H+;NiR2(aq) Ni2+(aq)+2R-(aq)。
Ni2+(aq)+2R-(aq)。(1)Ni2+的核外电子排布式为
(2)已知在pH=2时,离子交换过程Ni2+去除率很低,其原因为
(3)“脱络”(指镍元素由络合物NiR2转化成游离的Ni2+)过程中,R-与中间产物·OH(羟基自由基)反应生成难以与Ni2+络合的·R(有机物自由基),但·OH也能与H2O2发生反应。反应的方程式如下:
Ⅰ.Fe2++H2O2=Fe3++OH-+·OH
Ⅱ.R-+·OH=OH-+·R
平衡移动的角度解释加入FeSO4和H2O2能够实现“脱络”的原因是
(4)NiC2O4隔绝空气高温煅烧可制得Ni2O3,NiC2O4受热分解的化学方程式为
(5)硫酸镍铵(NH4)xNiy(SO4)m·nH2O可用于电镀等领域,为测定其组成,进行如下实验:
①称取4.670样品,配成250mL溶液A。
②取25.00mL溶液A,加足量浓NaOH溶液并加热,生成NH3 44.80mL (标准状况)。
③另取25.00mL溶液A,用0.05000mol/L的EDTA(Na2H2Y)标准溶液滴定其中的Ni2+(离子方程式为Ni2++H2Y2-=NiY2-+2H+),平行测定三次,平均消耗标准EDTA溶液20.00mL。
则硫酸镍铵的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.氧化还原滴定—取草酸(H2C2O4)溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol·L-1的高锰酸钾溶液滴定,发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。
表格中记录了实验数据:
(1)滴定时,KMnO4溶液应装在______ 式滴定管中,滴定终点时的现象是_______________ 。
(2)该草酸溶液的浓度为__________ 。
II.沉淀滴定――滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。
(3)参考下表中的数据,若用AgNO3滴定NaCl溶液,可选用的指示剂是_____ (填选项字母)。当Cl-恰好沉淀完全时,此时指示剂也恰好开始显色,请问此时指示剂的物质的量浓度为___________________ 。
A.NaSCN B.NaBr C.NaCN D.Na2CrO4
表格中记录了实验数据:
| 滴定次数 | 待测液体积 (mL) | 标准KMnO4溶液体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 3.00 | 23.00 |
| 第三次 | 25.00 | 1.00 | 22.50 |
| 第四次 | 25.00 | 4.00 | 24.10 |
(1)滴定时,KMnO4溶液应装在
(2)该草酸溶液的浓度为
II.沉淀滴定――滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。
(3)参考下表中的数据,若用AgNO3滴定NaCl溶液,可选用的指示剂是
| 难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| Ksp | 1.0×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
A.NaSCN B.NaBr C.NaCN D.Na2CrO4
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】六氯化钨(WCl6)可用作有机合成催化剂,熔点为283℃,沸点为340℃,易溶于CS2,极易水解。实验室中,先将三氧化钨(WO3)还原为金属钨(W)再制备WCl6,装置如图所示(夹持装置略)。回答下列问题:
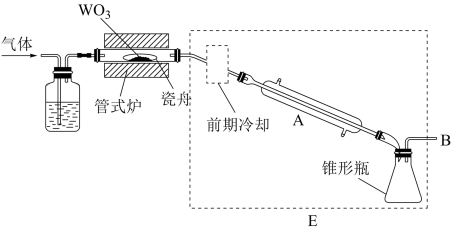
利用碘量法测定WCl6产品纯度,实验如下:
(1)称量:将足量CS2(易挥发)加入干燥的称量瓶中,盖紧称重为m1g;开盖并计时1分钟,盖紧称重为m2g;再开盖加入待测样品并计时1分钟,盖紧称重为m3g,则样品质量为_______ g(不考虑空气中水蒸气的干扰)。
(2)滴定:先将WCl6转化为可溶的Na2WO4,通过IO 离子交换柱发生反应:WO
离子交换柱发生反应:WO +Ba(IO3)2=BaWO4+2IO
+Ba(IO3)2=BaWO4+2IO ;交换结束后,向所得含IO
;交换结束后,向所得含IO 的溶液中加入适量酸化的KI溶液,发生反应:IO
的溶液中加入适量酸化的KI溶液,发生反应:IO +5I-+6H+=3I2+3H2O;反应完全后,用Na2S2O3标准溶液滴定,发生反应:I2+2S2O
+5I-+6H+=3I2+3H2O;反应完全后,用Na2S2O3标准溶液滴定,发生反应:I2+2S2O =2I-+S4O
=2I-+S4O 。滴定达终点时消耗cmol•L-1的Na2S2O3溶液VmL。称量时,若加入待测样品后,开盖时间超过1分钟,则滴定时消耗Na2S2O3溶液的体积将
。滴定达终点时消耗cmol•L-1的Na2S2O3溶液VmL。称量时,若加入待测样品后,开盖时间超过1分钟,则滴定时消耗Na2S2O3溶液的体积将_______ (填“偏大”“偏小”或“不变”),样品中WCl6质量分数的测定值将_______ (填“偏大”“偏小”或“不变”)。

利用碘量法测定WCl6产品纯度,实验如下:
(1)称量:将足量CS2(易挥发)加入干燥的称量瓶中,盖紧称重为m1g;开盖并计时1分钟,盖紧称重为m2g;再开盖加入待测样品并计时1分钟,盖紧称重为m3g,则样品质量为
(2)滴定:先将WCl6转化为可溶的Na2WO4,通过IO
 离子交换柱发生反应:WO
离子交换柱发生反应:WO +Ba(IO3)2=BaWO4+2IO
+Ba(IO3)2=BaWO4+2IO ;交换结束后,向所得含IO
;交换结束后,向所得含IO 的溶液中加入适量酸化的KI溶液,发生反应:IO
的溶液中加入适量酸化的KI溶液,发生反应:IO +5I-+6H+=3I2+3H2O;反应完全后,用Na2S2O3标准溶液滴定,发生反应:I2+2S2O
+5I-+6H+=3I2+3H2O;反应完全后,用Na2S2O3标准溶液滴定,发生反应:I2+2S2O =2I-+S4O
=2I-+S4O 。滴定达终点时消耗cmol•L-1的Na2S2O3溶液VmL。称量时,若加入待测样品后,开盖时间超过1分钟,则滴定时消耗Na2S2O3溶液的体积将
。滴定达终点时消耗cmol•L-1的Na2S2O3溶液VmL。称量时,若加入待测样品后,开盖时间超过1分钟,则滴定时消耗Na2S2O3溶液的体积将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】价—类二维图是学习元素化学的重要方法。如图为硫及其化合物的价—类二维图,请正确回答下列问题。

(1)填写图中缺失的类别A___ 和化学式B___ 。
(2)图中物质属于弱电解质的是___ (填化学式)。
(3)某同学利用价—类二维图预测H2S的性质,下列试剂可能与之发生反应的有___ 。
a.石蕊溶液 b.Fe c.KMnO4溶液 d.CuSO4溶液
(4)浓硫酸能使硫酸铜晶体变白,体现了浓硫酸的___ 性;与木炭在加热条件下剧烈反应,体现了浓硫酸的___ 性。下列气体可以用浓硫酸干燥的是___ 。
a.HBr b.SO2 c.Cl2 d.NH3
(5)硫代硫酸钠(Na2S2O3)常用于测定溶液中碘的含量,其反应方程式为:2Na2S2O3+I2=Na2S4O6+2NaI。
①反应中被氧化的元素为___ 。
②用单线桥法标出电子转移情况___ 。
③取某含碘样品溶液100mL,加入2滴淀粉溶液,不断滴加0.2000mol/L的Na2S2O3溶液至溶液恰好褪色(且半分钟内不变色),消耗Na2S2O3溶液21.82mL。则原样品中碘单质的浓度为___ mol/L。

(1)填写图中缺失的类别A
(2)图中物质属于弱电解质的是
(3)某同学利用价—类二维图预测H2S的性质,下列试剂可能与之发生反应的有
a.石蕊溶液 b.Fe c.KMnO4溶液 d.CuSO4溶液
(4)浓硫酸能使硫酸铜晶体变白,体现了浓硫酸的
a.HBr b.SO2 c.Cl2 d.NH3
(5)硫代硫酸钠(Na2S2O3)常用于测定溶液中碘的含量,其反应方程式为:2Na2S2O3+I2=Na2S4O6+2NaI。
①反应中被氧化的元素为
②用单线桥法标出电子转移情况
③取某含碘样品溶液100mL,加入2滴淀粉溶液,不断滴加0.2000mol/L的Na2S2O3溶液至溶液恰好褪色(且半分钟内不变色),消耗Na2S2O3溶液21.82mL。则原样品中碘单质的浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】实验室用硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]滴定法测定铬铁矿中铬含量的过程如下:
酸溶:准确称取0.1950 g铬铁矿试样放入锥形瓶中,加入适量磷酸和硫酸的混合酸,加热使试样完全溶解,冷却。
氧化:向上述溶液中滴加5滴1%的MnSO4溶液,再加入一定量的过硫酸铵[(NH4)2S2O8]溶液,摇匀,加热煮沸至出现紫红色,继续加热煮沸至紫红色褪去,冷却。[已知:①2Mn2+ + 5S2O82- + 8H2O = 10SO42- + 2MnO4- + 16H+;②继续加热煮沸后,溶液中过量(NH4)2S2O8和生成的HMnO4已分解除去]
滴定:用0.2050mol·L-1(NH4)2Fe(SO4)2标准溶液滴定上述溶液至终点,消耗19.50 mL标准溶液。(已知:Cr2O72-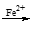 Cr3+)
Cr3+)
(1)过硫酸铵保存在棕色试剂瓶中的原因是___________ 。
(2)①“氧化”的目的是将试样溶液中的Cr3+氧化成Cr2O72-,加入5滴MnSO4溶液的目的是________________ (已知该条件下还原性:Cr3+ > Mn2+)。
②“氧化”过程中,如果继续加热煮沸时间不充足,会使铬含量的测定结果______ (填“偏大”“不变”或“偏小”)。
(3)计算铬铁矿中铬的质量分数(写出计算过程)。___________
酸溶:准确称取0.1950 g铬铁矿试样放入锥形瓶中,加入适量磷酸和硫酸的混合酸,加热使试样完全溶解,冷却。
氧化:向上述溶液中滴加5滴1%的MnSO4溶液,再加入一定量的过硫酸铵[(NH4)2S2O8]溶液,摇匀,加热煮沸至出现紫红色,继续加热煮沸至紫红色褪去,冷却。[已知:①2Mn2+ + 5S2O82- + 8H2O = 10SO42- + 2MnO4- + 16H+;②继续加热煮沸后,溶液中过量(NH4)2S2O8和生成的HMnO4已分解除去]
滴定:用0.2050mol·L-1(NH4)2Fe(SO4)2标准溶液滴定上述溶液至终点,消耗19.50 mL标准溶液。(已知:Cr2O72-
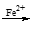 Cr3+)
Cr3+)(1)过硫酸铵保存在棕色试剂瓶中的原因是
(2)①“氧化”的目的是将试样溶液中的Cr3+氧化成Cr2O72-,加入5滴MnSO4溶液的目的是
②“氧化”过程中,如果继续加热煮沸时间不充足,会使铬含量的测定结果
(3)计算铬铁矿中铬的质量分数(写出计算过程)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是一些物质在常温时的电离平衡常数:
(1)表中①②③④的酸性由强到弱的顺序为___________ (填标号)。
(2)常温下,0.1 mol/L NaHC2O4溶液显___________ (填“酸”、“碱”或“中”)性,理由是___________ 。
(3)请写出向 溶液中通入少量CO2气体发生反应的离子方程式:
溶液中通入少量CO2气体发生反应的离子方程式:___________ 。
(4)等浓度的(NH4)2CO3、(NH4)2C2O4、NH4Cl、CH3COONH4溶液中 的浓度由大到小的顺序是
的浓度由大到小的顺序是___________ 。
(5)等浓度、等体积的醋酸和氨水混合后溶液中各离子浓度大小关系是___________ 。
(6)向等体积、等pH的醋酸和草酸溶液中分别加入足量的质量、大小都相同的镁条,反应结束后收集到氢气的体积分别为V1、V2,其大小关系为___________ ,反应相同时间内的平均反应速率分别为v1、v2,其大小关系为___________ 。
(7)请利用以下装置和提供的试剂(乙酸溶液、碳酸钠粉末、饱和碳酸钠溶液、饱和碳酸氢钠溶液、苯酚钠溶液)设计比较CH3COOH、H2CO3和 酸性强弱的实验方案:
酸性强弱的实验方案:_______ (要说明各装置盛装的溶液)。
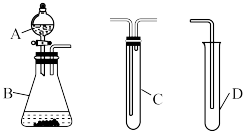
| ① | ② | ③ | ④ | ⑤ | |
| 物质 | CH3COOH | H2CO3 | H2C2O4 |  | NH3·H2O |
| K | 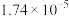 | 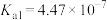  | 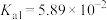 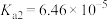 | 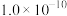 | 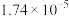 |
(2)常温下,0.1 mol/L NaHC2O4溶液显
(3)请写出向
 溶液中通入少量CO2气体发生反应的离子方程式:
溶液中通入少量CO2气体发生反应的离子方程式:(4)等浓度的(NH4)2CO3、(NH4)2C2O4、NH4Cl、CH3COONH4溶液中
 的浓度由大到小的顺序是
的浓度由大到小的顺序是(5)等浓度、等体积的醋酸和氨水混合后溶液中各离子浓度大小关系是
(6)向等体积、等pH的醋酸和草酸溶液中分别加入足量的质量、大小都相同的镁条,反应结束后收集到氢气的体积分别为V1、V2,其大小关系为
(7)请利用以下装置和提供的试剂(乙酸溶液、碳酸钠粉末、饱和碳酸钠溶液、饱和碳酸氢钠溶液、苯酚钠溶液)设计比较CH3COOH、H2CO3和
 酸性强弱的实验方案:
酸性强弱的实验方案:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为_______ 。
(2)同浓度的CH3COO-、 、
、 、ClO-结合H+的能力由强到弱的顺序为
、ClO-结合H+的能力由强到弱的顺序为_______ 。
(3)将少量CO2气体通入NaClO溶液中,写出反应的化学方程式:_______ 。
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
请回答下列问题:
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为
(2)同浓度的CH3COO-、
 、
、 、ClO-结合H+的能力由强到弱的顺序为
、ClO-结合H+的能力由强到弱的顺序为(3)将少量CO2气体通入NaClO溶液中,写出反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)水能发生自耦电离: ,液氨中
,液氨中 能发生类似的电离过程,液氨自耦电离的平衡常数表达式为
能发生类似的电离过程,液氨自耦电离的平衡常数表达式为_______ 。
(2)实验室常用NaOH溶液进行洗气,当用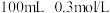 的NaOH溶液吸收标准状况下
的NaOH溶液吸收标准状况下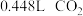 时,所得溶液中各离子浓度由大到小的顺序为
时,所得溶液中各离子浓度由大到小的顺序为_______ 。
(3)已知HnA为n元弱酸。写出HnA与足量NaOH反应的离子方程式:_______ 。HnA的电离方程式为_______ (写出最后一步电离)。
(4)联氨为二元弱碱,在水中的电离方式与氨相似。25℃联氨第一 步电离反应的平衡常数值为_______ (已知:N2H4+H+
 的 K=8.7×107)。联氨与硫酸形成的酸式盐的化学式为
的 K=8.7×107)。联氨与硫酸形成的酸式盐的化学式为_______ 。
(1)水能发生自耦电离:
 ,液氨中
,液氨中 能发生类似的电离过程,液氨自耦电离的平衡常数表达式为
能发生类似的电离过程,液氨自耦电离的平衡常数表达式为(2)实验室常用NaOH溶液进行洗气,当用
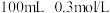 的NaOH溶液吸收标准状况下
的NaOH溶液吸收标准状况下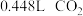 时,所得溶液中各离子浓度由大到小的顺序为
时,所得溶液中各离子浓度由大到小的顺序为(3)已知HnA为n元弱酸。写出HnA与足量NaOH反应的离子方程式:
(4)联氨为二元弱碱,在水中的电离方式与氨相似。25℃联氨第一 步电离反应的平衡常数值为

 的 K=8.7×107)。联氨与硫酸形成的酸式盐的化学式为
的 K=8.7×107)。联氨与硫酸形成的酸式盐的化学式为
您最近一年使用:0次



