铁的硫化物被认为是有前景的锂电池材料,但导电性较差,放电时易膨胀。
(1)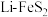 电池是综合性能较好的一种电池。
电池是综合性能较好的一种电池。
①水热法合成 纳米颗粒的方法是将等物质的量的
纳米颗粒的方法是将等物质的量的 、
、 、
、 研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为
研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为___________ 。
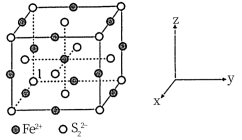
② 晶体的晶胞结构示意图如图所示,离子1的分数坐标是
晶体的晶胞结构示意图如图所示,离子1的分数坐标是 ,则离子1最近的
,则离子1最近的 分数坐标为
分数坐标为___________ (任写一个),每个 周围距离最近且相等的
周围距离最近且相等的 有
有___________ 个。
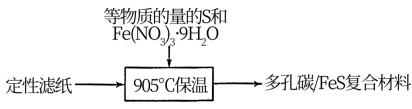
(2)①将 镶嵌在多孔碳中制成多孔碳/
镶嵌在多孔碳中制成多孔碳/ 复合材料,该电极材料相较
复合材料,该电极材料相较 具有的优势是放电时不易膨胀且
具有的优势是放电时不易膨胀且___________ 。多孔碳/ 复合材料制取方法如下,定性滤纸的作用是提供碳源和
复合材料制取方法如下,定性滤纸的作用是提供碳源和___________ 。
②分别取多孔碳、多孔碳/ 电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/
电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/ 最终转化为
最终转化为 ,固体残留率为50%。
,固体残留率为50%。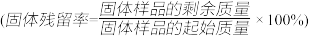
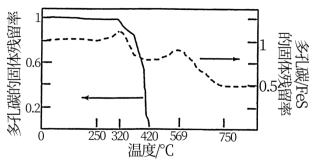
420℃~569℃时,多孔碳/ 固体残留率增大的原因是
固体残留率增大的原因是___________ 。
③ 做为锂电池正极材料,放电时先后发生如下反应:
做为锂电池正极材料,放电时先后发生如下反应: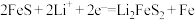
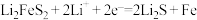
该多孔碳/ 电极质量为4.8g,该电极理论上最多可以得电子
电极质量为4.8g,该电极理论上最多可以得电子___________  。(写出计算过程)
。(写出计算过程)
(1)
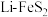 电池是综合性能较好的一种电池。
电池是综合性能较好的一种电池。①水热法合成
 纳米颗粒的方法是将等物质的量的
纳米颗粒的方法是将等物质的量的 、
、 、
、 研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为
研磨置于反应釜中,加入蒸馏水加热使之恰好反应,该反应的化学方程式为②
 晶体的晶胞结构示意图如图所示,离子1的分数坐标是
晶体的晶胞结构示意图如图所示,离子1的分数坐标是 ,则离子1最近的
,则离子1最近的 分数坐标为
分数坐标为 周围距离最近且相等的
周围距离最近且相等的 有
有
(2)①将
 镶嵌在多孔碳中制成多孔碳/
镶嵌在多孔碳中制成多孔碳/ 复合材料,该电极材料相较
复合材料,该电极材料相较 具有的优势是放电时不易膨胀且
具有的优势是放电时不易膨胀且 复合材料制取方法如下,定性滤纸的作用是提供碳源和
复合材料制取方法如下,定性滤纸的作用是提供碳源和
②分别取多孔碳、多孔碳/
 电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/
电极在氧气中加热,测得固体残留率随温度变化情况如图所示,多孔碳/ 最终转化为
最终转化为 ,固体残留率为50%。
,固体残留率为50%。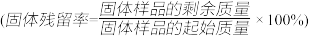

420℃~569℃时,多孔碳/
 固体残留率增大的原因是
固体残留率增大的原因是③
 做为锂电池正极材料,放电时先后发生如下反应:
做为锂电池正极材料,放电时先后发生如下反应: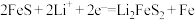
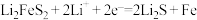
该多孔碳/
 电极质量为4.8g,该电极理论上最多可以得电子
电极质量为4.8g,该电极理论上最多可以得电子 。(写出计算过程)
。(写出计算过程)
更新时间:2021-01-22 09:43:55
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】我国科学家用粗氢氧化高钴[Co(OH)3]制备硫酸钴晶体(CoSO4∙7H2O),其工艺流程如下。

已知:ⅰ.还原浸出液中的阳离子有:Co2+、H+、Fe2+和Ca2+等
iⅱ.部分物质的溶度积常数如下(25℃)
ⅲ.CoSO4∙7H2O溶解度随温度升高而明显增大
(1)氢氧化高钴溶于硫酸的化学方程式是_____________ 。
(2)浸出Co2+时,理论上氧化剂和还原剂物质的量之比为_____________ 。
(3)写出“氧化沉铁”的离子方程式_____________ ;
25℃时,浊液中铁离子浓度为_____________ mol/L(此时pH为4)。
(4)结合平衡移动原理解释“氟化沉钙”步骤加入过量NaF的原因_____________ 。
(5)P507萃取后,经反萃取得到硫酸钴溶液,将硫酸钴溶液经_____________ 操作,得到硫酸钴晶体。
(6)用滴定法测定硫酸钴晶体中的钴含量,其原理和操作如下。
在溶液中,用铁氰化钾将Co(Ⅱ)氧化为Co(Ⅲ),过量的铁氰化钾以Co(Ⅱ)标准液返滴定。反应的方程式为: 。
。
已知:铁氰化钾标准液浓度为c mol/L,Co(Ⅱ)标准液质量浓度为ρg/L。
取mg硫酸钴晶体,加水配成200mL溶液,取20mL待测液进行滴定,消耗V1mL铁氰化钾标准液、V2mL Co(Ⅱ)标准液。
计算样品中钴含量ω=_____________ (以钴的质量分数ω计)。

已知:ⅰ.还原浸出液中的阳离子有:Co2+、H+、Fe2+和Ca2+等
iⅱ.部分物质的溶度积常数如下(25℃)
物质 | Ksp |
CaF2 |
|
Fe(OH)3 |
|
(1)氢氧化高钴溶于硫酸的化学方程式是
(2)浸出Co2+时,理论上氧化剂和还原剂物质的量之比为
(3)写出“氧化沉铁”的离子方程式
25℃时,浊液中铁离子浓度为
(4)结合平衡移动原理解释“氟化沉钙”步骤加入过量NaF的原因
(5)P507萃取后,经反萃取得到硫酸钴溶液,将硫酸钴溶液经
(6)用滴定法测定硫酸钴晶体中的钴含量,其原理和操作如下。
在溶液中,用铁氰化钾将Co(Ⅱ)氧化为Co(Ⅲ),过量的铁氰化钾以Co(Ⅱ)标准液返滴定。反应的方程式为:
 。
。已知:铁氰化钾标准液浓度为c mol/L,Co(Ⅱ)标准液质量浓度为ρg/L。
取mg硫酸钴晶体,加水配成200mL溶液,取20mL待测液进行滴定,消耗V1mL铁氰化钾标准液、V2mL Co(Ⅱ)标准液。
计算样品中钴含量ω=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】由含碘废水制取碘酸钾的一种工艺如下:
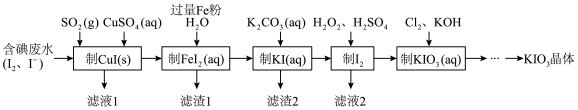
⑴ 写出KIO3在日常生活中的一个重要应用________________________ 。
⑵ 检验“含碘废水”中是否含有单质I2的常用试剂是________ (写试剂名称)。
⑶ 通入SO2的目的是将I2还原为I-,该反应的离子方程式为______________________ 。
⑷ 工艺中五种物质的制备反应中,不涉及氧化还原反应的步骤是“制________ ”。
⑸ “制KI(aq)”时,该温度下水的离子积为Kw=1.0×10-13,Ksp[Fe(OH)2]=9.0×10-15。
为避免0.9 mol·L-1 FeI2溶液中Fe2+水解生成胶状物吸附I-,起始加入K2CO3必须保持溶液的pH不大于______ 。
⑹ “制KIO3溶液”反应的离子方程式为__________________ 。

⑺ KCl、KIO3的溶解度曲线如图所示。流程中由“KIO3(aq)”得到KIO3晶体的操作步骤为_____________________ 。

⑴ 写出KIO3在日常生活中的一个重要应用
⑵ 检验“含碘废水”中是否含有单质I2的常用试剂是
⑶ 通入SO2的目的是将I2还原为I-,该反应的离子方程式为
⑷ 工艺中五种物质的制备反应中,不涉及氧化还原反应的步骤是“制
⑸ “制KI(aq)”时,该温度下水的离子积为Kw=1.0×10-13,Ksp[Fe(OH)2]=9.0×10-15。
为避免0.9 mol·L-1 FeI2溶液中Fe2+水解生成胶状物吸附I-,起始加入K2CO3必须保持溶液的pH不大于
⑹ “制KIO3溶液”反应的离子方程式为

⑺ KCl、KIO3的溶解度曲线如图所示。流程中由“KIO3(aq)”得到KIO3晶体的操作步骤为
您最近一年使用:0次
【推荐3】回收钴废料能有效缓解金属资源浪费、环境污染等问题。一种以含钴催化剂废料(主要含Co、Fe,还含有少量的CoO、FeO、Fe2O3、BaO)制备氧化钴(Co2O3)的工艺流程如图所示:
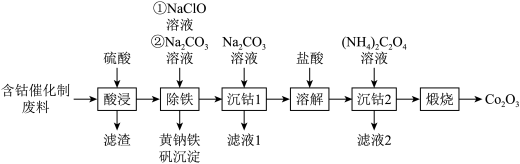
已知:i.金属钴与铁具有相似的化学性质:
ii.氧化性Co3+>ClO-。
回答下列问题:
(1)“酸浸”后,“滤渣”的主要成分有_____ (填化学式)。
(2)“除铁”时先加入NaClO溶液,主要反应的离子方程式为_____ ,再加入Na2CO3溶液调节pH为2.5~3.0,生成黄钠铁矾沉淀。
(3)“滤液2”中主要溶质的化合物类型:______ (填“离子化合物”或“共价化合物”)。
(4)“沉钴2”中产生的CoC2O4在空气中“煅烧”同时只产生使澄清石灰水变浑浊的气体,该反应的化学方程式为:______ ,若取50 g含钴催化剂废料,将按以上流程中的“煅烧”后产生的气体通入澄清石灰水中,得到100 g白色沉淀,则含钴催化剂废料中钴元素的质量分数为:_____ 。(相对原子质量:Co:59、Ca:40、C:12、O:16)

已知:i.金属钴与铁具有相似的化学性质:
ii.氧化性Co3+>ClO-。
回答下列问题:
(1)“酸浸”后,“滤渣”的主要成分有
(2)“除铁”时先加入NaClO溶液,主要反应的离子方程式为
(3)“滤液2”中主要溶质的化合物类型:
(4)“沉钴2”中产生的CoC2O4在空气中“煅烧”同时只产生使澄清石灰水变浑浊的气体,该反应的化学方程式为:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)锌锰干电池是应用最普遍的电池之一(如图所示),锌锰干电池的负极材料是______ ,负极发生的电极反应方程式为_______ 。若反应消耗16.25 g负极材料,则电池中转移电子的物质的量为________ mol。
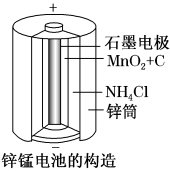
(2)目前常用的镍(Ni)镉(Cd)电池总反应式可以表示为:Cd+2NiO(OH)+2H2O 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是________ 。
A.Cd是负极 B.Ni(OH)2是正极
C.充电时化学能转变为电能 D.放电时化学能转变为电能
(3)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知X极为电池的________ (填“正”或“负”)极,Y极的电极反应为________ (填“氧化”或“还原”)反应。

(1)锌锰干电池是应用最普遍的电池之一(如图所示),锌锰干电池的负极材料是

(2)目前常用的镍(Ni)镉(Cd)电池总反应式可以表示为:Cd+2NiO(OH)+2H2O
 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均难溶于水,但能溶于酸,以下说法中正确的是A.Cd是负极 B.Ni(OH)2是正极
C.充电时化学能转变为电能 D.放电时化学能转变为电能
(3)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知X极为电池的

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】某地区利用其自然资源建立的工业体系如下图所示。
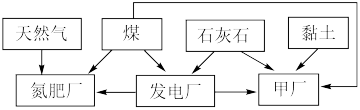
回答下列问题:
(1)“甲厂”为提高反应速率和原料的利用率,应先将石灰石进行___________ 处理。依据所使用的资源分析,“甲厂”的产品是___________ 。
(2)天然气中含有少量有害气体 ,常用NaOH溶液进行洗涤除去,反应的离子方程式为
,常用NaOH溶液进行洗涤除去,反应的离子方程式为___________ 。若改为使用三乙醇胺[N(CH2CH2OH)3]溶液洗涤,则每年节约资金可达百万元。已知在常温下三乙醇胺为液体,沸点为380℃,与 的反应为
的反应为 。解释能节约资金的原因
。解释能节约资金的原因___________ 。
(3)煤中含有一定量 。为减少大气污染,在煤燃烧发电时需加入石灰石脱硫,简称“钙基固硫”,“钙基固硫”最终得到的含硫物质的化学式为
。为减少大气污染,在煤燃烧发电时需加入石灰石脱硫,简称“钙基固硫”,“钙基固硫”最终得到的含硫物质的化学式为___________ 。后来改为在煤燃烧前,用 溶液溶解煤中的
溶液溶解煤中的 进行脱硫,写出反应化学方程式
进行脱硫,写出反应化学方程式___________ 。
(4)氮肥厂产生的“氨氮”废水中含有铵盐,直接排放会产生水体污染。传统的处理方法有多种。近年,电化学处理“氨氮”废水成为了研究热点,其中的一种原理如下图所示。
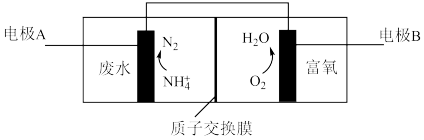
①检验废水中含有 的操作是
的操作是___________ 。
②电极B是___________ 极。
③写出电极A上发生的电极反应式___________ 。

回答下列问题:
(1)“甲厂”为提高反应速率和原料的利用率,应先将石灰石进行
(2)天然气中含有少量有害气体
 ,常用NaOH溶液进行洗涤除去,反应的离子方程式为
,常用NaOH溶液进行洗涤除去,反应的离子方程式为 的反应为
的反应为 。解释能节约资金的原因
。解释能节约资金的原因(3)煤中含有一定量
 。为减少大气污染,在煤燃烧发电时需加入石灰石脱硫,简称“钙基固硫”,“钙基固硫”最终得到的含硫物质的化学式为
。为减少大气污染,在煤燃烧发电时需加入石灰石脱硫,简称“钙基固硫”,“钙基固硫”最终得到的含硫物质的化学式为 溶液溶解煤中的
溶液溶解煤中的 进行脱硫,写出反应化学方程式
进行脱硫,写出反应化学方程式(4)氮肥厂产生的“氨氮”废水中含有铵盐,直接排放会产生水体污染。传统的处理方法有多种。近年,电化学处理“氨氮”废水成为了研究热点,其中的一种原理如下图所示。

①检验废水中含有
 的操作是
的操作是②电极B是
③写出电极A上发生的电极反应式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某小组研究Cu2+和Fe3+的氧化性,进行如下实验。
实验Ⅰ: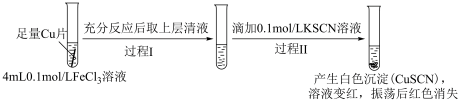
已知:1.(SCN)2 是黄色液体,氧化性:I2 < (SCN)2 < Br2。
2.K3[Fe(CN)6]溶液可用于Fe2+的检验,生成蓝色沉淀。
3.Fe3+与SCN-可以形成多种微粒,例如[Fe(SCN)]2+、Fe(SCN)3等溶液显红色。
(1)实验Ⅰ过程Ⅰ中Cu与FeCl3反应的化学方程式是___________ 。
(2)实验Ⅰ过程Ⅱ中溶液变红,说明产生了Fe3+,分析可能原因。
假设①:Fe2+被Cu2+氧化。
过程Ⅱ发生反应的电极反应式:
a.氧化反应:Fe2+-e-+3SCN-=Fe(SCN)3
b.还原反应:___________ 。
假设②:Cu2+和SCN-发生反应生成(SCN)2,进而将清液中的Fe2+氧化为Fe3+。
设计实验Ⅱ证实假设。
实验Ⅱ: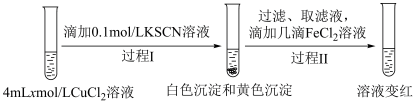
i.
___________ 。
ⅱ.实验Ⅱ中过程Ⅱ的离子方程式为___________ 。
(3)设计实验进一步研究Fe3+能否氧化SCN-。
实验Ⅲ:
①实验Ⅲ中加入K3[Fe(CN)6]溶液后,若___________ (写出实验现象),
说明在该实验条件下,Fe3+未能氧化SCN-。
②进一步查阅资料发现:Fe3+与SCN-可以发生氧化还原反应。该小组通过实验证明了该反应的发生。请你在答题卡方框中用文字或图示 设计实验方案,并描述相关的实验现象:___________ 。
实验Ⅰ:

已知:1.(SCN)2 是黄色液体,氧化性:I2 < (SCN)2 < Br2。
2.K3[Fe(CN)6]溶液可用于Fe2+的检验,生成蓝色沉淀。
3.Fe3+与SCN-可以形成多种微粒,例如[Fe(SCN)]2+、Fe(SCN)3等溶液显红色。
(1)实验Ⅰ过程Ⅰ中Cu与FeCl3反应的化学方程式是
(2)实验Ⅰ过程Ⅱ中溶液变红,说明产生了Fe3+,分析可能原因。
假设①:Fe2+被Cu2+氧化。
过程Ⅱ发生反应的电极反应式:
a.氧化反应:Fe2+-e-+3SCN-=Fe(SCN)3
b.还原反应:
假设②:Cu2+和SCN-发生反应生成(SCN)2,进而将清液中的Fe2+氧化为Fe3+。
设计实验Ⅱ证实假设。
实验Ⅱ:

i.

ⅱ.实验Ⅱ中过程Ⅱ的离子方程式为
(3)设计实验进一步研究Fe3+能否氧化SCN-。
实验Ⅲ:

①实验Ⅲ中加入K3[Fe(CN)6]溶液后,若
说明在该实验条件下,Fe3+未能氧化SCN-。
②进一步查阅资料发现:Fe3+与SCN-可以发生氧化还原反应。该小组通过实验证明了该反应的发生。请你在
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】铁、铜都是重要的过渡元素,它们的单质和化合物在生活、生产中有广泛应用。
(1)基态Fe原子价电子轨道表示式为__________________ 。
(2)已知铜的配合物A的结构简式如图所示。 的配位数为
的配位数为________ ,该配合物中的第二周期元素的电负性由大到小的顺序为__________ 。
②配体氨基乙酸根(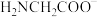 )受热分解可产生
)受热分解可产生 和
和 ,
, 的VSEPR模型名称为
的VSEPR模型名称为_________ 。
(3)亚铁氰化钾,化学式为 ,呈黄色结晶性粉末。
,呈黄色结晶性粉末。 中配体
中配体 的配位原子是
的配位原子是________ (填元素符号), 中C原子的杂化方式为
中C原子的杂化方式为__________ , 中
中 键和
键和 键的数目之比为
键的数目之比为______ 。
(4) 呈黑色或灰黑色,已知:晶胞中
呈黑色或灰黑色,已知:晶胞中 的位置如图1所示,
的位置如图1所示, 位于
位于 所构成的四面体中心,晶胞的侧视图如图2所示。则
所构成的四面体中心,晶胞的侧视图如图2所示。则 配位数为
配位数为_______ 。已知图1中A原子的原子分数坐标为 ,则与A原子距离最近的
,则与A原子距离最近的 的原子分数坐标为
的原子分数坐标为_________ 。
(1)基态Fe原子价电子轨道表示式为
(2)已知铜的配合物A的结构简式如图所示。

 的配位数为
的配位数为②配体氨基乙酸根(
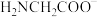 )受热分解可产生
)受热分解可产生 和
和 ,
, 的VSEPR模型名称为
的VSEPR模型名称为(3)亚铁氰化钾,化学式为
 ,呈黄色结晶性粉末。
,呈黄色结晶性粉末。 中配体
中配体 的配位原子是
的配位原子是 中C原子的杂化方式为
中C原子的杂化方式为 中
中 键和
键和 键的数目之比为
键的数目之比为(4)
 呈黑色或灰黑色,已知:晶胞中
呈黑色或灰黑色,已知:晶胞中 的位置如图1所示,
的位置如图1所示, 位于
位于 所构成的四面体中心,晶胞的侧视图如图2所示。则
所构成的四面体中心,晶胞的侧视图如图2所示。则 配位数为
配位数为 ,则与A原子距离最近的
,则与A原子距离最近的 的原子分数坐标为
的原子分数坐标为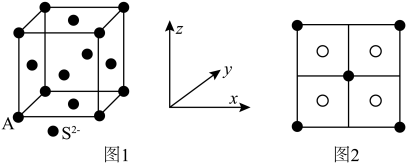
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】化学中的某些元素是与生命活动密不可分的元素,请回答下列问题。
(1)NH4NO3是一种重要的化学肥料,其中N原子的杂化方式是______ 。
(2)维生素C是一种水溶性维生素,水果和蔬菜中含量丰富,该物质结构简式如图所示。以下关于维生素C的说法正确的是______ 。
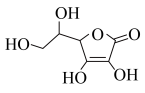
a.分子中既含有极性键又含有非极性键
b.1 mol 分子中含有4 mol π键
c.该物质的熔点可能高于NaCl
d.分子中所含元素电负性由大到小的顺序为O>C>H
(3)维生素C晶体溶于水的过程中要克服的微粒间作用力有______ 。
(4)KSCN溶液可用于Fe3+的检验,原因是铁离子外围有较多能量相近的空轨道,因此能与一些分子或离子形成配合物。Fe3+的价电子排布为______ ,与之形成配合物的分子或离子中的配位原子应具备的结构特征是______ 。
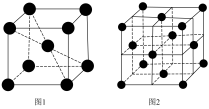
(5)1183K以下纯铁晶体的晶胞如图1所示,1183K以上则转变为图2所示晶胞,则图1和图2中,铁原子的配位数之比为______ 。
(1)NH4NO3是一种重要的化学肥料,其中N原子的杂化方式是
(2)维生素C是一种水溶性维生素,水果和蔬菜中含量丰富,该物质结构简式如图所示。以下关于维生素C的说法正确的是

a.分子中既含有极性键又含有非极性键
b.1 mol 分子中含有4 mol π键
c.该物质的熔点可能高于NaCl
d.分子中所含元素电负性由大到小的顺序为O>C>H
(3)维生素C晶体溶于水的过程中要克服的微粒间作用力有
(4)KSCN溶液可用于Fe3+的检验,原因是铁离子外围有较多能量相近的空轨道,因此能与一些分子或离子形成配合物。Fe3+的价电子排布为
(5)1183K以下纯铁晶体的晶胞如图1所示,1183K以上则转变为图2所示晶胞,则图1和图2中,铁原子的配位数之比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】下表为周期表的一部分,请参照元素在表中的位置,回答下列问题:
(1)画出元素⑥的离子结构示意图_____________________ 。
(2)元素④的简单离子半径_____ 元素⑤的简单离子半径(填“>”、“=”“<”)。
(3)⑤和⑦的最高价氧化物对应水化物的碱性由强到弱的顺序为___________ (填化学式);
(4)②和④的氢化物的稳定性由强到弱的顺序为________________ (填化学式)。
(5)④⑤两种元素的原子按1:1组成的常见化合物的电子式为_______________ 。
(6)元素①的氟化物与元素③的氢化物相遇,立即化合生成白色固体,写出该白色固体的结构式,并标注出其中的配位键______________ 。
(7)元素①的最高价氧化物所对应水化物是一元弱酸,本身不能电离出 H+,写出其在水中的电离方程式____________________ 。
(8)元素⑧对应的含氧酸有H2SeO3和H2SeO4,其中H2SeO3的 K1和 K2分别为 2.7×10-3和 2.5×10-8,H2SeO4第一步几乎完全电离,K2为1.2×10-2,请根据结构与性质的关系,解释 H2SeO4比 H2SeO3酸性强的原因___________________ 。
(9)元素②的一种单质具有导电性,其结构如右图所示:
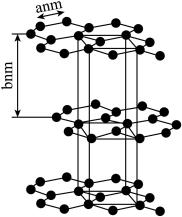
①该单质与金刚石互为_______________________ ;
②12.0 g该单质的体积为________________ cm3(用a、b表示)。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ||||||
| 4 | ⑦ | ⑧ |
(1)画出元素⑥的离子结构示意图
(2)元素④的简单离子半径
(3)⑤和⑦的最高价氧化物对应水化物的碱性由强到弱的顺序为
(4)②和④的氢化物的稳定性由强到弱的顺序为
(5)④⑤两种元素的原子按1:1组成的常见化合物的电子式为
(6)元素①的氟化物与元素③的氢化物相遇,立即化合生成白色固体,写出该白色固体的结构式,并标注出其中的配位键
(7)元素①的最高价氧化物所对应水化物是一元弱酸,本身不能电离出 H+,写出其在水中的电离方程式
(8)元素⑧对应的含氧酸有H2SeO3和H2SeO4,其中H2SeO3的 K1和 K2分别为 2.7×10-3和 2.5×10-8,H2SeO4第一步几乎完全电离,K2为1.2×10-2,请根据结构与性质的关系,解释 H2SeO4比 H2SeO3酸性强的原因
(9)元素②的一种单质具有导电性,其结构如右图所示:

①该单质与金刚石互为
②12.0 g该单质的体积为
您最近一年使用:0次





