实验室通常是在NH3和NH4Cl存在条件下,以活性炭为催化剂,用H2O2氧化CoCl2溶液来制备三氯化六氨合钴[Co(NH3)6]Cl3,该反应属于大量放热的反应。某小组用如图所示装置制备[Co(NH3)6]Cl3,实验步骤如下:
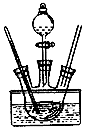
Ⅰ.称取研细的CoCl2•6H2O10.0g和NH4Cl5.0g于烧杯中溶解,将溶液转入三颈烧瓶,加入25mL浓氨水和适量活性炭粉末,逐滴加入5mL30%的H2O2溶液。
Ⅱ.用水浴将混合物加热至60℃,恒温20分钟,然后用冰水浴冷却,充分结晶后过滤。
Ⅲ.将沉淀溶于热的盐酸中,趁热过滤,滤液中加适量浓盐酸并冷却结晶。
Ⅳ.过滤、用乙醇洗涤晶体并在105℃条件下烘干。
试回答下列问题:
(1)制备[Co(NH3)6]Cl3的化学方程式是___ 。
(2)请指出装置中存在的一处缺陷___ 。
(3)若将5mL30%的H2O2溶液一次性加入三颈烧瓶,会出现的问题是__ 。
(4)与[Co(NH3)6]Cl3类似的产品还有[Co(NH3)5Cl]Cl2,请简述验证某晶体是[Co(NH3)6]Cl3还是[Co(NH3)5•Cl]Cl2的实验方案___ 。
(5)步骤Ⅲ中趁热过滤的主要目的是___ ,滤液中加适量浓盐酸的主要目的是___ 。
(6)乙醇洗涤与蒸馏水洗涤相比优点是___ 。

Ⅰ.称取研细的CoCl2•6H2O10.0g和NH4Cl5.0g于烧杯中溶解,将溶液转入三颈烧瓶,加入25mL浓氨水和适量活性炭粉末,逐滴加入5mL30%的H2O2溶液。
Ⅱ.用水浴将混合物加热至60℃,恒温20分钟,然后用冰水浴冷却,充分结晶后过滤。
Ⅲ.将沉淀溶于热的盐酸中,趁热过滤,滤液中加适量浓盐酸并冷却结晶。
Ⅳ.过滤、用乙醇洗涤晶体并在105℃条件下烘干。
试回答下列问题:
(1)制备[Co(NH3)6]Cl3的化学方程式是
(2)请指出装置中存在的一处缺陷
(3)若将5mL30%的H2O2溶液一次性加入三颈烧瓶,会出现的问题是
(4)与[Co(NH3)6]Cl3类似的产品还有[Co(NH3)5Cl]Cl2,请简述验证某晶体是[Co(NH3)6]Cl3还是[Co(NH3)5•Cl]Cl2的实验方案
(5)步骤Ⅲ中趁热过滤的主要目的是
(6)乙醇洗涤与蒸馏水洗涤相比优点是
21-22高三上·天津·期末 查看更多[1]
(已下线)天津市和平区2021届高三上学期期末考试化学试题
更新时间:2021-01-23 15:45:56
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】碳酸钠俗称纯碱,用途非常广泛,我国化学家侯德榜发明了“侯氏制碱法”。某化学兴趣小组在实验室中模拟侯氏制碱法制备 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如图所示。
,实验流程如图所示。
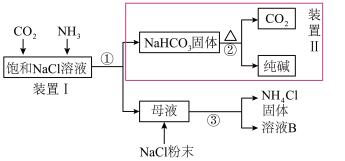
(1)①②③所涉及的操作方法中,包含过滤的是______ (填序号)。
(2)上述实验流程中可循环利用的物质是______ (填化学式)。
(3)向母液中加入NaCl粉末,存在 。为使
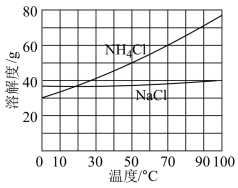
。为使 沉淀充分析出并分离,根据图中NaCl和
沉淀充分析出并分离,根据图中NaCl和 溶解度曲线,需采用的操作为
溶解度曲线,需采用的操作为______ 、______ 过滤、洗涤、干燥。
(4)检验用该纯碱配制的溶液中含有 的方法是
的方法是______ 。
 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如图所示。
,实验流程如图所示。

(1)①②③所涉及的操作方法中,包含过滤的是
(2)上述实验流程中可循环利用的物质是
(3)向母液中加入NaCl粉末,存在
 。为使
。为使 沉淀充分析出并分离,根据图中NaCl和
沉淀充分析出并分离,根据图中NaCl和 溶解度曲线,需采用的操作为
溶解度曲线,需采用的操作为(4)检验用该纯碱配制的溶液中含有
 的方法是
的方法是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】宏观辨识与微观探析是化学学科重要的学科素养。回答下列问题:
Ⅰ.已知某无色水样中只含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 的若干种。某化学研究性学习小组对该水样的成分进行检检验:
的若干种。某化学研究性学习小组对该水样的成分进行检检验:
①取部分水样;
②向水样中滴加足量硝酸钡溶液,产生白色沉淀;
③向步骤②所得沉淀中滴加足量稀盐酸,沉淀部分溶解;
④向步骤③所得溶液中滴加硝酸银溶液,又产生白色沉淀。
(1)该水样中一定存在的离子是
(2)若要确定可能存在的离子是否存在,还需进行的实验操作是
Ⅱ.现有 、
、 、NaCl、
、NaCl、 四种溶液,该小组同学设计如下实验步骤进行鉴别:
四种溶液,该小组同学设计如下实验步骤进行鉴别:
①取等体积的上述四种溶液A、B、C、D分别置于四支试管中,对四支试管均进行下列操作:加入过量的NaOH溶液、加热,将湿润的红色石蕊试纸靠近试管口。观察到盛装B、D溶液的试管口的试纸变蓝。
②向①中反应后的四支试管中,分别依次加入足量 溶液,观察到盛装B、C溶液的试管内产生白色沉淀。
溶液,观察到盛装B、C溶液的试管内产生白色沉淀。
(3)溶液A、B、C、D中的溶质依次为
(4)溶液B与NaOH溶液共热时发生反应的离子方程式为
(5)有同学提出用一种试剂即可将四种溶液鉴别出来,该试剂为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)下列各组物质中互为同素异形体的是:___________
A.CO、CO2 B.金刚石和石墨 C.冰、干冰 D.液氧、氧气 E.红磷、白磷
(2)写出下列反应方程式:
①写出NH4HCO3的电离方程式:___________ 。
②胃舒平[主要成分AlOH3]中和胃酸(盐酸)的离子反应方程式:___________ 。
③盐酸除铁锈的离子反应方程式:___________ 。
(3)对一份稀溶液作初步分析后发现,溶液无色、澄清,其中可能含有SO 、Na、CO
、Na、CO 、H、NO
、H、NO 、HCO
、HCO 、Cl中的若干种。然后又作了如下分析,以确定这些离子是否存在。
、Cl中的若干种。然后又作了如下分析,以确定这些离子是否存在。
①用石蕊试液检测该溶液时,溶液显红色。
②取2mL该溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。请回答下列问题:
原溶液中一定存在的离子是___________ ,一定不存在的离子是___________ 。按上述实验操作,不能确定原溶液中有Cl,请说明原因:___________ 。
(1)下列各组物质中互为同素异形体的是:
A.CO、CO2 B.金刚石和石墨 C.冰、干冰 D.液氧、氧气 E.红磷、白磷
(2)写出下列反应方程式:
①写出NH4HCO3的电离方程式:
②胃舒平[主要成分AlOH3]中和胃酸(盐酸)的离子反应方程式:
③盐酸除铁锈的离子反应方程式:
(3)对一份稀溶液作初步分析后发现,溶液无色、澄清,其中可能含有SO
 、Na、CO
、Na、CO 、H、NO
、H、NO 、HCO
、HCO 、Cl中的若干种。然后又作了如下分析,以确定这些离子是否存在。
、Cl中的若干种。然后又作了如下分析,以确定这些离子是否存在。①用石蕊试液检测该溶液时,溶液显红色。
②取2mL该溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。请回答下列问题:
原溶液中一定存在的离子是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】钴及其化合物有重要的用途,研究其结构有重要意义。
(1)基态Co的价层电子排布式是3d74s2,轨道表示式是 。
。____ 在元素周期表中,该元素属于____ (填“d”或“ds”)区。
(2)[Co(NH3)5Cl]Cl2是Co3+的一种重要配合物。
①该配合物的一种配体是NH3。NH3的空间结构呈____ 形,是_____ (填“极性”或“非极性”)分子。
②该配合物中Co3+参与杂化的6个能量相近的空轨道分别是2个3d、1个_____ 和3个____ 。
③设计实验证实该配合物溶于水时,离子键发生断裂,配位键没有断裂。
实验如下:称取2.51g该配合物,先加水溶解,再加足量AgNO3溶液,____ (补全实验操作和数据)。
相对分子质量:[Co(NH3)5Cl]Cl2-250.5,AgCl-143.5。
(3)钴蓝可用于青花瓷的颜料。钴蓝晶体是由图1所示的结构平移构成。图1包含Ⅰ型和Ⅱ型两种小立方体。图2是钴蓝的晶胞。
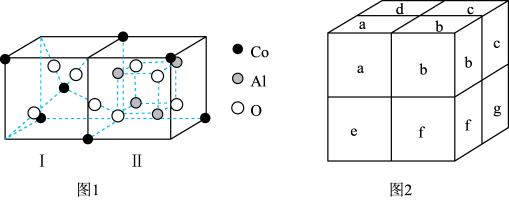
①图2中Ⅱ型小立方体分别是b、____ (填字母序号)。
②钴蓝晶体中三种原子个数比N(Co):N(Al):N(O)=____ 。
(1)基态Co的价层电子排布式是3d74s2,轨道表示式是
 。
。(2)[Co(NH3)5Cl]Cl2是Co3+的一种重要配合物。
①该配合物的一种配体是NH3。NH3的空间结构呈
②该配合物中Co3+参与杂化的6个能量相近的空轨道分别是2个3d、1个
③设计实验证实该配合物溶于水时,离子键发生断裂,配位键没有断裂。
实验如下:称取2.51g该配合物,先加水溶解,再加足量AgNO3溶液,
相对分子质量:[Co(NH3)5Cl]Cl2-250.5,AgCl-143.5。
(3)钴蓝可用于青花瓷的颜料。钴蓝晶体是由图1所示的结构平移构成。图1包含Ⅰ型和Ⅱ型两种小立方体。图2是钴蓝的晶胞。

①图2中Ⅱ型小立方体分别是b、
②钴蓝晶体中三种原子个数比N(Co):N(Al):N(O)=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】(1)氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如表中所示:
试从结构的角度分析它们熔点不同的原因___________________________________ 。
(2)N、P、As位于同一主族,基态氮原子的核外共有________ 种不同运动状态的电子,与PO43-互为等电子体的分子有________________ (填一种即可)。
(3)铬原子的最高能层符号是_______ ,其价电子轨道表示式为____________________ 。
(4)比较第二电离能Cu_______ Zn(填“>”、“=”、“<")。
(5)AuCl3是一种褐红色晶体,吸湿性极强,易溶于水和乙醇,无论是固态、还是气态,它都是以二聚体Au2Cl6的形式存在。写出Au2Cl6的结构式__________________________ .
(6)已知Zn2+、Au+均能与CN-形成配离子, Zn2+与CN-形成的配离子为正四面体形,Au+与CN-形成的配离子为直线形. 工业上常用Au+和CN-形成的配离子与Zn单质反应来提取Au单质,写出该反应的离子方程式___________________________________________________________________________________ 。
物质 | BN | AIN | GaN |
熔点/℃ | 3000 | 2200 | 1700 |
试从结构的角度分析它们熔点不同的原因
(2)N、P、As位于同一主族,基态氮原子的核外共有
(3)铬原子的最高能层符号是
(4)比较第二电离能Cu
(5)AuCl3是一种褐红色晶体,吸湿性极强,易溶于水和乙醇,无论是固态、还是气态,它都是以二聚体Au2Cl6的形式存在。写出Au2Cl6的结构式
(6)已知Zn2+、Au+均能与CN-形成配离子, Zn2+与CN-形成的配离子为正四面体形,Au+与CN-形成的配离子为直线形. 工业上常用Au+和CN-形成的配离子与Zn单质反应来提取Au单质,写出该反应的离子方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】铱( )属于铂系金属,铂系金属包括钌(
)属于铂系金属,铂系金属包括钌( )、锇(
)、锇( )、铑(
)、铑( )、铱(
)、铱( )、钯(
)、钯( )、铂(
)、铂( )六种金属。其中铑、铱、钯、铂在周期表中的相对位置如图所示。
)六种金属。其中铑、铱、钯、铂在周期表中的相对位置如图所示。
回答下列问题:
(1)基态铱原子的价层电子排布式为_____ 。
(2)实验室常用氯化钯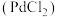 溶液检验
溶液检验 ,发生反应为
,发生反应为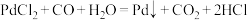 。
。
①在标准状况下,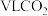 含
含 键数目为
键数目为_____ ( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
② 分子中
分子中 键类型是
键类型是_____ (填字母)。
A. B.
B. C.
C. D.
D.
(3)实验证明,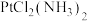 的结构有两种:
的结构有两种: 呈棕黄色,有极性,有抗癌活性,在水中的溶解度为
呈棕黄色,有极性,有抗癌活性,在水中的溶解度为 ,水解后能与草酸
,水解后能与草酸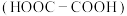 反应生成
反应生成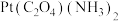 ;B呈淡黄色,无极性,无抗癌活性,在水中的溶解度为
;B呈淡黄色,无极性,无抗癌活性,在水中的溶解度为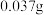 ,水解后不能与草酸反应。
,水解后不能与草酸反应。
①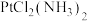 的空间构型是
的空间构型是_____ (填“四面体形”或“平面四边形”)。
②画出A的结构图示:_____ 。
③ 中碳原子的杂化类型是
中碳原子的杂化类型是_____ ,提供孤电子对的原子是_____ (填元素符号)。
 )属于铂系金属,铂系金属包括钌(
)属于铂系金属,铂系金属包括钌( )、锇(
)、锇( )、铑(
)、铑( )、铱(
)、铱( )、钯(
)、钯( )、铂(
)、铂( )六种金属。其中铑、铱、钯、铂在周期表中的相对位置如图所示。
)六种金属。其中铑、铱、钯、铂在周期表中的相对位置如图所示。 |  |
 |  |
 |  |
(1)基态铱原子的价层电子排布式为
(2)实验室常用氯化钯
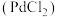 溶液检验
溶液检验 ,发生反应为
,发生反应为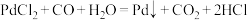 。
。①在标准状况下,
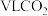 含
含 键数目为
键数目为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。②
 分子中
分子中 键类型是
键类型是A.
 B.
B. C.
C. D.
D.
(3)实验证明,
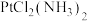 的结构有两种:
的结构有两种: 呈棕黄色,有极性,有抗癌活性,在水中的溶解度为
呈棕黄色,有极性,有抗癌活性,在水中的溶解度为 ,水解后能与草酸
,水解后能与草酸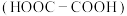 反应生成
反应生成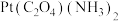 ;B呈淡黄色,无极性,无抗癌活性,在水中的溶解度为
;B呈淡黄色,无极性,无抗癌活性,在水中的溶解度为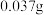 ,水解后不能与草酸反应。
,水解后不能与草酸反应。①
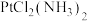 的空间构型是
的空间构型是②画出A的结构图示:
③
 中碳原子的杂化类型是
中碳原子的杂化类型是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】1000 mL某无色待测液中除含有0.2 mol·L-1的Na+外,还可能含有下列离子中的一种或多种:
查阅资料发现,Br2在常温下是深红棕色液体,微溶于水,其水溶液为橙黄色。类比用淀粉-KI试纸检验Cl2的原理,Cl2也可以与Br-发生类似的反应得到Br2;现进行如下实验操作(每次实验所加试剂均过量):
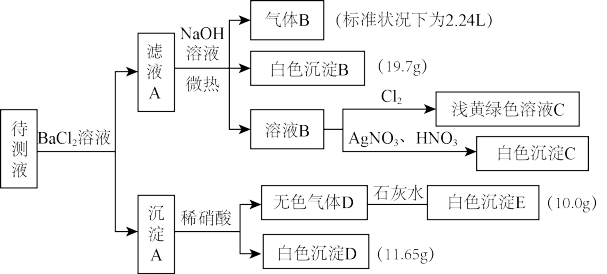
(1)写出生成白色沉淀B的离子方程式:_______ 。
(2)待测液中肯定不存在的阳离子是_______ 。
(3)待测液中一定含有的阴离子是_______ ,可能含有的阴离子是_______ 。
(4)判断原溶液中K+是否存在,_______ (填“是”或“否”),若存在,求K+物质的量浓度的最小值,若不存在,请说明理由_______ 。
(5)将滤液A和沉淀A分开的操作是过滤和洗涤。洗涤的操作是_______ 。
| 阳离子 | K+、NH 、Fe3+、Ba2+ 、Fe3+、Ba2+ |
| 阴离子 | Cl-、Br-、CO 、HCO 、HCO 、SO 、SO |

(1)写出生成白色沉淀B的离子方程式:
(2)待测液中肯定不存在的阳离子是
(3)待测液中一定含有的阴离子是
(4)判断原溶液中K+是否存在,
(5)将滤液A和沉淀A分开的操作是过滤和洗涤。洗涤的操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】选择装置,完成实验。

(1)用饱和食盐水除去氯气中的氯化氢,应选用______ (填序号,下同)。
(2)除去食盐水中的泥沙,应选用______ 。
(3)用自来水制取蒸馏水,应选用______ 。
(4)用四氯化碳提取碘水中的碘,应选用______ 。

(1)用饱和食盐水除去氯气中的氯化氢,应选用
(2)除去食盐水中的泥沙,应选用
(3)用自来水制取蒸馏水,应选用
(4)用四氯化碳提取碘水中的碘,应选用
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】以工业废渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下:

(1)氯化过程中控制废渣过量、在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。
①若某学生在上述流程中发现某含钙离子盐的化学式为CaO3Cl2,试根据盐的定义写出这种盐组成的表达式_______ 。
②刚开始生成Ca(ClO)2的化学方程式为_______ 。
③提高Cl2转化为Ca(ClO)2的转化率的可行措施有_______ (填序号)。
a.适当减缓通入Cl2的速率 b.充分搅拌浆料 c.加水使Ca(OH)2完全溶解
(2)氯化完成后过滤。
①滤渣的主要成分为_______ (填化学式)。
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2]与n[CaCl2]_______ 1∶5(填“>”“<”或“=”)。
(3)向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3。你认为可能的原因是_______ 。写出可能发生的化学方程式_______ 。
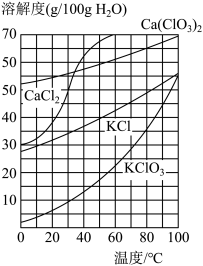

(1)氯化过程中控制废渣过量、在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。
①若某学生在上述流程中发现某含钙离子盐的化学式为CaO3Cl2,试根据盐的定义写出这种盐组成的表达式
②刚开始生成Ca(ClO)2的化学方程式为
③提高Cl2转化为Ca(ClO)2的转化率的可行措施有
a.适当减缓通入Cl2的速率 b.充分搅拌浆料 c.加水使Ca(OH)2完全溶解
(2)氯化完成后过滤。
①滤渣的主要成分为
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2]与n[CaCl2]
(3)向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3。你认为可能的原因是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】硫酸镍晶体(NiSO4•7H2O)可用于电镀工业,可用含镍废催化剂为原料来制备。已知某化工厂的含镍废催化剂主要含有Ni,还含有Al、Fe的单质及其他不溶杂质(不溶于酸碱)。某小组通过查阅资料,设计了如下图所示的制备流程:
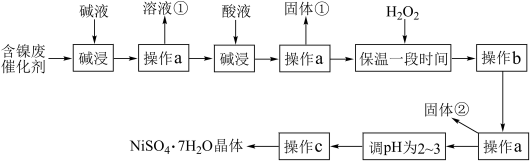
已知: Ksp[Fe(OH)3]=4.0×10-38 ,Ksp[Ni(OH)2]=1.2×10-15
(1)“碱浸”过程中发生反应的离子方程式是_______________________________ 。
(2)操作a所用到的玻璃仪器有烧杯、________ 、________ ;操作c的名称为____________ 、____________ 、过滤、洗涤。
(3)固体①是______________ ;加H2O2的目的是(用离子方程式表示)_____________ 。
(4)调pH为2-3时所加的酸是________ 。
(5)操作b为调节溶液的pH,若经过操作b后溶液中c(Ni2+)=2mol·L-1,当铁离子恰好完全沉淀溶液中c(Fe3+)=1.0×10-5mol·L-1时,溶液中是否有Ni(OH)2沉淀生成?________ (填“是”或“否”)。
(6)NiSO4•7H2O可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在放电过程中总反应的化学方程式是NiOOH+MH=Ni(OH)2+M,则NiMH电池充电过程中,阳极的电极反应式为_______ 。

已知: Ksp[Fe(OH)3]=4.0×10-38 ,Ksp[Ni(OH)2]=1.2×10-15
(1)“碱浸”过程中发生反应的离子方程式是
(2)操作a所用到的玻璃仪器有烧杯、
(3)固体①是
(4)调pH为2-3时所加的酸是
(5)操作b为调节溶液的pH,若经过操作b后溶液中c(Ni2+)=2mol·L-1,当铁离子恰好完全沉淀溶液中c(Fe3+)=1.0×10-5mol·L-1时,溶液中是否有Ni(OH)2沉淀生成?
(6)NiSO4•7H2O可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在放电过程中总反应的化学方程式是NiOOH+MH=Ni(OH)2+M,则NiMH电池充电过程中,阳极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】从废钼催化剂(主要成分为MoO3、MoS2,含少量NiS、NiO、Fe2O3等)中回收利用金属的一种工艺流程如图所示。

已知:①“沉钼”前钼元素主要以MoO 形式存在;
形式存在;
②该条件下Ksp(NiCO3)=1.5×10-7。
(1)“焙烧”生成的气体主要成分为_______ (填化学式)。
(2)“沉钼”的离子方程式为_______ 。
(3)“酸浸”时,控制硫酸浓度,加料完成后,在一定的温度下发生反应。提高镍元素浸出率的方法还有_______ 。
(4)“除铁”后所得滤液中c(Ni2+)=1.0mol·L-1,“沉镍”后所得滤液中c( )=1.0×10-5mol·L-1,则沉镍率=
)=1.0×10-5mol·L-1,则沉镍率=_______ [沉镍率= ×100%,计算过程中不考虑溶液体积变化]。
×100%,计算过程中不考虑溶液体积变化]。
(5)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
从NiSO4溶液获得稳定的NiSO4•6H2O晶体的操作是:_______ 、洗涤、干燥等。
(6)硫酸镍晶体溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中的阳离子具有正八面体结构,该配离子的结构可表示为_______ 。

已知:①“沉钼”前钼元素主要以MoO
 形式存在;
形式存在;②该条件下Ksp(NiCO3)=1.5×10-7。
(1)“焙烧”生成的气体主要成分为
(2)“沉钼”的离子方程式为
(3)“酸浸”时,控制硫酸浓度,加料完成后,在一定的温度下发生反应。提高镍元素浸出率的方法还有
(4)“除铁”后所得滤液中c(Ni2+)=1.0mol·L-1,“沉镍”后所得滤液中c(
 )=1.0×10-5mol·L-1,则沉镍率=
)=1.0×10-5mol·L-1,则沉镍率= ×100%,计算过程中不考虑溶液体积变化]。
×100%,计算过程中不考虑溶液体积变化]。(5)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
| 温度 | 低于30.8℃ | 30.8~53.8℃ | 53.8~280℃ | 高于280℃ |
| 晶体形态 | NiSO4•7H2O | NiSO4•6H2O | 多种结晶水合物 | NiSO4 |
(6)硫酸镍晶体溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中的阳离子具有正八面体结构,该配离子的结构可表示为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】活性ZnO俗称锌1-3,能改逬玻璃的化学稳定性,可用于生产特种玻璃,在橡胶的虫产中能缩短硫化时间,在涂料、油漆等工业也有重要应用。工业上由粗ZnO(含FeO、CuO等.)制备活性ZnO,采取酸浸、净化除杂、中和沉降、干燥煅烧等步骤,工艺流程如下:
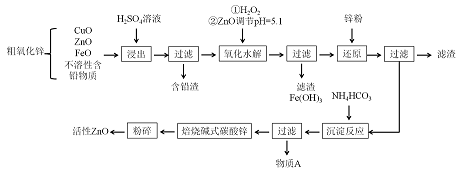
(1)上述流程中,浸出用的是60%H2SO4(1.5g/cm3),这种硫酸的物质的量浓度为________ (保留两位小数)
(2)已知ZnO为两性氧化物,与氢氧化钠溶液反应生成可溶性的锌酸盐(ZnO2-),写出反应的离子方程式________________
(3)写出加H2O2时发生反应的离子方程式________________
(4)除去Fe(OH)3后,在滤液中加入Zn的目的是________
(5)上述流程中多次进行了过滤橾作,请写出过滤时用到的玻璃仪器:________________
(6)物质A是________ ,检验该溶质阴离子的方法是________
(7)取碱式碳酸锌6.82g,溶于盐酸生成CO2448mL(标准状况下),溶解过程消耗HCl 0. 12mol,若该碱式盐中氢元素的质量分数为1.76%,试推测该碱式碳酸锌的化学式________

(1)上述流程中,浸出用的是60%H2SO4(1.5g/cm3),这种硫酸的物质的量浓度为
(2)已知ZnO为两性氧化物,与氢氧化钠溶液反应生成可溶性的锌酸盐(ZnO2-),写出反应的离子方程式
(3)写出加H2O2时发生反应的离子方程式
(4)除去Fe(OH)3后,在滤液中加入Zn的目的是
(5)上述流程中多次进行了过滤橾作,请写出过滤时用到的玻璃仪器:
(6)物质A是
(7)取碱式碳酸锌6.82g,溶于盐酸生成CO2448mL(标准状况下),溶解过程消耗HCl 0. 12mol,若该碱式盐中氢元素的质量分数为1.76%,试推测该碱式碳酸锌的化学式
您最近一年使用:0次



