自热化学链重整制氢 工艺的原理如图所示:
工艺的原理如图所示:
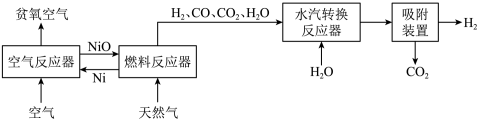
回答下列问题:
(1)25℃、101 时,5.9g
时,5.9g 与足量
与足量 反应生成
反应生成 放出47.2
放出47.2 的热量,则在“空气反应器”中发生反应的热化学方程式为
的热量,则在“空气反应器”中发生反应的热化学方程式为_______ 。
(2)“燃料反应器”中发生的部分反应有:
(Ⅰ)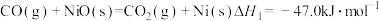
(Ⅱ)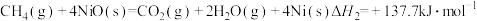
(Ⅲ)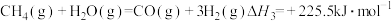
则反应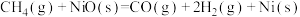 的
的
_______  。
。
(3)“水汽转换反应器”中发生的反应为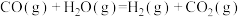 (平衡常数
(平衡常数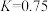 ),将天然气看作是纯净的
),将天然气看作是纯净的 (假定向水汽转换反应器中补充的水的物质的量等于甲烷的物质的量),若在t℃时进行转换,水汽转换反应器中某时刻
(假定向水汽转换反应器中补充的水的物质的量等于甲烷的物质的量),若在t℃时进行转换,水汽转换反应器中某时刻 、
、 、
、 、
、 浓度之比为
浓度之比为 此时
此时
_______ 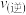 (填“>”、“=”或“<”),理由是
(填“>”、“=”或“<”),理由是_______ 。
(4)甲烷制氢传统工艺有水蒸气重整部分氧化重整以及联合重整等, 工艺重整是一种联合重整,涉及反应的热化学方程式如下:
工艺重整是一种联合重整,涉及反应的热化学方程式如下:
水蒸气重整反应: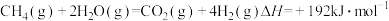
部分氧化重整反应: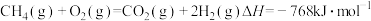
采用水蒸气重整的优点是_______ ;若上述两个反应在保持自热条件下(假设无热量损失),理论上1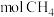 至多可获得
至多可获得 的物质的量为
的物质的量为_______ (结果保留1位小数)。
 工艺的原理如图所示:
工艺的原理如图所示:
回答下列问题:
(1)25℃、101
 时,5.9g
时,5.9g 与足量
与足量 反应生成
反应生成 放出47.2
放出47.2 的热量,则在“空气反应器”中发生反应的热化学方程式为
的热量,则在“空气反应器”中发生反应的热化学方程式为(2)“燃料反应器”中发生的部分反应有:
(Ⅰ)
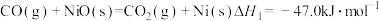
(Ⅱ)
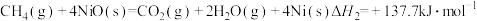
(Ⅲ)
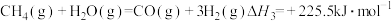
则反应
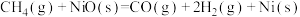 的
的
 。
。(3)“水汽转换反应器”中发生的反应为
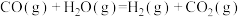 (平衡常数
(平衡常数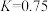 ),将天然气看作是纯净的
),将天然气看作是纯净的 (假定向水汽转换反应器中补充的水的物质的量等于甲烷的物质的量),若在t℃时进行转换,水汽转换反应器中某时刻
(假定向水汽转换反应器中补充的水的物质的量等于甲烷的物质的量),若在t℃时进行转换,水汽转换反应器中某时刻 、
、 、
、 、
、 浓度之比为
浓度之比为 此时
此时
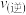 (填“>”、“=”或“<”),理由是
(填“>”、“=”或“<”),理由是(4)甲烷制氢传统工艺有水蒸气重整部分氧化重整以及联合重整等,
 工艺重整是一种联合重整,涉及反应的热化学方程式如下:
工艺重整是一种联合重整,涉及反应的热化学方程式如下:水蒸气重整反应:
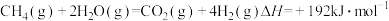
部分氧化重整反应:
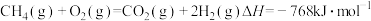
采用水蒸气重整的优点是
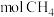 至多可获得
至多可获得 的物质的量为
的物质的量为
更新时间:2021-01-26 10:54:26
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】甲醇氧化为甲醛和水的反应可看作以下两个连续反应:
ⅰ.
ⅱ.H2(g)+ O2(g)=H2O(g) ΔH2=-247.8kJ/mol
O2(g)=H2O(g) ΔH2=-247.8kJ/mol
已知: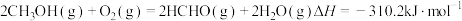
(1)
___________ 。
(2)要提高反应ⅰ中甲醇平衡转化率,可采取的措施有___________ (写出两条)
(3)应用负载银催化时反应ⅰ会发生以下副反应:
ⅲ.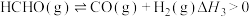
ⅳ.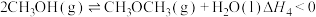
其他条件相同时,以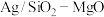 为催化剂,研究银负载量对催化剂活性的影响,实验数据如图所示:
为催化剂,研究银负载量对催化剂活性的影响,实验数据如图所示:

①依据实验数据应选择的最佳反应条件是___________ 。
②温度由650℃至700℃甲醛收率下降的可能原因是___________ 。
(4)通过电催化法可将甲醇转化为甲醛,装置如图所示(电极均为惰性电极)
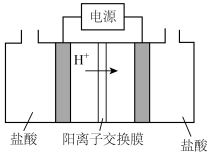
①电极 连接电源的
连接电源的___________ 极(填“正”或“负”)。
②阳极室产生 后发生的反应有:
后发生的反应有:___________ 、
(5)电解后甲醛含量测定方法如下:(溶液中无 、
、 剩余)
剩余)
已知:


若滴定过程中消耗 碘V1L,消耗
碘V1L,消耗 标准
标准 溶液V2L,则电解后甲醛的含量为
溶液V2L,则电解后甲醛的含量为___________  。
。
ⅰ.

ⅱ.H2(g)+
 O2(g)=H2O(g) ΔH2=-247.8kJ/mol
O2(g)=H2O(g) ΔH2=-247.8kJ/mol已知:
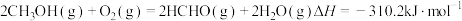
(1)

(2)要提高反应ⅰ中甲醇平衡转化率,可采取的措施有
(3)应用负载银催化时反应ⅰ会发生以下副反应:
ⅲ.
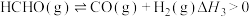
ⅳ.
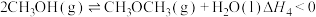
其他条件相同时,以
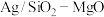 为催化剂,研究银负载量对催化剂活性的影响,实验数据如图所示:
为催化剂,研究银负载量对催化剂活性的影响,实验数据如图所示:
①依据实验数据应选择的最佳反应条件是
②温度由650℃至700℃甲醛收率下降的可能原因是
(4)通过电催化法可将甲醇转化为甲醛,装置如图所示(电极均为惰性电极)

①电极
 连接电源的
连接电源的②阳极室产生
 后发生的反应有:
后发生的反应有:
(5)电解后甲醛含量测定方法如下:(溶液中无
 、
、 剩余)
剩余)已知:



若滴定过程中消耗
 碘V1L,消耗
碘V1L,消耗 标准
标准 溶液V2L,则电解后甲醛的含量为
溶液V2L,则电解后甲醛的含量为 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】我国科学家研发的“液态阳光”计划通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢制备甲醇。
(1)制备甲醇主反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-48.7kJ/mol。
CH3OH(g)+H2O(g)△H=-48.7kJ/mol。
该过程中还存在一个生成CO的副反应,结合反应:CO(g)+2H2(g)=CH3OH(g)△H=-90.0kJ/mol
写出该副反应的热化学方程式:_______ 。
(2)将CO2和H2按物质的量比1:3混合,以固定流速通过盛放Cu/Zn/A/Zr催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。 。
。
①催化剂活性最好的温度为_______ 。
a.483K b.503 K c.1523 K d.543 K
②温度由523K升到543K,CO2的平衡转化率和CH3OH的实验产率均降低,解释原因:_______ 。
(3)使用Cu2O-ZnO薄膜电极作阴极,通过电催化法将二氧化碳转化为甲醇。
①将铜箔放入煮沸的饱和磕酸铜溶液中,制得Cu2O薄膜电极。反应的离子方程式为_______ 。
②用Cu2O薄膜电极作阴极,Zn(NO3)2溶液作电解液,采用电沉积法制备Cu2O-ZnO薄膜电极,制备完成后电解液中检测到了 制备ZnO薄膜的电极反应式为
制备ZnO薄膜的电极反应式为_______ 。
(1)制备甲醇主反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H=-48.7kJ/mol。
CH3OH(g)+H2O(g)△H=-48.7kJ/mol。该过程中还存在一个生成CO的副反应,结合反应:CO(g)+2H2(g)=CH3OH(g)△H=-90.0kJ/mol
写出该副反应的热化学方程式:
(2)将CO2和H2按物质的量比1:3混合,以固定流速通过盛放Cu/Zn/A/Zr催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。

 。
。①催化剂活性最好的温度为
a.483K b.503 K c.1523 K d.543 K
②温度由523K升到543K,CO2的平衡转化率和CH3OH的实验产率均降低,解释原因:
(3)使用Cu2O-ZnO薄膜电极作阴极,通过电催化法将二氧化碳转化为甲醇。
①将铜箔放入煮沸的饱和磕酸铜溶液中,制得Cu2O薄膜电极。反应的离子方程式为
②用Cu2O薄膜电极作阴极,Zn(NO3)2溶液作电解液,采用电沉积法制备Cu2O-ZnO薄膜电极,制备完成后电解液中检测到了
 制备ZnO薄膜的电极反应式为
制备ZnO薄膜的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】处理 、
、 是减少空气污染的重要途径。
是减少空气污染的重要途径。
已知:①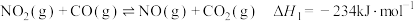
②
③
④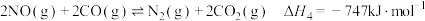
回答下列问题:
(1)
___________  。
。
(2)已知反应①的正反应活化能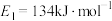 ,则其逆反应活化能
,则其逆反应活化能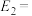
___________  。
。
(3)向密闭反应器中按 投料,发生反应④。相同时间内,不同温度下,测得
投料,发生反应④。相同时间内,不同温度下,测得 的转化率与催化剂Cat1、Cat2的关系如图所示。
的转化率与催化剂Cat1、Cat2的关系如图所示。___________ (填“Cat1”或“Cat2”)。
②Cat1作用下,400℃时b点________ (填“达到”或“未达到”)平衡状态,判断依据是________ 。
③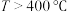 ,b→c的可能原因是
,b→c的可能原因是___________ 。
(4)在甲、乙均为1L的恒容密闭容器中均充入 和
和 ,在恒温和绝热两种条件下仅发生反应④,测得压强变化如图所示。
,在恒温和绝热两种条件下仅发生反应④,测得压强变化如图所示。___________ (填“恒温”或“绝热”)。
②乙容器中0~4min内 的平均速率为
的平均速率为___________ mol∙L-1∙min-1。a点放出的热量为___________ kJ。
③平衡常数:
___________ (填“大于”“小于”或“等于”) 。
。
 、
、 是减少空气污染的重要途径。
是减少空气污染的重要途径。已知:①
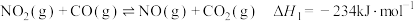
②

③

④
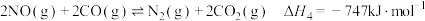
回答下列问题:
(1)

 。
。(2)已知反应①的正反应活化能
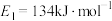 ,则其逆反应活化能
,则其逆反应活化能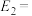
 。
。(3)向密闭反应器中按
 投料,发生反应④。相同时间内,不同温度下,测得
投料,发生反应④。相同时间内,不同温度下,测得 的转化率与催化剂Cat1、Cat2的关系如图所示。
的转化率与催化剂Cat1、Cat2的关系如图所示。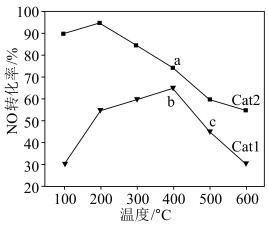
②Cat1作用下,400℃时b点
③
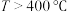 ,b→c的可能原因是
,b→c的可能原因是(4)在甲、乙均为1L的恒容密闭容器中均充入
 和
和 ,在恒温和绝热两种条件下仅发生反应④,测得压强变化如图所示。
,在恒温和绝热两种条件下仅发生反应④,测得压强变化如图所示。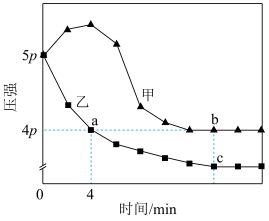
②乙容器中0~4min内
 的平均速率为
的平均速率为③平衡常数:

 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】工业利用甲醇在催化剂作用下制取 涉及的反应如下:
涉及的反应如下:
①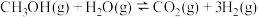

②

请回答下列问题:
(1)CO和H2合成甲醇的热化学方程式为 △H3,则△H3=
△H3,则△H3=_______ 。
(2)向一个装有催化剂的体积不变密闭容器中通入一定量的CO2和H2发生反应②,测得反应速率和温度的关系如图甲所示,BC段反应速率降低的原因可能是_______ 。若该反应在一定温度下达到平衡后,将容器压缩,容器内H2的平衡转化率为 ,测定结果如图乙所示,
,测定结果如图乙所示, 随压强增大,开始不变,一定程度后逐渐增大的原因是
随压强增大,开始不变,一定程度后逐渐增大的原因是_______ 。

(3)向两个体积均为2 L的密闭容器中分别充入1 mol CH3OH(g)和1.3 mol H2O(g)、1 mol CH3OH(g)和1 mol H2O(g),发生上述反应①和②,进行有关实验。已知CH3OH(g)分解率接近100%,平衡时容器中CO的物质的量与温度的关系如图丙。

①容器中充入1 mol CH3OH(g)和1.3 mol H2O(g)的变化曲线为_______ (填“I”或“II”),理由是_______ 。
②温度为 时反应在5 min时达到平衡,计算曲线II中0~5 min内v(CO)=
时反应在5 min时达到平衡,计算曲线II中0~5 min内v(CO)=_______ 。该温度下,反应 的平衡常数K=
的平衡常数K=_______ 。
 涉及的反应如下:
涉及的反应如下:①
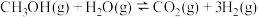

②


请回答下列问题:
(1)CO和H2合成甲醇的热化学方程式为
 △H3,则△H3=
△H3,则△H3=(2)向一个装有催化剂的体积不变密闭容器中通入一定量的CO2和H2发生反应②,测得反应速率和温度的关系如图甲所示,BC段反应速率降低的原因可能是
 ,测定结果如图乙所示,
,测定结果如图乙所示, 随压强增大,开始不变,一定程度后逐渐增大的原因是
随压强增大,开始不变,一定程度后逐渐增大的原因是
(3)向两个体积均为2 L的密闭容器中分别充入1 mol CH3OH(g)和1.3 mol H2O(g)、1 mol CH3OH(g)和1 mol H2O(g),发生上述反应①和②,进行有关实验。已知CH3OH(g)分解率接近100%,平衡时容器中CO的物质的量与温度的关系如图丙。

①容器中充入1 mol CH3OH(g)和1.3 mol H2O(g)的变化曲线为
②温度为
 时反应在5 min时达到平衡,计算曲线II中0~5 min内v(CO)=
时反应在5 min时达到平衡,计算曲线II中0~5 min内v(CO)= 的平衡常数K=
的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、CO、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
Ⅰ.脱硝:已知:H2的燃烧热为285.8 kJ/mol
N2(g) + 2O2(g)= 2NO2(g) △H= +133 kJ/mol
H2O(g) =H2O(l) △H= -44 kJ/mol
(1)催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为_____________ 。
Ⅱ.脱碳:
(2)向2L恒容密闭容器中加入2 mol CO2、6 mol H2,在适当的催化剂作用下,发生反应 CO2(g) + 3H2(g) CH3OH(l) + H2O(l)。下列叙述能说明此反应达到平衡状态的是
CH3OH(l) + H2O(l)。下列叙述能说明此反应达到平衡状态的是__________ 。
A.混合气体的平均式量保持不变 B.CO2和H2的体积分数保持不变
C.CO2和H2的转化率相等 D.混合气体的密度保持不变
E.1 mol CO2生成的同时有3 mol H—H键断裂
(3)在T1℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H2和CO,发生反应CO(g) + 2H2(g) CH3OH(g)反应达到平衡时CH3OH的体积分数(V%)与n(H2)/n(CO)的关系如图所示。
CH3OH(g)反应达到平衡时CH3OH的体积分数(V%)与n(H2)/n(CO)的关系如图所示。

①当起始n(H2)/n(CO)=2,经过5min达到平衡,CO的转化率为0.4,则0~5min内平均反应速率V(H2)=___________ 。若此时再向容器中加入CO(g)和CH3OH(g)各0.4mol,达新平衡时H2的转化率将__________ (选填“增大”、“减小”或“不变”);
②当起始n(H2)/n(CO)=3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的_________ 点(选填“D”、“E”或“F”)
Ⅲ.脱硫:
(4)如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。物质A的化学式为_______ ,阴极的电极反应式是_______________________ 。
Ⅰ.脱硝:已知:H2的燃烧热为285.8 kJ/mol
N2(g) + 2O2(g)= 2NO2(g) △H= +133 kJ/mol
H2O(g) =H2O(l) △H= -44 kJ/mol
(1)催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为
Ⅱ.脱碳:
(2)向2L恒容密闭容器中加入2 mol CO2、6 mol H2,在适当的催化剂作用下,发生反应 CO2(g) + 3H2(g)
 CH3OH(l) + H2O(l)。下列叙述能说明此反应达到平衡状态的是
CH3OH(l) + H2O(l)。下列叙述能说明此反应达到平衡状态的是A.混合气体的平均式量保持不变 B.CO2和H2的体积分数保持不变
C.CO2和H2的转化率相等 D.混合气体的密度保持不变
E.1 mol CO2生成的同时有3 mol H—H键断裂
(3)在T1℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H2和CO,发生反应CO(g) + 2H2(g)
 CH3OH(g)反应达到平衡时CH3OH的体积分数(V%)与n(H2)/n(CO)的关系如图所示。
CH3OH(g)反应达到平衡时CH3OH的体积分数(V%)与n(H2)/n(CO)的关系如图所示。
①当起始n(H2)/n(CO)=2,经过5min达到平衡,CO的转化率为0.4,则0~5min内平均反应速率V(H2)=
②当起始n(H2)/n(CO)=3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的
Ⅲ.脱硫:
(4)如图电解装置可将雾霾中的NO、SO2分别转化为NH4+和SO42-。物质A的化学式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】燃煤火力发电厂会产生大量的NOx、SO2、CO2,排放会对环境造成污染。
(1)通常情况下,当1gC(s)完全燃烧时释放出33kJ热量,该反应的热化学方程式为_______ 。
(2)用活性炭还原处理氮氧化物,有关反应为C(s)+2NO(g) N2(g)+CO2(g)△H。在2L恒容密闭器中加入足量C与NO发生反应,所得数据如下表。
N2(g)+CO2(g)△H。在2L恒容密闭器中加入足量C与NO发生反应,所得数据如下表。
①700℃时,若反应2min达到平衡,0~2min内的CO2平均反应速率v=_______ ;该温度下的平衡常数K=_______ 。
②结合表中数据,判断该反应的△H_______ 0(填“>”或“<”)。
③判断该反应达到平衡的依据是_______ 。
A.容器内气体密度恒定B.容器内各气体浓度恒定
C.容器内压强恒定D.2v正(NO)=v逆(N2)
(3)已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示。由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为_______ 。
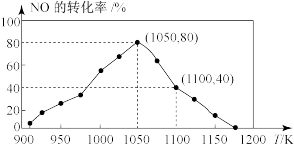
(1)通常情况下,当1gC(s)完全燃烧时释放出33kJ热量,该反应的热化学方程式为
(2)用活性炭还原处理氮氧化物,有关反应为C(s)+2NO(g)
 N2(g)+CO2(g)△H。在2L恒容密闭器中加入足量C与NO发生反应,所得数据如下表。
N2(g)+CO2(g)△H。在2L恒容密闭器中加入足量C与NO发生反应,所得数据如下表。| 实验编号 | 温度/℃ | 起始时NO的物质的量/mol | 平衡时N2的物质的量/mol |
| 1 | 700 | 0.24 | 0.08 |
| 2 | 800 | 0.40 | 0.09 |
②结合表中数据,判断该反应的△H
③判断该反应达到平衡的依据是
A.容器内气体密度恒定B.容器内各气体浓度恒定
C.容器内压强恒定D.2v正(NO)=v逆(N2)
(3)已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示。由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】(1)已知H2S的燃烧热ΔH=-akJ·mol-1,写出表示H2S燃烧反应的热化学方程式__ ,表示H2S燃烧热的热化学方程式__ 。
(2)若将FeCl3溶液蒸干灼烧,最后得到的固体产物主要是__ (填化学式)。FeCl3水溶液呈__ (填“酸”、“中”、“碱”)性,原因为:__ (用离子方程式表示)。
(3)炒过菜的铁锅未及时洗净(残液中有NaCl),第二天便会被腐蚀而出现红褐色铁锈,试回答:铁锅的腐蚀属于电化腐蚀,其原因是__ 。此时铁锅锈蚀主要是吸氧腐蚀,电极反应方程式为:负极:__ ,正极__ 。
(4)估计下列各变化过程是熵增加还是熵减小。(用A、B、C填空)
NH4NO3爆炸:2NH4NO3(s)=2N2(g)+4H2O(g)+O2(g)__
水煤气转化:CO(g)+H2O(g)=CO2(g)+H2(g)__
臭氧的生成:3O2(g)=2O3(g)__
A.熵增大 B.熵减小 C.熵变很小
(2)若将FeCl3溶液蒸干灼烧,最后得到的固体产物主要是
(3)炒过菜的铁锅未及时洗净(残液中有NaCl),第二天便会被腐蚀而出现红褐色铁锈,试回答:铁锅的腐蚀属于电化腐蚀,其原因是
(4)估计下列各变化过程是熵增加还是熵减小。(用A、B、C填空)
NH4NO3爆炸:2NH4NO3(s)=2N2(g)+4H2O(g)+O2(g)
水煤气转化:CO(g)+H2O(g)=CO2(g)+H2(g)
臭氧的生成:3O2(g)=2O3(g)
A.熵增大 B.熵减小 C.熵变很小
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】尿素(NH2CONH2)是目前含氮量最高的氮肥。国内外主要以NH3和CO2为原料进行合成。主要通过以下二个反应进行:
第一步:2NH3(l)+CO2(g) H2NCOONH4(l) △H1=-117.2kJ·mol-1
H2NCOONH4(l) △H1=-117.2kJ·mol-1
第二步:H2NCOONH4(l) H2O(l)+H2NCONH2(l) △H2=+21.7kJ·mol-1
H2O(l)+H2NCONH2(l) △H2=+21.7kJ·mol-1
请回答:
(1)已知:NH3(l) NH3(g) △H3= ckJ·mol-1。火电厂烟气脱硝所使用的还原剂氨气主要来自于尿素水解。则反应NH2CONH2(l)+H2O(l)
NH3(g) △H3= ckJ·mol-1。火电厂烟气脱硝所使用的还原剂氨气主要来自于尿素水解。则反应NH2CONH2(l)+H2O(l) 2NH3(g)+CO2(g)的△H4=
2NH3(g)+CO2(g)的△H4=_________ kJ·mol-1(用含c的式子表示),该反应能在常温下缓慢发生的主要原因是__________________ 。
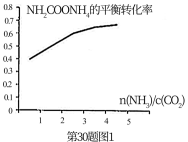
(2)①一定条件下,n(NH3)/n(CO2)对NH2COONH4的平衡转化率会产生明显的影响,如图1所示。NH2COONH4的平衡转化率随n(NH3)/n(CO2)增大而上升,试分析其原因:_______________ 。
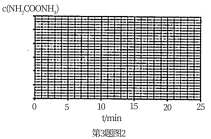
②恒温密闭容器中,一定量的NH3和CO2反应合成尿素,第10 min达到平衡。若相同条件下反应1的速率要快于反应2,请在图中画出0~15min内,NH2COONH4的物质的量浓度随时间变化曲线____________ 。
③下图表示不同条件下,反应:N2(g) +3H2(g) 2NH3(g)的产物浓度随时间的变化曲线。
2NH3(g)的产物浓度随时间的变化曲线。

下列有关说法中,正确的是____________ 。
A.达到平衡时间最快的是II
B.反应约10分钟后,三个反应均已达到平衡
C.I条件下氢气的平衡转化率大于Ⅱ
D.三个反应的平衡常数一定相同
(3)用电化学方法可以实现低温常压合成氨。下图是以含N3-熔融盐为电解质,电解合成氨装置的工作原理示意图。阴极的电极反应是_______________________ 。

第一步:2NH3(l)+CO2(g)
 H2NCOONH4(l) △H1=-117.2kJ·mol-1
H2NCOONH4(l) △H1=-117.2kJ·mol-1第二步:H2NCOONH4(l)
 H2O(l)+H2NCONH2(l) △H2=+21.7kJ·mol-1
H2O(l)+H2NCONH2(l) △H2=+21.7kJ·mol-1请回答:
(1)已知:NH3(l)
 NH3(g) △H3= ckJ·mol-1。火电厂烟气脱硝所使用的还原剂氨气主要来自于尿素水解。则反应NH2CONH2(l)+H2O(l)
NH3(g) △H3= ckJ·mol-1。火电厂烟气脱硝所使用的还原剂氨气主要来自于尿素水解。则反应NH2CONH2(l)+H2O(l) 2NH3(g)+CO2(g)的△H4=
2NH3(g)+CO2(g)的△H4=(2)①一定条件下,n(NH3)/n(CO2)对NH2COONH4的平衡转化率会产生明显的影响,如图1所示。NH2COONH4的平衡转化率随n(NH3)/n(CO2)增大而上升,试分析其原因:

②恒温密闭容器中,一定量的NH3和CO2反应合成尿素,第10 min达到平衡。若相同条件下反应1的速率要快于反应2,请在图中画出0~15min内,NH2COONH4的物质的量浓度随时间变化曲线

③下图表示不同条件下,反应:N2(g) +3H2(g)
 2NH3(g)的产物浓度随时间的变化曲线。
2NH3(g)的产物浓度随时间的变化曲线。
下列有关说法中,正确的是
A.达到平衡时间最快的是II
B.反应约10分钟后,三个反应均已达到平衡
C.I条件下氢气的平衡转化率大于Ⅱ
D.三个反应的平衡常数一定相同
(3)用电化学方法可以实现低温常压合成氨。下图是以含N3-熔融盐为电解质,电解合成氨装置的工作原理示意图。阴极的电极反应是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氮及其化合物是科学家们一直在探究的问题,它们在工农业生产和生命活动中起着重要的作用。回答下列问题:
(1)N2和H2合成氨的化学方程式:________ ,该反应的
_______ 0(填“大于”、“小于”或“等于”)。
(2)氮循环是指氮在自然界中的循环转化过程,是生物圈内基本的物质循环之一,存在较多蓝、绿藻类的酸性水体中存在如下图所示的氮循环,请回答相关问题:
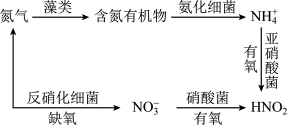
① 在亚硝酸菌作用下的硝化过程的离子方程式是
在亚硝酸菌作用下的硝化过程的离子方程式是___________ 。
②恒温时在亚硝酸菌的作用下发生该反应,能说明体系达到平衡状态的是___________ (填标号)。
A.溶液的pH不再改变
B. 的消耗速率和
的消耗速率和 的生成速率相等
的生成速率相等
C.溶液中 、
、 、
、 、
、 的总物质的量保持不变
的总物质的量保持不变
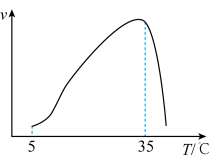
③实验测得在其它条件一定时, 硝化反应的速率随温度变化曲线如下图所示,温度高于35℃时反应速率迅速下降的原因可能是
硝化反应的速率随温度变化曲线如下图所示,温度高于35℃时反应速率迅速下降的原因可能是___________ 。
(3)硝酸工业的尾气成分主要是 ,通常利用
,通常利用 处理,将其转化为无毒物质后排放,该反应的化学方程式为
处理,将其转化为无毒物质后排放,该反应的化学方程式为___________ 。
(1)N2和H2合成氨的化学方程式:

(2)氮循环是指氮在自然界中的循环转化过程,是生物圈内基本的物质循环之一,存在较多蓝、绿藻类的酸性水体中存在如下图所示的氮循环,请回答相关问题:

①
 在亚硝酸菌作用下的硝化过程的离子方程式是
在亚硝酸菌作用下的硝化过程的离子方程式是②恒温时在亚硝酸菌的作用下发生该反应,能说明体系达到平衡状态的是
A.溶液的pH不再改变
B.
 的消耗速率和
的消耗速率和 的生成速率相等
的生成速率相等C.溶液中
 、
、 、
、 、
、 的总物质的量保持不变
的总物质的量保持不变③实验测得在其它条件一定时,
 硝化反应的速率随温度变化曲线如下图所示,温度高于35℃时反应速率迅速下降的原因可能是
硝化反应的速率随温度变化曲线如下图所示,温度高于35℃时反应速率迅速下降的原因可能是
(3)硝酸工业的尾气成分主要是
 ,通常利用
,通常利用 处理,将其转化为无毒物质后排放,该反应的化学方程式为
处理,将其转化为无毒物质后排放,该反应的化学方程式为
您最近一年使用:0次



