认识含硫物质的性质及转化规律,能帮助我们更好地认识自然和保护环境。
(1)酸雨的形成原因。将SO2气体通入蒸馏水中,取出部分溶液并用pH计测定其pH,每隔10min读数一次,所得数据如下:
随着时间的推移,pH逐渐变小的原因是___________ (用化学方程式表示)。
(2)防治SO2对环境的污染。
①从物质分类角度看,SO2属于酸性氧化物。工业上常用熟石灰将SO2转化为亚硫酸盐,写出所得亚硫酸盐的化学式:___________ 。
②从元素价态看,SO2中S元素为+4价,既具有氧化性,又具有还原性。用生物质热解气(主要成分为CO、CH4、H2)可将SO2在高温下还原成单质硫。写出CO还原SO2反应的化学方程式:___________ 。
(3)获取空气质量信息。某化学小组为了测定空气中SO2的体积分数,做了如下实验:取标准状况下的空气20.00L(含N2、O2、CO2、SO2),缓慢通过足量溴水,反应的化学方程式为: 。在所得溶液中加入稍过量的BaCl2溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为4.66g。
。在所得溶液中加入稍过量的BaCl2溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为4.66g。
①检验沉淀是否洗涤干净的方法是___________ 。
②空气样品中SO2的体积分数为___________ 。
(1)酸雨的形成原因。将SO2气体通入蒸馏水中,取出部分溶液并用pH计测定其pH,每隔10min读数一次,所得数据如下:
| 时间(min) | 0 | 10 | 20 | 30 | 40 |
| pH | 4.95 | 4.94 | 4.86 | 4.85 | 4.85 |
随着时间的推移,pH逐渐变小的原因是
(2)防治SO2对环境的污染。
①从物质分类角度看,SO2属于酸性氧化物。工业上常用熟石灰将SO2转化为亚硫酸盐,写出所得亚硫酸盐的化学式:
②从元素价态看,SO2中S元素为+4价,既具有氧化性,又具有还原性。用生物质热解气(主要成分为CO、CH4、H2)可将SO2在高温下还原成单质硫。写出CO还原SO2反应的化学方程式:
(3)获取空气质量信息。某化学小组为了测定空气中SO2的体积分数,做了如下实验:取标准状况下的空气20.00L(含N2、O2、CO2、SO2),缓慢通过足量溴水,反应的化学方程式为:
 。在所得溶液中加入稍过量的BaCl2溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为4.66g。
。在所得溶液中加入稍过量的BaCl2溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为4.66g。①检验沉淀是否洗涤干净的方法是
②空气样品中SO2的体积分数为
20-21高一上·江苏连云港·期末 查看更多[3]
广东省深圳市光明区2022-2023学年高一下学期开学考试化学试题(已下线)专题06 非金属及其化合物-备战2021届高考化学二轮复习题型专练江苏省连云港市2020-2021学年高一上学期期末调研考试化学试题
更新时间:2021-01-27 10:23:09
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】在化学课上围绕浓硫酸的化学性质进行如下实验探究,将适量的蔗糖放入烧杯中,加几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质。请回答下列问题:
(1)生成的这种黑色物质(单质)是(填化学式)____________________ 。
(2)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的污染物之一,这种刺激性气味气体为(填化学式)_________ ,反应的化学方程式为________ 。
(3)根据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有(填字母)_______ 。
A.酸性 B.吸水性
C.脱水性 D.强氧化性
(4)将(2)中产生的有刺激性气味的气体通入品红溶液中,可以看到品红溶液_______ ,说明这种气体有______ 性;将(2)中产生的有刺激性气味的气体通入氯水中,发生反应的化学方程式为_______ 。
(5)能否用澄清石灰水鉴别(2)中产生的两种气体 (填“能”或“不能”)________ ,若不能,请写出两种可以鉴别这两种气体的试剂:________________ 。
(1)生成的这种黑色物质(单质)是(填化学式)
(2)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的污染物之一,这种刺激性气味气体为(填化学式)
(3)根据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有(填字母)
A.酸性 B.吸水性
C.脱水性 D.强氧化性
(4)将(2)中产生的有刺激性气味的气体通入品红溶液中,可以看到品红溶液
(5)能否用澄清石灰水鉴别(2)中产生的两种气体 (填“能”或“不能”)
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】
 和
和 会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列方法中的问题。
会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列方法中的问题。
 的除去(双碱法):用
的除去(双碱法):用 吸收
吸收 ,并用
,并用 使
使 再生,
再生, 溶液
溶液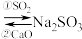 溶液,写出过程①的离子方程式:
溶液,写出过程①的离子方程式:___________________ 。
 和
和 会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列方法中的问题。
会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列方法中的问题。 的除去(双碱法):用
的除去(双碱法):用 吸收
吸收 ,并用
,并用 使
使 再生,
再生, 溶液
溶液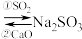 溶液,写出过程①的离子方程式:
溶液,写出过程①的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】下图为硫及其化合物的“价-类”二维图。
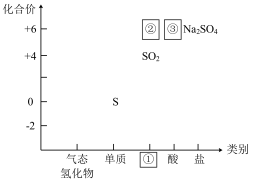
(1)填写二维图缺失的类别①_______ 和化学式②_______ 和化学式③_______ 。
(2)写出Na2SO4的电离方程式_______ 。
(3)写出两个生成Na2SO4的化学方程式(以含钠元素的不同类别物质 为原料)。
①_______ 。
②_______ 。
(4)预测SO2可能发生的反应(不考虑氧化还原反应),填写表格。

(1)填写二维图缺失的类别①
(2)写出Na2SO4的电离方程式
(3)写出两个生成Na2SO4的化学方程式(以
①
②
(4)预测SO2可能发生的反应(不考虑氧化还原反应),填写表格。
| 分析类别 | 反应规律 | 可能的化学方程式 |
| SO2属于 | 可与水反应生成相应的酸 | |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】分类法在化学学习中应用广泛。
(1)为了保护环境,应减少SO2在大气中的排放。SO2属于酸性氧化物,可与NaOH、___ (填与NaOH不同类别的一种具体物质)等反应。写出SO2与NaOH反应的化学方程式___ 。
(2)氯化铁(FeCl3)可用于金属蚀刻、污水处理等,是重要的化工原料。写出两个生成FeCl3的化学方程式(以含铁元素的不同类别物质 为原料)。
①___ 。
②___ 。
(1)为了保护环境,应减少SO2在大气中的排放。SO2属于酸性氧化物,可与NaOH、
(2)氯化铁(FeCl3)可用于金属蚀刻、污水处理等,是重要的化工原料。写出两个生成FeCl3的化学方程式(以含铁元素的
①
②
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在煤中加入适量生石灰,可以大大减少煤燃烧时SO2的排放,请你写出涉及反应的化学方程式_______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】W、X、Y、Z、M、G五种短周期元素,原子序数依次增大。W、Z同主族,可形成离子化合物ZW;Y 、M同主族,可形成MY2、 MY3两种分子;X的气态氢化物水溶液呈碱性。
请回答下列问题:
(1)Y在元素周期表中的位置为__________ ;
(2)上述五种元素的最高价氧化物对应的水化物酸性最强的是__________ (写化学式)
(3)W、Y、Z、G形成的简单离子的半径大小顺序是__________ (用化学符号表示)
(4)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有__________ (任写两个)
(5)Y与M的氢化物中,热稳定性差的是________ (填化学式),沸点高的是________ (填化学式)
(6)ZW的电子式为__________ ,W2Y2的电子式为_____ ,用电子式表示Z2M的形成过程:______ 。
(7)MY2和G2均能使品红溶液褪色,常温常压下若将相同体积的MY2和G2气体同时通入品红溶液,品红溶液__________ (填“褪色”或“不褪色”),请用相关离子方程式解释原因_______ 。
(8)已知
工业制镁时,电解MgCl2而不电解MgO的原因是是__________ ;制铝时,电解Al2O3而不电解AlCl3的原因是__________ 。
(9)最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如下图所示,已知断裂1 mol N—N吸收167 kJ热量,生成1 mol N≡N放出942kJ。根据以上信息和数据,下列说法正确的是__________ 。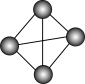
请回答下列问题:
(1)Y在元素周期表中的位置为
(2)上述五种元素的最高价氧化物对应的水化物酸性最强的是
(3)W、Y、Z、G形成的简单离子的半径大小顺序是
(4)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有
(5)Y与M的氢化物中,热稳定性差的是
(6)ZW的电子式为
(7)MY2和G2均能使品红溶液褪色,常温常压下若将相同体积的MY2和G2气体同时通入品红溶液,品红溶液
(8)已知
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
(9)最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如下图所示,已知断裂1 mol N—N吸收167 kJ热量,生成1 mol N≡N放出942kJ。根据以上信息和数据,下列说法正确的是__________ 。

| A.N4属于一种新型化合物 | B.N4晶体熔点高,硬度大 |
| C.相同质量的N4的能量高于N2 | D.1molN4转变为N2将吸收882kJ的能量. |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,采用了中间有热交换器的转化器,如图所示,按此密闭体系中气体的流向,a、b、d三处流入(流出)的气体分别为_____ 、_____ 、______ 。
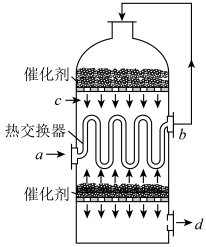
A.SO2 B.SO3、O2 C.SO2、O2 D.SO2、SO3、O2

A.SO2 B.SO3、O2 C.SO2、O2 D.SO2、SO3、O2
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。有关物质的部分性质如下表:
实验室用干燥而纯净的二氧化硫和氯气合成硫酰氯,反应的化学方程式为SO2(g)+Cl2(g) SO2Cl2(l)
SO2Cl2(l)
△H=-97.3kJ/mol。装置如图所示(夹持仪器已省略),请回答有关问题:
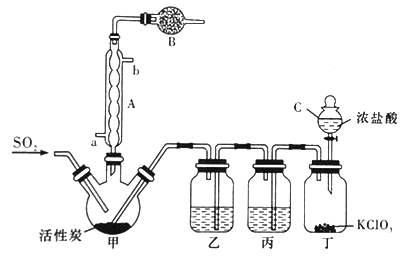
(1)仪器C的名称为___________________ 。
(2)仪器B的作用是_____________________ 。
(3)装置丙的作用为____________ ,若缺少装置乙,则硫酰氯会水解,该反应的化学方程式为___________________ 。
(4)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有_________ (填序号)
①先通冷凝水,再通气 ②控制气流速率,宜慢不宜快
③若三颈烧瓶发烫,可适当降温 ④加热三颈烧瓶
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:2ClSO3H=H2SO4+SO2Cl2,此方法得到的产品中会混有硫酸。
①从分解产物中分离出硫酰氯的方法是___________________ 。
②请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、紫色石蕊溶液)__________________________ 。
| 物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
| SO2Cl2 | -54.1 | 69.1 | ①易水解,产生大量白雾 ②易分解:SO2Cl2 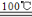 SO2↑+Cl2↑ SO2↑+Cl2↑ |
| H2SO4 | 10.4 | 338 | 具有吸水性且不易分解 |
实验室用干燥而纯净的二氧化硫和氯气合成硫酰氯,反应的化学方程式为SO2(g)+Cl2(g)
 SO2Cl2(l)
SO2Cl2(l)△H=-97.3kJ/mol。装置如图所示(夹持仪器已省略),请回答有关问题:

(1)仪器C的名称为
(2)仪器B的作用是
(3)装置丙的作用为
(4)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有
①先通冷凝水,再通气 ②控制气流速率,宜慢不宜快
③若三颈烧瓶发烫,可适当降温 ④加热三颈烧瓶
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:2ClSO3H=H2SO4+SO2Cl2,此方法得到的产品中会混有硫酸。
①从分解产物中分离出硫酰氯的方法是
②请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、紫色石蕊溶液)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】I.硫元素是动植物生长不可缺少的元素,硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
(1)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的试剂是_______ 。
(2)甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO4,方案乙:由Cu→CuO→CuSO4
①方案甲中,铜和浓硫酸反应的化学方程式是_______ 。
②这两种方案,你认为哪一种方案更合理?_______ 。理由是_______ 。
II.氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:
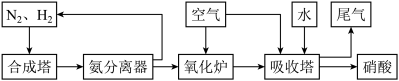
(3)合成塔中发生反应的化学方程式为_______ 。
(4)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的_______ 性质。
(5)氧化炉中,NH3转化为NO的化学方程式为_______ 。
(1)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的试剂是
(2)甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO4,方案乙:由Cu→CuO→CuSO4
①方案甲中,铜和浓硫酸反应的化学方程式是
②这两种方案,你认为哪一种方案更合理?
II.氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:

(3)合成塔中发生反应的化学方程式为
(4)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的
(5)氧化炉中,NH3转化为NO的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】硫酸厂的烟道气会严重污染环境,为保护环境、变废为宝,有多种脱硫方案,如石灰石-石膏法、氨水法、活性炭法、氧化镁法等。请写出下列反应的化学方程式。
(1)二氧化硫与熟石灰反应_______ 。
(2)亚硫酸钙( )与氧气反应
)与氧气反应_______ 。
(3)二氧化硫与氨水反应_______ 。
(4)亚硫酸铵与氧气反应_______ 。
(1)二氧化硫与熟石灰反应
(2)亚硫酸钙(
 )与氧气反应
)与氧气反应(3)二氧化硫与氨水反应
(4)亚硫酸铵与氧气反应
您最近一年使用:0次



