电子工业中,常用FeCl3溶液腐蚀覆在绝缘板上的铜箔制造印刷电路板。化学实验小组从腐蚀废液(含FeCl3、FeCl2、CuCl2)中回收铜并重新获得FeCl3晶体的流程如图:
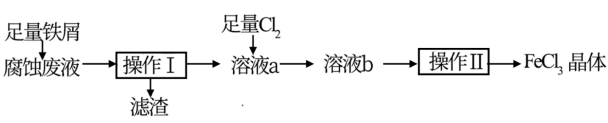
回答下列问题:
(1)检验腐蚀废液中含有Fe3+常用试剂是___ 。
(2)滤渣的成分是___ (填化学式)。从滤渣中获得铜单质,可选用的试剂是___ (填标号)。
A.稀盐酸 B.浓硫酸 C.稀硝酸 D.氯化铜溶液
(3)向溶液a中通入Cl2发生反应的离子方程式为___ 。有同学建议,使用H2O2代替Cl2以减少污染,则反应中氧化剂与还原剂的物质的量之比为___ 。
(4)甲同学用酸性KMnO4溶液检测溶液b中是否含有Fe2+。乙同学认为甲的方案不正确,理由是__ (用离子方程式表示)。

回答下列问题:
(1)检验腐蚀废液中含有Fe3+常用试剂是
(2)滤渣的成分是
A.稀盐酸 B.浓硫酸 C.稀硝酸 D.氯化铜溶液
(3)向溶液a中通入Cl2发生反应的离子方程式为
(4)甲同学用酸性KMnO4溶液检测溶液b中是否含有Fe2+。乙同学认为甲的方案不正确,理由是
更新时间:2021-01-28 19:11:42
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一、一种回收废旧磷酸亚铁锂电池正极片(主要成分为LiFePO4、炭黑和铝箔)中金属的流程如下:

(1)步骤① 中“碱溶”的化学方程式为___________
(2)步骤② 中反应的离子方程式为___________ ,若用H2O2代替HNO3,其反应的离子方程式为___________
(3)步骤④ 反应的离子方程式为___________

(1)步骤① 中“碱溶”的化学方程式为
(2)步骤② 中反应的离子方程式为
(3)步骤④ 反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO2、Fe3O4.采用以下工艺流程可由黏土钒矿制备NH4VO3。
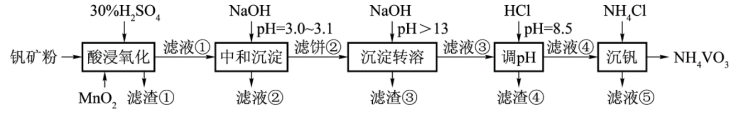
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“酸浸氧化”中,VO+和VO2+被氧化成 ,同时还有
,同时还有_______ 离子被氧化。写出VO+转化为 反应的离子方程式
反应的离子方程式_______ 。
(2)“沉淀转溶”中,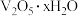 转化为钒酸盐溶解。滤渣③的主要成分是
转化为钒酸盐溶解。滤渣③的主要成分是_______ 。

该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ |
| 开始沉淀pH | 1.9 | 7.0 | 3.0 | 8.1 |
| 完全沉淀pH | 3.2 | 9.0 | 4.7 | 10.1 |
(1)“酸浸氧化”中,VO+和VO2+被氧化成
 ,同时还有
,同时还有 反应的离子方程式
反应的离子方程式(2)“沉淀转溶”中,
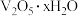 转化为钒酸盐溶解。滤渣③的主要成分是
转化为钒酸盐溶解。滤渣③的主要成分是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】以下是利用主要成分为Cu2S和Fe2O3的工业废弃固体(其他成分不参与反应)制备有关物质,实验流程如图所示:
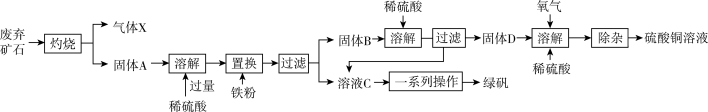
回答下列问题:
(1)气体X的化学式为____ 。
(2)加入铁粉时发生反应的离子方程式为:2H++Fe=Fe2++H2↑、____ 。
(3)常温下,固体D、O2和稀硫酸混合后几乎不反应,而加少量绿矾后随即发生反应。已知FeSO4对此反应起催化作用,则催化过程中反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O、_____ 。
(4)除杂时需先加合适的氧化剂将Fe2+氧化为Fe3+,再加试剂Y调节溶液pH以除去Fe3+,则氧化剂及试剂Y可以是____ (填编号)。
a.H2O2、CuO b.HNO3、Cu(OH)2 c.KMnO4、CuCl2 d.漂白粉、CuCO3
(5)无水硫酸铜受热分解生成氧化铜和气体,受热温度不同气体可能为SO3、SO2和O2中的一种、两种或三种。现设计如下实验测定产生的SO2、SO3和O2的物质的量,并计算各物质的化学计量数,从而确定CuSO4分解的化学方程式(已知实验结束时,硫酸铜完全分解)。
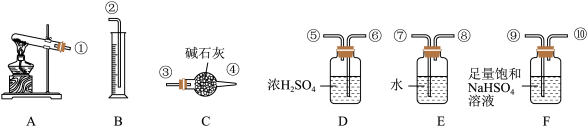
①仪器C的名称是_____ ,仪器F的作用是____ 。
②组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为:①→⑨→⑩→⑥→⑤→_____ → → → →②(填接口序号)。
③若某小组称取6.4g无水CuSO4,实验过程中装置C增加的质量为3.84g,量筒中水的体积折算成标准状况下气体体积224mL,请通过计算确定实验条件下CuSO4分解的化学方程式:___ 。

回答下列问题:
(1)气体X的化学式为
(2)加入铁粉时发生反应的离子方程式为:2H++Fe=Fe2++H2↑、
(3)常温下,固体D、O2和稀硫酸混合后几乎不反应,而加少量绿矾后随即发生反应。已知FeSO4对此反应起催化作用,则催化过程中反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O、
(4)除杂时需先加合适的氧化剂将Fe2+氧化为Fe3+,再加试剂Y调节溶液pH以除去Fe3+,则氧化剂及试剂Y可以是
a.H2O2、CuO b.HNO3、Cu(OH)2 c.KMnO4、CuCl2 d.漂白粉、CuCO3
(5)无水硫酸铜受热分解生成氧化铜和气体,受热温度不同气体可能为SO3、SO2和O2中的一种、两种或三种。现设计如下实验测定产生的SO2、SO3和O2的物质的量,并计算各物质的化学计量数,从而确定CuSO4分解的化学方程式(已知实验结束时,硫酸铜完全分解)。

①仪器C的名称是
②组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为:①→⑨→⑩→⑥→⑤→
③若某小组称取6.4g无水CuSO4,实验过程中装置C增加的质量为3.84g,量筒中水的体积折算成标准状况下气体体积224mL,请通过计算确定实验条件下CuSO4分解的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】氰化氢(HCN,易挥发,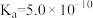 )主要应用于电镀、采矿、药物合成等工业生产。HCN、
)主要应用于电镀、采矿、药物合成等工业生产。HCN、 能抑制人体组织细胞内酶的活性,不能直接排放到环境中。
能抑制人体组织细胞内酶的活性,不能直接排放到环境中。
(1)Na2S2O3在临床上常用于氰化物的解毒剂。解毒的原理是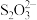 将
将 转化为
转化为 和
和 。验证该转化过程中生成
。验证该转化过程中生成 的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,
的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,_______ 。
(2)Cu2+可催化过氧化氢氧化废水中的 。
。
①反应不能在酸性条件下进行,原因是_______
②在含氰废水总量、过氧化氢用量和溶液pH一定的情况下,反应相同时间,测得 的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过
的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过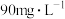 时,
时, 的氧化去除率有所下降,原因是
的氧化去除率有所下降,原因是_______ 。

(3)通过电激发产生 和
和 可处理废水中的
可处理废水中的 ,其可能的反应机理如图所示。
,其可能的反应机理如图所示。
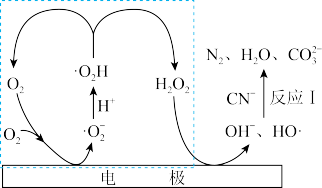
①反应I的离子方程式为_______ 。
②虚线方框内的过程可描述为_______ 。
(4)在铜镍为催化剂(Cu、CuO为活性组分,Cu的催化活性效果更好)的条件下,可利用反应: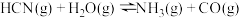

除去废气中的HCN。将含相同比例的HCN(g)、H2O(g)、CO(g)[或N2(g)]混合气体分别通过催化剂,反应相同的时间,测得HCN(g)的去除率随温度变化如图所示。200℃时含CO的混合气体中HCN(g)的去除率较高,而400℃时含CO的混合气体中HCN(g)的去除率较低。其原因是_______ 。

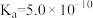 )主要应用于电镀、采矿、药物合成等工业生产。HCN、
)主要应用于电镀、采矿、药物合成等工业生产。HCN、 能抑制人体组织细胞内酶的活性,不能直接排放到环境中。
能抑制人体组织细胞内酶的活性,不能直接排放到环境中。(1)Na2S2O3在临床上常用于氰化物的解毒剂。解毒的原理是
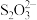 将
将 转化为
转化为 和
和 。验证该转化过程中生成
。验证该转化过程中生成 的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,
的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,(2)Cu2+可催化过氧化氢氧化废水中的
 。
。①反应不能在酸性条件下进行,原因是
②在含氰废水总量、过氧化氢用量和溶液pH一定的情况下,反应相同时间,测得
 的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过
的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过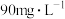 时,
时, 的氧化去除率有所下降,原因是
的氧化去除率有所下降,原因是
(3)通过电激发产生
 和
和 可处理废水中的
可处理废水中的 ,其可能的反应机理如图所示。
,其可能的反应机理如图所示。
①反应I的离子方程式为
②虚线方框内的过程可描述为
(4)在铜镍为催化剂(Cu、CuO为活性组分,Cu的催化活性效果更好)的条件下,可利用反应:
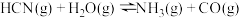

除去废气中的HCN。将含相同比例的HCN(g)、H2O(g)、CO(g)[或N2(g)]混合气体分别通过催化剂,反应相同的时间,测得HCN(g)的去除率随温度变化如图所示。200℃时含CO的混合气体中HCN(g)的去除率较高,而400℃时含CO的混合气体中HCN(g)的去除率较低。其原因是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】电子工业中常用覆铜板为材料,利用FeCl3溶液做“腐蚀液”制作印刷电路板。从废腐蚀液(含FeCl3,FeCl2和CuCl2)中回收Cu并实现FeCl3溶液循环再利用,其工艺流程如下:

回答下列问题:
(1)工业上制作印刷电路板时发生的化学反应方程式为_______ 。
(2)操作方法①为_______ ,固体A的成分为_______ (填化学式)。
(3)实验室检验溶液A中是否含有FeCl3的试剂为_______ 溶液(填化学式)。
(4)溶液A中加入NaOH溶液时产生的实验现象为_______ 。
(5)若回收过程中取废腐蚀液V L,回收到a g Cu,则废腐蚀液中Cu2+的物质的量浓度为_______ mol/L(用含a和V的表达式表示)。

回答下列问题:
(1)工业上制作印刷电路板时发生的化学反应方程式为
(2)操作方法①为
(3)实验室检验溶液A中是否含有FeCl3的试剂为
(4)溶液A中加入NaOH溶液时产生的实验现象为
(5)若回收过程中取废腐蚀液V L,回收到a g Cu,则废腐蚀液中Cu2+的物质的量浓度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】锌锰干电池是很古老的一次性电池,它的生产原料主要有软锰矿和闪锌矿。已知闪锌矿中含ZnS约80%,FeS、CuS、SiO2共约7%,其余为水分;软锰矿中含MnO2约a%,SiO2约20%,Al2O3约4%,其余为水分。科研人员开发了综合利用软锰矿和闪锌矿的同槽酸浸工艺,工艺流程如下图所示。
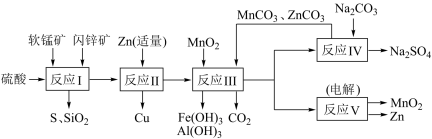
请回答下列问题:
(1)反应I需不断搅拌,目的是____________________________ 。
(2)检验反应I的滤液中含有Fe3+的试剂为____________ ;写出反应I中由FeS生成Fe3+的离子方程式____________________________________ 。
(3)反应Ⅱ加入适量锌的作用是__________________ ;反应III中MnO2的作用是________________ 。
(4)已知ZnCO3、MnCO3的Ksp分别为1.4×10-10、2.2×10-11;要使反应IV之后的溶液中Zn2+、Mn2+浓度均降到1.0×10-6mol/L,则溶液中残留的CO32-浓度至少为__________ mol/L。
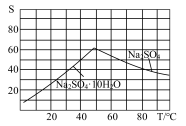
(5)图是Na2SO4和Na2SO4•10H2O的溶解 度曲线(g/100g水),则Ⅳ中得到Na2SO4固体的操作是:将分离出MnCO3和ZnCO3后的滤液________ →__________ → 用乙醇洗涤→干燥。用乙醇洗涤而不用水洗的原因是_________________________________________ 。

请回答下列问题:
(1)反应I需不断搅拌,目的是
(2)检验反应I的滤液中含有Fe3+的试剂为
(3)反应Ⅱ加入适量锌的作用是
(4)已知ZnCO3、MnCO3的Ksp分别为1.4×10-10、2.2×10-11;要使反应IV之后的溶液中Zn2+、Mn2+浓度均降到1.0×10-6mol/L,则溶液中残留的CO32-浓度至少为
(5)图是Na2SO4和Na2SO4•10H2O的溶解 度曲线(g/100g水),则Ⅳ中得到Na2SO4固体的操作是:将分离出MnCO3和ZnCO3后的滤液

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某校化学兴趣小组探究SO2与FeCl3溶液的反应。
资料:铁氰化钾 可以与Fe2+形成蓝色沉淀,常用于Fe2+检验。
可以与Fe2+形成蓝色沉淀,常用于Fe2+检验。

(1)实验室常用70%硫酸与亚硫酸钠固体制备SO2,写出反应的化学方程式_______ 。
(2)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由黄色变成浅绿色,写出相关反应的离子方程式_______ 。
(3)向试管B中溶液通入SO2至饱和,溶液变成红色,静置5min后,溶液的颜色从红色慢慢变回黄色。静置9h后,溶液慢慢由黄色变为浅绿色。
①甲同学认为溶液变红的原因是通入SO2后,Fe3+水解程度增大,形成Fe(OH)3胶体。乙同学根据SO2的性质否定了这一推论,原因是_______ 。
②丙同学取上述5min后的黄色溶液,滴加盐酸酸化的BaCl2溶液,产生白色沉淀。该同学认为SO2与Fe3+发生氧化还原反应。丁同学认为该结论不严谨,重新设计并进行实验,证明两者发生了氧化还原反应,写出实验方案及现象_______ 。
(4)查阅资料:Fe3+能与S(IV)微粒形成红色配合物。
该小组同学分析SO2水溶液成分,猜想可能是其中含S(IV)微粒SO2、H2SO3、_______ 与Fe3+形成配合物而使溶液呈现红色。进行如下实验:
①a=_______ 。
②根据实验I现象,溶液中SO2、H2SO3浓度增大,红色消失,说明红色物质可能与SO2、H2SO3无关;_______ ,红色物质可能与 有关。
有关。
(5)通过上述实验可得结论:
①SO2与FeCl3溶液的反应,可以发生配位反应、氧化还原反应。
②_______ 。
资料:铁氰化钾
 可以与Fe2+形成蓝色沉淀,常用于Fe2+检验。
可以与Fe2+形成蓝色沉淀,常用于Fe2+检验。
(1)实验室常用70%硫酸与亚硫酸钠固体制备SO2,写出反应的化学方程式
(2)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由黄色变成浅绿色,写出相关反应的离子方程式
(3)向试管B中溶液通入SO2至饱和,溶液变成红色,静置5min后,溶液的颜色从红色慢慢变回黄色。静置9h后,溶液慢慢由黄色变为浅绿色。
①甲同学认为溶液变红的原因是通入SO2后,Fe3+水解程度增大,形成Fe(OH)3胶体。乙同学根据SO2的性质否定了这一推论,原因是
②丙同学取上述5min后的黄色溶液,滴加盐酸酸化的BaCl2溶液,产生白色沉淀。该同学认为SO2与Fe3+发生氧化还原反应。丁同学认为该结论不严谨,重新设计并进行实验,证明两者发生了氧化还原反应,写出实验方案及现象
(4)查阅资料:Fe3+能与S(IV)微粒形成红色配合物。
该小组同学分析SO2水溶液成分,猜想可能是其中含S(IV)微粒SO2、H2SO3、
| 序号 | 实验 | 加入试剂 | 现象 |
| I |  | 2mL1mol/LNaHSO3溶液;再滴加几滴盐酸 | 溶液变成红色,比(3)中溶液红色深;滴加盐酸后,溶液颜色由红色变成黄色 |
| II | 2mL1mol/LNa2SO3溶液 | 溶液变成红色,比I中溶液红色深 |
②根据实验I现象,溶液中SO2、H2SO3浓度增大,红色消失,说明红色物质可能与SO2、H2SO3无关;
 有关。
有关。(5)通过上述实验可得结论:
①SO2与FeCl3溶液的反应,可以发生配位反应、氧化还原反应。
②
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】生物浸出技术在金属冶炼中应用广泛。嗜热细菌在65-80℃酸性水溶液及氧气存在下,能氧化黄铜矿(主要成分CuFeS2)产生硫酸盐,进而生产铜和绿矾,主要流程如图:
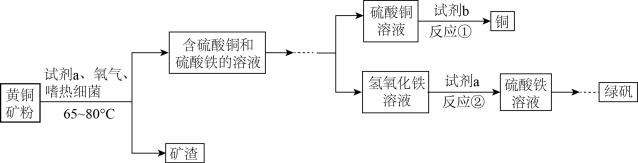
(1)分离出矿渣的操作是_______ 。该操作需要的玻璃仪器有烧杯、玻璃棒、_______ 。
(2)若试剂b为Fe粉,反应①的化学方程式为_______ 。
(3)氢氧化铁与试剂a发生中和反应,试剂a为_______ (填化学式),反应②的化学方程式为_______ 。
(4)最后由硫酸铁溶液获得绿矾晶体(FeSO4∙7H2O)的操作步骤依次为:加适量铁粉、过滤、蒸发浓缩、_______ 、过滤、洗涤、干燥。写出加适量铁粉时发生反应的离子反应方程式_______ 。

(1)分离出矿渣的操作是
(2)若试剂b为Fe粉,反应①的化学方程式为
(3)氢氧化铁与试剂a发生中和反应,试剂a为
(4)最后由硫酸铁溶液获得绿矾晶体(FeSO4∙7H2O)的操作步骤依次为:加适量铁粉、过滤、蒸发浓缩、
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】电子工业用 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,运用所学知识,回答下列问题。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,运用所学知识,回答下列问题。
(1)请写出 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式___________ 。
(2)某研究性学习小组为测定 溶液腐蚀铜后所得溶液的组成,进行了研究,其中部分实验如下:
溶液腐蚀铜后所得溶液的组成,进行了研究,其中部分实验如下:
①取少量待测液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是___________ 。
②溶液组成的测定:取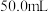 待测液,加入足量的
待测液,加入足量的 溶液,得到
溶液,得到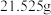 白色沉淀,则溶液中
白色沉淀,则溶液中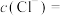
___________  。
。
(3)从腐蚀废液(主要含 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液,废液处理流程如下:
溶液,废液处理流程如下:
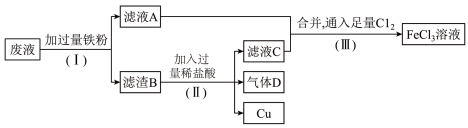
①滤渣B中主要含有___________ ,气体D是___________ 。
②写出步骤(Ⅲ)中生成 的化学方程式
的化学方程式___________ 。
③步骤(Ⅲ)中,将 换成
换成___________ 也能达到同样的目的,写出所换成的物质将 氧化为
氧化为 的离子方程式
的离子方程式___________ 。
 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,运用所学知识,回答下列问题。
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,运用所学知识,回答下列问题。(1)请写出
 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式(2)某研究性学习小组为测定
 溶液腐蚀铜后所得溶液的组成,进行了研究,其中部分实验如下:
溶液腐蚀铜后所得溶液的组成,进行了研究,其中部分实验如下:①取少量待测液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是
②溶液组成的测定:取
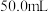 待测液,加入足量的
待测液,加入足量的 溶液,得到
溶液,得到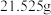 白色沉淀,则溶液中
白色沉淀,则溶液中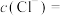
 。
。(3)从腐蚀废液(主要含
 、
、 、
、 )中回收铜,并重新获得
)中回收铜,并重新获得 溶液,废液处理流程如下:
溶液,废液处理流程如下:
①滤渣B中主要含有
②写出步骤(Ⅲ)中生成
 的化学方程式
的化学方程式③步骤(Ⅲ)中,将
 换成
换成 氧化为
氧化为 的离子方程式
的离子方程式
您最近一年使用:0次



