生物浸出技术在金属冶炼中应用广泛。嗜热细菌在65-80℃酸性水溶液及氧气存在下,能氧化黄铜矿(主要成分CuFeS2)产生硫酸盐,进而生产铜和绿矾,主要流程如图:
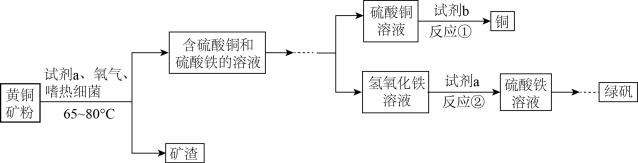
(1)分离出矿渣的操作是_______ 。该操作需要的玻璃仪器有烧杯、玻璃棒、_______ 。
(2)若试剂b为Fe粉,反应①的化学方程式为_______ 。
(3)氢氧化铁与试剂a发生中和反应,试剂a为_______ (填化学式),反应②的化学方程式为_______ 。
(4)最后由硫酸铁溶液获得绿矾晶体(FeSO4∙7H2O)的操作步骤依次为:加适量铁粉、过滤、蒸发浓缩、_______ 、过滤、洗涤、干燥。写出加适量铁粉时发生反应的离子反应方程式_______ 。

(1)分离出矿渣的操作是
(2)若试剂b为Fe粉,反应①的化学方程式为
(3)氢氧化铁与试剂a发生中和反应,试剂a为
(4)最后由硫酸铁溶液获得绿矾晶体(FeSO4∙7H2O)的操作步骤依次为:加适量铁粉、过滤、蒸发浓缩、
更新时间:2023/10/08 08:33:55
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】铜镉渣主要含锌、铜、铁、镉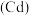 、钴
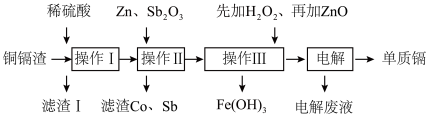
、钴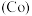 等单质。湿法炼锌产生的铜镉渣用于生产金属镉的工艺流程如下:
等单质。湿法炼锌产生的铜镉渣用于生产金属镉的工艺流程如下:
下表列出了相关金属离子生成氢氧化物沉淀的 (金属离子的起始浓度均为
(金属离子的起始浓度均为 )
)
(1)酸浸时,粉碎铜镉渣的目的是___________ 。
(2)操作I产生的滤渣I主要成分为___________ (填化学式)。如果在实验室模拟该工艺流程,洗涤该沉淀的操作方法是___________ 。
(3)①操作Ⅲ中先加入适量 ,发生反应的离子方程式为
,发生反应的离子方程式为___________ 。
②再加入 控制反应液的
控制反应液的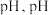 范围为
范围为___________ 。
③若加入的 不足,加入
不足,加入 后所得的电解液中会含有
后所得的电解液中会含有 元素。请设计实验方案加以检验:
元素。请设计实验方案加以检验:___________ 。
(4)处理含镉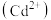 废水,常加入
废水,常加入 实现沉淀转化,若反应达到平衡后,溶液中的
实现沉淀转化,若反应达到平衡后,溶液中的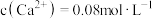 ,溶液中
,溶液中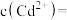
___________  [已知
[已知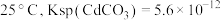 ,
,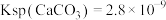 ]。
]。
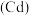 、钴
、钴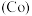 等单质。湿法炼锌产生的铜镉渣用于生产金属镉的工艺流程如下:
等单质。湿法炼锌产生的铜镉渣用于生产金属镉的工艺流程如下:
下表列出了相关金属离子生成氢氧化物沉淀的
 (金属离子的起始浓度均为
(金属离子的起始浓度均为 )
)| 氢氧化物 |  |  |  |
开始沉淀的 | 1.5 | 6.5 | 7.2 |
沉淀完全的 | 3.3 | 9.9 | 9.5 |
(2)操作I产生的滤渣I主要成分为
(3)①操作Ⅲ中先加入适量
 ,发生反应的离子方程式为
,发生反应的离子方程式为②再加入
 控制反应液的
控制反应液的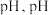 范围为
范围为③若加入的
 不足,加入
不足,加入 后所得的电解液中会含有
后所得的电解液中会含有 元素。请设计实验方案加以检验:
元素。请设计实验方案加以检验:(4)处理含镉
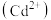 废水,常加入
废水,常加入 实现沉淀转化,若反应达到平衡后,溶液中的
实现沉淀转化,若反应达到平衡后,溶液中的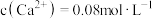 ,溶液中
,溶液中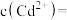
 [已知
[已知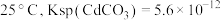 ,
,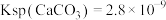 ]。
]。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】FeCO3是制备补血剂原料之一。一种在实验室里制备FeCO3的流程如图所示:
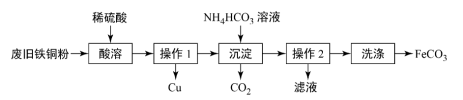
回答下列问题:
(1)“酸溶”时,常采取加热或搅拌措施,其目的是___ 。
(2)写出酸溶步骤的离子反应方程式___ 。
(3)“操作1”和“操作2”为___ 操作。
(4)写出“沉淀”时反应的化学方程式:___ 。
(4)“沉淀”反应前,检验溶液中是否含有Fe2+且不含Fe3+,写出检验的具体操作___ 。
(5)检验FeCO3是否“洗涤”干净的方法是___ 。

回答下列问题:
(1)“酸溶”时,常采取加热或搅拌措施,其目的是
(2)写出酸溶步骤的离子反应方程式
(3)“操作1”和“操作2”为
(4)写出“沉淀”时反应的化学方程式:
(4)“沉淀”反应前,检验溶液中是否含有Fe2+且不含Fe3+,写出检验的具体操作
(5)检验FeCO3是否“洗涤”干净的方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】硫酸锰是一种重要的化工中问体。一种以高硫锰矿(主要成分为含锰化合物及FeS)为原料制备硫酸锰的工艺流程如下:

已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、 MgO。
②金属离子在水溶液中沉淀的pH范围如下表所示(25°C):
③离子浓度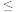 10-5mol·L-1时,离子沉淀完全。
10-5mol·L-1时,离子沉淀完全。
请回答:
(1)“混合焙烧”主要目的是_______
(2)若试剂a为MnO2,则氧化步骤发生反应的离子方程式为_______ ,若省略“氧化”步骤,造成的影响是_______ 。
(3)“中和除杂”时,应控制溶液的pH范围是_______ 。
(4)“氟化除杂”后,溶液中c(F- )浓度为0.05mol/L。则溶液中c(Mg2+)和c (Ca2+)的比值=_______ (已知: Ksp(MgF2)= 6.4×10-10; Ksp(CaF2)=3.6×10-12)
(5)“碳化结晶”时选择NH4HCO3, NH4HCO3溶液中各离子浓度大小顺序为_______ ,(已知CH3COONH4溶液呈中性)“碳化结晶”时发生反应的离子方程式为_______ ,“碳化结晶”时不选择Na2CO3溶液的原因是_______ 。

已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、 MgO。
②金属离子在水溶液中沉淀的pH范围如下表所示(25°C):
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Al(OH)3 |
| 开始沉淀 | 1.9 | 7.6 | 7.3 | 3.0 |
| 完全沉淀 | 3.2 | 9.6 | 9.3 | 5.2 |
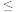 10-5mol·L-1时,离子沉淀完全。
10-5mol·L-1时,离子沉淀完全。请回答:
(1)“混合焙烧”主要目的是
(2)若试剂a为MnO2,则氧化步骤发生反应的离子方程式为
(3)“中和除杂”时,应控制溶液的pH范围是
(4)“氟化除杂”后,溶液中c(F- )浓度为0.05mol/L。则溶液中c(Mg2+)和c (Ca2+)的比值=
(5)“碳化结晶”时选择NH4HCO3, NH4HCO3溶液中各离子浓度大小顺序为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】固体粉末X中含有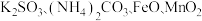 等物质,取X进行连续实验,过程如下:
等物质,取X进行连续实验,过程如下:
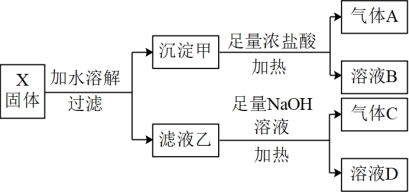
回答下列问题:
(1)产生“气体A”的离子方程式为_______ ;
(2)“溶液B”中存在的所有阳离子有_______ ;
(3)“气体C”的检验方法为_______ ;
(4)向“溶液D”中加入足量盐酸酸化的 溶液,发现有沉淀,说明其中存在
溶液,发现有沉淀,说明其中存在_______ (填离子符号)。
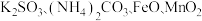 等物质,取X进行连续实验,过程如下:
等物质,取X进行连续实验,过程如下:
回答下列问题:
(1)产生“气体A”的离子方程式为
(2)“溶液B”中存在的所有阳离子有
(3)“气体C”的检验方法为
(4)向“溶液D”中加入足量盐酸酸化的
 溶液,发现有沉淀,说明其中存在
溶液,发现有沉淀,说明其中存在
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】碘化钠在医药中用作甲状腺肿瘤防治剂、祛痰剂和利尿剂,也用作食品添加剂、感光剂等。工业上用NaOH溶液、水合肼制取碘化钠固体,其制备流程图如下:
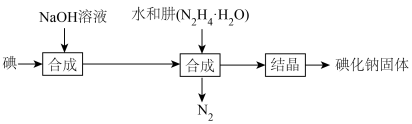
已知: 在100℃以上分解。
在100℃以上分解。
(1)已知:在合成过程的反应产物中含有NaIO3,则在合成过程中消耗了3molI2,所生成NaIO3的物质的量为___________ mol。
(2)写出还原过程中的离子方程式___________ ;在还原过程中,为了加快反应,可采取可提高反应温度,但温度不得超过___________ ℃;请选择下列试剂检测所得碘化钠固体中是否含有NaIO3杂质___________ (选填字母)。
A.FeCl2溶液 B.冰醋酸 C.KI溶液 D.淀粉溶液
(3)测定产品中NaI含量的实验步骤如下:
a.称取4.000g样品、溶解,在250mL容量瓶中定容;
b.量取25.00ml待测液于锥形瓶中,然后加入足量的FeCl3溶液,充分反应后,再加入淀粉溶液作指示剂;
c.用 的Na2S2O3溶液进行滴定至终点(发生反应的方程式为:
的Na2S2O3溶液进行滴定至终点(发生反应的方程式为: ),重复测定2次,所得的相关数据如下表:
),重复测定2次,所得的相关数据如下表:
①操作b中,加入足量的FeCl3溶液时所发生的离子方程式为___________ 。
②滴定终点观察到的现象为___________ 。
③计算该样品中NaI的含量为___________ 。(只写出有具体数值的表达式即可)
(4)碘化钠固体的保存方法是___________ 。

已知:
 在100℃以上分解。
在100℃以上分解。(1)已知:在合成过程的反应产物中含有NaIO3,则在合成过程中消耗了3molI2,所生成NaIO3的物质的量为
(2)写出还原过程中的离子方程式
A.FeCl2溶液 B.冰醋酸 C.KI溶液 D.淀粉溶液
(3)测定产品中NaI含量的实验步骤如下:
a.称取4.000g样品、溶解,在250mL容量瓶中定容;
b.量取25.00ml待测液于锥形瓶中,然后加入足量的FeCl3溶液,充分反应后,再加入淀粉溶液作指示剂;
c.用
 的Na2S2O3溶液进行滴定至终点(发生反应的方程式为:
的Na2S2O3溶液进行滴定至终点(发生反应的方程式为: ),重复测定2次,所得的相关数据如下表:
),重复测定2次,所得的相关数据如下表:| 测定序号 | 待测液体积/mL | 标准液滴定管起点读数/mL | 标准液滴定管终点读数/mL |
| 1 | 25.00 | 0.06 | 24.04 |
| 2 | 25.00 | 0.02 | 24.02 |
| 3 | 25.00 | 0.12 | 24.14 |
②滴定终点观察到的现象为
③计算该样品中NaI的含量为
(4)碘化钠固体的保存方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】实验室以锈蚀程度很大的废铁屑为原料制备FeCl3·6H2O晶体的流程可简要表示如下:
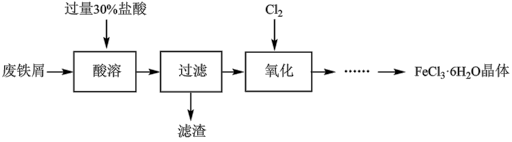
已知:在水溶液中Fe2+能与K3Fe(CN)6生成蓝色沉淀Fe3[Fe(CN)6]2。
试回答下列问题:
(1) “酸溶”过程中发生主要反应有:
①Fe + 2H+= Fe2++ H2↑;②Fe2O3+ 6 H+= 2Fe3++ 3H2O;③__________________ 。(用离子方程式)
(2) “酸溶”需控制温度在40℃左右,最佳的加热方式是____________ 。
(3) “氧化”过程可在下图所示装置中进行。
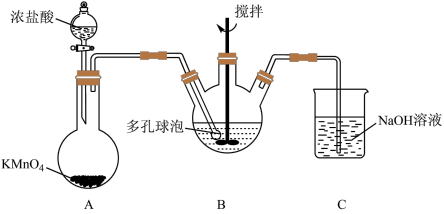
①装置A中KMnO4与浓盐酸反应生成MnCl2和Cl2,其离子方程式为______________________ 。
②装置C的作用是__________________________________________________ 。
③为使Cl2能充分发生反应,除在B中使用多孔球泡和搅拌外,实验中可采取的措施是_____________________________________________________________________ 。
④证明装置B溶液中Fe2+已完全________________________________________________________________ 。

已知:在水溶液中Fe2+能与K3Fe(CN)6生成蓝色沉淀Fe3[Fe(CN)6]2。
试回答下列问题:
(1) “酸溶”过程中发生主要反应有:
①Fe + 2H+= Fe2++ H2↑;②Fe2O3+ 6 H+= 2Fe3++ 3H2O;③
(2) “酸溶”需控制温度在40℃左右,最佳的加热方式是
(3) “氧化”过程可在下图所示装置中进行。

①装置A中KMnO4与浓盐酸反应生成MnCl2和Cl2,其离子方程式为
②装置C的作用是
③为使Cl2能充分发生反应,除在B中使用多孔球泡和搅拌外,实验中可采取的措施是
④证明装置B溶液中Fe2+已完全
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.(1)指出如下图实验装置中的错误之处(加热装置中烧杯底部已垫有石棉网)
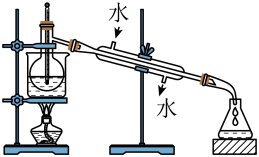
①_____________ ;②_________ 。
(2)图是某学生的过滤操作示意图,其操作不规范的是______
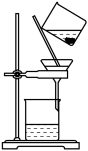
a 漏斗下口尖端未紧靠烧杯壁 b 玻璃棒有引流 作用
c 将滤纸湿润,使其紧贴漏斗壁 d 滤纸边缘低于漏斗口边缘
e 用玻璃棒在漏斗中轻轻搅动以加快过滤速度
Ⅱ.海藻中提取碘的流程如图,已知氧化过程发生反应的化学方程式为:Cl2+2KI=2KCl+I2。请回答下列问题:

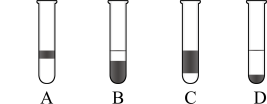
(1)指出提取碘的过程中有关实验操作①和②的名称:__________ ;________ 。
(2)在3 mL含碘的水溶液中加入1mL四氯化碳,振荡静置后观察到试管里的分层现象是上图中的_____ (注:试管中深色区为有色溶液),上层无色溶液的溶质是_____ 下层颜色是_____ 。
(3)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过的操作是_______ 。

①
(2)图是某学生的过滤操作示意图,其操作不规范的是

a 漏斗下口尖端未紧靠烧杯壁 b 玻璃棒有引流 作用
c 将滤纸湿润,使其紧贴漏斗壁 d 滤纸边缘低于漏斗口边缘
e 用玻璃棒在漏斗中轻轻搅动以加快过滤速度
Ⅱ.海藻中提取碘的流程如图,已知氧化过程发生反应的化学方程式为:Cl2+2KI=2KCl+I2。请回答下列问题:


(1)指出提取碘的过程中有关实验操作①和②的名称:
(2)在3 mL含碘的水溶液中加入1mL四氯化碳,振荡静置后观察到试管里的分层现象是上图中的
(3)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过的操作是
您最近一年使用:0次
【推荐2】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如图所示。回答下列问题:
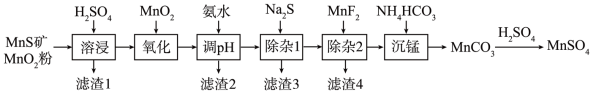
相关金属离子[c0(Mn+)=0.1mol∙L-1]形成氢氧化物沉淀的 pH范围如表:
(1)“滤渣1”含有S和_______ ; 写出“溶浸”中二氧化锰与硫化锰反应的化学方程式为_______
(2)“氧化”中添加适量的MnO2的作用是将 Fe2+氧化为 Fe3+,写出该反应的离子方程式为_______ 。
(3)调pH范围为4.7~6,滤渣2成分的化学式为_________ 。
(4)“除杂1”的目的是除去Zn2+和 Ni2+,“滤渣3”的主要成分是__________ 。
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是_______ 。
(6)写出“沉锰”的离子方程式_______
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为 LiNixCoyMnzO2,其中Ni、Co、Mn 的化合价分别为+2、+3、+4 当x=y= 时,z=
时,z=_______ 。

相关金属离子[c0(Mn+)=0.1mol∙L-1]形成氢氧化物沉淀的 pH范围如表:
| 金属离子 | Mn2+ | Fe2+ | Fe³⁺ | Al3⁺ | Mg2+ | Zn2+ | Ni2+ |
| 开始沉淀的 pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“滤渣1”含有S和
(2)“氧化”中添加适量的MnO2的作用是将 Fe2+氧化为 Fe3+,写出该反应的离子方程式为
(3)调pH范围为4.7~6,滤渣2成分的化学式为
(4)“除杂1”的目的是除去Zn2+和 Ni2+,“滤渣3”的主要成分是
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
(6)写出“沉锰”的离子方程式
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为 LiNixCoyMnzO2,其中Ni、Co、Mn 的化合价分别为+2、+3、+4 当x=y=
 时,z=
时,z=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】以二氧化铈(CeO2)为原料制备碳酸铈(Ce2(CO3)3)的工业流程如下:
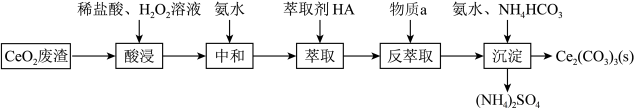
已知水溶液中的Ce3+能被有机萃取剂(HA)萃取,萃取原理可表示为 ;回答下列问题:
;回答下列问题:
(1)写出两条可以提高酸浸效率的措施___________ 、___________ 。
(2)写出酸浸过程中发生反应的离子方程式___________ ,其中H2O2的作用是___________ 。
(3)萃取前加氨水中和的目的是___________ (用平衡移动的原理解释)。
(4)写出物质a的化学式___________ 。
(5)写出沉淀过程的离子方程式___________ 。
(6)该流程中可循环使用的试剂为___________ 。

已知水溶液中的Ce3+能被有机萃取剂(HA)萃取,萃取原理可表示为
 ;回答下列问题:
;回答下列问题:(1)写出两条可以提高酸浸效率的措施
(2)写出酸浸过程中发生反应的离子方程式
(3)萃取前加氨水中和的目的是
(4)写出物质a的化学式
(5)写出沉淀过程的离子方程式
(6)该流程中可循环使用的试剂为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】二茂铁 是一种橙黄色粉末,其熔点是
是一种橙黄色粉末,其熔点是 ,在
,在 时开始升华;沸点是
时开始升华;沸点是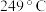 ,不溶于水,易溶于苯、乙醚等有机溶剂;化学性质稳定,
,不溶于水,易溶于苯、乙醚等有机溶剂;化学性质稳定, 内不分解。制备二茂铁的原理:
内不分解。制备二茂铁的原理: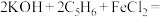
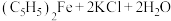 ,制备装置(夹持装置未画出)和实验步骤如下:
,制备装置(夹持装置未画出)和实验步骤如下:
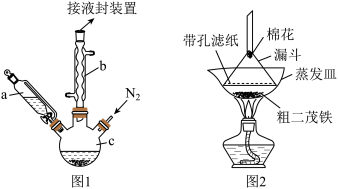
①在三颈烧瓶中加入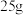 粉末状的
粉末状的 ,并从仪器a中加入
,并从仪器a中加入 无水乙醚到烧瓶中,充分搅拌,同时通
无水乙醚到烧瓶中,充分搅拌,同时通 约
约 ;
;
②再从仪器a滴入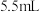 环戊二烯(
环戊二烯( )后搅拌;
)后搅拌;
③将 无水
无水 与
与 (二甲亚砜,作溶剂)配成的溶液
(二甲亚砜,作溶剂)配成的溶液 装入仪器a中,慢慢滴入仪器c中,
装入仪器a中,慢慢滴入仪器c中,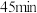 滴完,继续搅拌
滴完,继续搅拌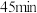 ;
;
④再从仪器a加入 无水乙醚搅拌;
无水乙醚搅拌;
⑤将c中的液体转入分液漏斗中,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器b的作用是_______
(2)步骤①中通入约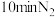 的目的是
的目的是_______ 。
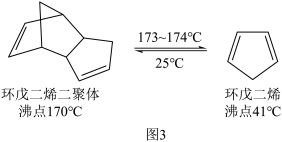
(3)制备二茂铁的原料环戊二烯( )可由环戊二烯二聚体获得,已知二者的转化关系如图3,则从二者混合物中分离得到环戊二烯的操作方法为
)可由环戊二烯二聚体获得,已知二者的转化关系如图3,则从二者混合物中分离得到环戊二烯的操作方法为_______ 。
(4)该套发生装置还可以制取溴苯,恒压分液漏斗中加入苯和液溴,分液漏斗中加入铁粉,写出该反应的化学方程式:_______
(5)步骤⑤中先用盐酸洗涤再用水洗,用盐酸洗涤的目的是_______ ,判断已水洗干净的方法是_______
(6)二茂铁粗产品的提纯过程在图2装置中进行,其操作名称为_______ ;该操作中棉花的作用是_______ 。
(7)若最终制得纯净的二茂铁 ,环戊二烯(
,环戊二烯( )的密度为
)的密度为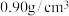 该二茂铁的产率为
该二茂铁的产率为_______ (产率=产品实际产量÷理论产量)。
 是一种橙黄色粉末,其熔点是
是一种橙黄色粉末,其熔点是 ,在
,在 时开始升华;沸点是
时开始升华;沸点是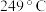 ,不溶于水,易溶于苯、乙醚等有机溶剂;化学性质稳定,
,不溶于水,易溶于苯、乙醚等有机溶剂;化学性质稳定, 内不分解。制备二茂铁的原理:
内不分解。制备二茂铁的原理: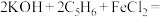
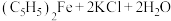 ,制备装置(夹持装置未画出)和实验步骤如下:
,制备装置(夹持装置未画出)和实验步骤如下:
①在三颈烧瓶中加入
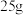 粉末状的
粉末状的 ,并从仪器a中加入
,并从仪器a中加入 无水乙醚到烧瓶中,充分搅拌,同时通
无水乙醚到烧瓶中,充分搅拌,同时通 约
约 ;
;②再从仪器a滴入
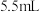 环戊二烯(
环戊二烯( )后搅拌;
)后搅拌;③将
 无水
无水 与
与 (二甲亚砜,作溶剂)配成的溶液
(二甲亚砜,作溶剂)配成的溶液 装入仪器a中,慢慢滴入仪器c中,
装入仪器a中,慢慢滴入仪器c中,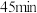 滴完,继续搅拌
滴完,继续搅拌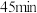 ;
;④再从仪器a加入
 无水乙醚搅拌;
无水乙醚搅拌;⑤将c中的液体转入分液漏斗中,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器b的作用是
(2)步骤①中通入约
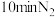 的目的是
的目的是(3)制备二茂铁的原料环戊二烯(
 )可由环戊二烯二聚体获得,已知二者的转化关系如图3,则从二者混合物中分离得到环戊二烯的操作方法为
)可由环戊二烯二聚体获得,已知二者的转化关系如图3,则从二者混合物中分离得到环戊二烯的操作方法为
(4)该套发生装置还可以制取溴苯,恒压分液漏斗中加入苯和液溴,分液漏斗中加入铁粉,写出该反应的化学方程式:
(5)步骤⑤中先用盐酸洗涤再用水洗,用盐酸洗涤的目的是
(6)二茂铁粗产品的提纯过程在图2装置中进行,其操作名称为
(7)若最终制得纯净的二茂铁
 ,环戊二烯(
,环戊二烯( )的密度为
)的密度为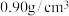 该二茂铁的产率为
该二茂铁的产率为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
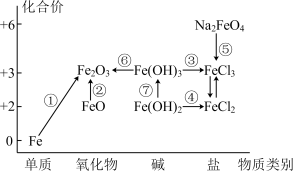
【推荐3】元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为铁元素的“价一类”二维图,箭头表示部分物质间的转化关系。
(1) 中Fe的化合价为
中Fe的化合价为______________________ 。
(2)磁性氧化铁的化学式为______________________ ,将其完全溶于较浓的盐酸中,其反应的离子方程式为______________________ 。
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
______________________ 。
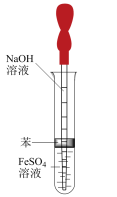
(4)根据下左图装置,用NaOH 溶液、铁屑、稀 等试剂制备
等试剂制备 沉淀。
沉淀。______________________ 。
②在I和Ⅱ中加入试剂后,应先______________________ (选填“打开”或“关闭”)止水夹。某同学用上右图装置也可制备 沉淀,原因是
沉淀,原因是______________________ 。
(5)已知 在强碱溶液中稳定存在,pH越小稳定性越差;则制备
在强碱溶液中稳定存在,pH越小稳定性越差;则制备 时需要在
时需要在______________________ (填“酸性”“碱性”或“中性”)环境中进行;  也可以作为净水剂,能与水反应生成具有吸附性的 Fe(OH)₃胶体和一种无色无味气体,写出其中离子方程式:
也可以作为净水剂,能与水反应生成具有吸附性的 Fe(OH)₃胶体和一种无色无味气体,写出其中离子方程式:______________________ 。检验溶液中 的试剂是
的试剂是______________________ 。
(1)
 中Fe的化合价为
中Fe的化合价为(2)磁性氧化铁的化学式为
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
(4)根据下左图装置,用NaOH 溶液、铁屑、稀
 等试剂制备
等试剂制备 沉淀。
沉淀。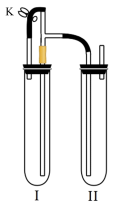
②在I和Ⅱ中加入试剂后,应先
 沉淀,原因是
沉淀,原因是(5)已知
 在强碱溶液中稳定存在,pH越小稳定性越差;则制备
在强碱溶液中稳定存在,pH越小稳定性越差;则制备 时需要在
时需要在 也可以作为净水剂,能与水反应生成具有吸附性的 Fe(OH)₃胶体和一种无色无味气体,写出其中离子方程式:
也可以作为净水剂,能与水反应生成具有吸附性的 Fe(OH)₃胶体和一种无色无味气体,写出其中离子方程式: 的试剂是
的试剂是
您最近一年使用:0次



