下列说法正确的
①任何稀的强酸与稀的强碱反应生成 放出的热即为中和热
放出的热即为中和热
②对任何一个化学平衡,其他条件不变时,当温度发生变化,平衡一定发生移动
③平衡正向移动,某反应物的转化率一定增大
④一个化学反应的限度是可以改变的
⑤铁片与稀盐酸制取氢气时,加入 固体或
固体或 固体都不影响生成氢气的速率
固体都不影响生成氢气的速率
①任何稀的强酸与稀的强碱反应生成
 放出的热即为中和热
放出的热即为中和热②对任何一个化学平衡,其他条件不变时,当温度发生变化,平衡一定发生移动
③平衡正向移动,某反应物的转化率一定增大
④一个化学反应的限度是可以改变的
⑤铁片与稀盐酸制取氢气时,加入
 固体或
固体或 固体都不影响生成氢气的速率
固体都不影响生成氢气的速率| A.②④ | B.②④⑤ | C.①③④ | D.除⑤以外 |
更新时间:2021-02-03 11:45:42
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关热化学方程式书写与对应表述均正确的是
A.稀硫酸与 NaOH溶液反应: NaOH溶液反应: |
B.在101kPa下 的燃烧热 的燃烧热 ,则水分解的热化学方程式为 ,则水分解的热化学方程式为 |
C.已知 的燃烧热 的燃烧热 ,则有 ,则有 |
D.已知9.6g硫粉与11.2g铁粉混合加热生成17.6g FeS时放出19.12kJ热量,则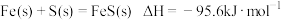 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列热化学方程式书写正确的是(ΔH的绝对值均正确)
A.S(s)+ O2(g)===SO3(g) ΔH=-315 kJ·mol-1(燃烧热) O2(g)===SO3(g) ΔH=-315 kJ·mol-1(燃烧热) |
| B.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1(中和热) |
| C.C2H5OH+3O2===2CO2+3H2O ΔH=-1 368.8 kJ·mol-1(反应热) |
| D.2H2O(g)===2H2(g)+O2(g) ΔH=-483.6 kJ·mol-1(反应热) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】Burns 和Dainton研究发现Cl2与CO合成COCl2的反应机理如下:
①Cl2(g) 2Cl· (g)快;
2Cl· (g)快;
②CO(g) + Cl· (g) COCl· (g)快;
COCl· (g)快;
③COCl· (g) + Cl2(g) COCl2(g) + Cl· (g)慢。
COCl2(g) + Cl· (g)慢。
其中反应②存在V正= k正c(CO)c(Cl·)、V逆= k 逆c(COCl· )。
下列说法正确的是
①Cl2(g)
 2Cl· (g)快;
2Cl· (g)快;②CO(g) + Cl· (g)
 COCl· (g)快;
COCl· (g)快;③COCl· (g) + Cl2(g)
 COCl2(g) + Cl· (g)慢。
COCl2(g) + Cl· (g)慢。其中反应②存在V正= k正c(CO)c(Cl·)、V逆= k 逆c(COCl· )。
下列说法正确的是
| A.使用催化剂反应②的k正、k逆均不发生改变 |
B.反应②的平衡常数K = |
| C.升高温度反应②的k正增加,k逆减小 |
| D.选择合适的催化剂能加快该反应的速率,并提高COCl2的平衡产率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】科学家研究发现,在一种特殊催化剂和水参与下, 和
和 可高选择性地直接合成
可高选择性地直接合成 ,其反应机理如图所示,其中
,其反应机理如图所示,其中 表示被吸附在催化剂表面的M。
表示被吸附在催化剂表面的M。
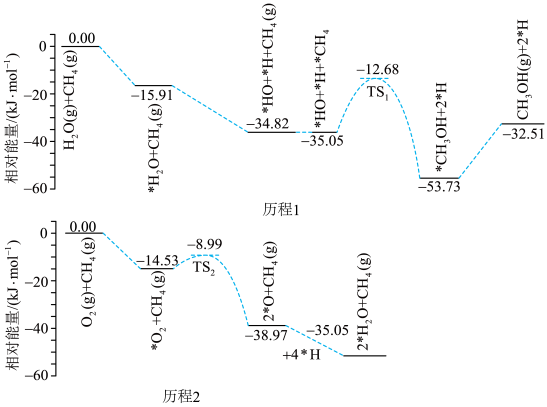
下列说法错误的是
 和
和 可高选择性地直接合成
可高选择性地直接合成 ,其反应机理如图所示,其中
,其反应机理如图所示,其中 表示被吸附在催化剂表面的M。
表示被吸附在催化剂表面的M。
下列说法错误的是
A.在催化剂表面,存在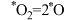 ,该过程放热 ,该过程放热 |
B.总反应是化合反应, 在总反应中相当于催化 在总反应中相当于催化 |
C.若起始时加入的是 、 、 、 、 ,则产物甲醇分子一定是 ,则产物甲醇分子一定是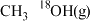 |
D.该过程的决速步反应为取代反应: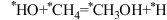 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一真空定容的密闭容器中盛有1mol PCl5,发生反应PCl5(g)  PCl3(g)+Cl2(g),一定条件下平衡时PCl5所占的体积百分数为M,若相同条件相同容器中,最初放入0.5mol PCl5,则平衡时,PCl5的体积百分数为N,下列结论正确的是
PCl3(g)+Cl2(g),一定条件下平衡时PCl5所占的体积百分数为M,若相同条件相同容器中,最初放入0.5mol PCl5,则平衡时,PCl5的体积百分数为N,下列结论正确的是
 PCl3(g)+Cl2(g),一定条件下平衡时PCl5所占的体积百分数为M,若相同条件相同容器中,最初放入0.5mol PCl5,则平衡时,PCl5的体积百分数为N,下列结论正确的是
PCl3(g)+Cl2(g),一定条件下平衡时PCl5所占的体积百分数为M,若相同条件相同容器中,最初放入0.5mol PCl5,则平衡时,PCl5的体积百分数为N,下列结论正确的是| A.M>N | B.M=N | C.M<N | D.无法比较 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】对于处于化学平衡状态的反应C(s)+H2O(g) CO(g)+H2(g);ΔH>0,既要提高反应速率又要提高H2O的转化率,下列措施中可行的是
CO(g)+H2(g);ΔH>0,既要提高反应速率又要提高H2O的转化率,下列措施中可行的是
 CO(g)+H2(g);ΔH>0,既要提高反应速率又要提高H2O的转化率,下列措施中可行的是
CO(g)+H2(g);ΔH>0,既要提高反应速率又要提高H2O的转化率,下列措施中可行的是| A.增大H2O(g)的浓度 | B.升高温度 |
| C.降低压强 | D.增加碳的量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】工业上利用固体Ga与 高温条件下合成半导体材料氮化镓(GaN)固体,同时有氢气生成。反应中,每生成3mol
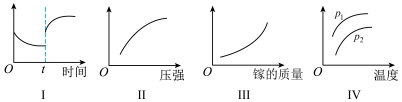
高温条件下合成半导体材料氮化镓(GaN)固体,同时有氢气生成。反应中,每生成3mol 时放出30.8kJ的热量。恒温恒容密闭体系内进行上述反应,下列有关下图的表达正确的是
时放出30.8kJ的热量。恒温恒容密闭体系内进行上述反应,下列有关下图的表达正确的是
 高温条件下合成半导体材料氮化镓(GaN)固体,同时有氢气生成。反应中,每生成3mol
高温条件下合成半导体材料氮化镓(GaN)固体,同时有氢气生成。反应中,每生成3mol 时放出30.8kJ的热量。恒温恒容密闭体系内进行上述反应,下列有关下图的表达正确的是
时放出30.8kJ的热量。恒温恒容密闭体系内进行上述反应,下列有关下图的表达正确的是
| A.I图像中如果纵坐标为正反应速率,则t时刻改变的条件可以为升温或加压 |
B.Ⅱ图像中纵坐标可以为 的百分含量 的百分含量 |
| C.Ⅲ图像中纵坐标可以为化学反应速率 |
D.Ⅳ图像中纵坐标可以为体系内混合气体平均相对分子质量,且 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某温度下,某反应达平衡时平衡常数K=c(C)·c(D)/c(A)·c(B)。恒容时,温度升高,C的物质的量浓度减小。下列说法正确的是( )
| A.该反应的焓变ΔH>0 |
| B.恒温恒容时,增大体系压强,c(D)一定增大 |
| C.升高温度,逆反应速率减小 |
D.该反应的化学方程式可能为A(g)+B(g) C(g)+D(g) C(g)+D(g) |
您最近一年使用:0次

 +OH-
+OH-



