T ℃时,在2 L的密闭容器中,气体X、Y和Z三种物质的物质的量随时间变化的曲线如图所示,下列描述正确的是


A.容器中化学反应为X(g)+Y(g)  Z(g) Z(g) |
| B.0~10 s,X表示的平均化学反应速率为0.04 mol/(L·s) |
| C.使用催化剂只能加快0~10 s间的反应速率 |
| D.10s时Z的浓度为1.6mol/L |
19-20高二上·海南海口·阶段练习 查看更多[2]
更新时间:2021-01-15 00:03:51
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应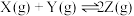
 ,一段时间后达到平衡。反应过程中测定的数据如下表:
,一段时间后达到平衡。反应过程中测定的数据如下表:
下列说法正确的是
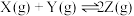
 ,一段时间后达到平衡。反应过程中测定的数据如下表:
,一段时间后达到平衡。反应过程中测定的数据如下表:| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.前4min内反应的平均速率 |
B.其他条件不变,升高温度,反应达到新平衡前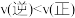 |
| C.该温度下此反应的平衡常数K=1.44 |
| D.其他条件不变,再充入0.2molZ,平衡时X的体积分数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】将一定物质的量的HI(g)置于2L的恒容密闭容器中,只发生反应2HI(g)  H2(g)+I2(g) △H,在其他条件相同时,反应物HI(g)的物质的量n(mol)随反应时间(min)的变化情况如下表:
H2(g)+I2(g) △H,在其他条件相同时,反应物HI(g)的物质的量n(mol)随反应时间(min)的变化情况如下表:
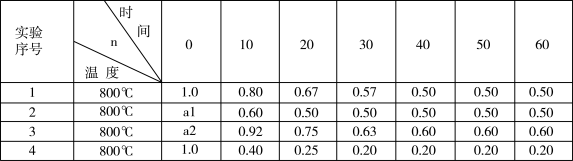
根据表中数据,下列说法正确的是
 H2(g)+I2(g) △H,在其他条件相同时,反应物HI(g)的物质的量n(mol)随反应时间(min)的变化情况如下表:
H2(g)+I2(g) △H,在其他条件相同时,反应物HI(g)的物质的量n(mol)随反应时间(min)的变化情况如下表:
根据表中数据,下列说法正确的是
| A.在实验1中,反应在10至20分钟时间内v(HI)=1.3×10-2mol/(L•min) |
| B.在实验2中,第20min时反应恰好达到平衡状态 |
| C.根据实验2和实验3,无法说明浓度越大反应速率越快 |
| D.根据实验2和实验4,无法判断反应△H的正负号 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】高炉炼铁过程中发生反应:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ΔH=akJ/mol,该反应在不同温度下的平衡常数见右表。下列说法正确的是( )
2Fe(s)+3CO2(g) ΔH=akJ/mol,该反应在不同温度下的平衡常数见右表。下列说法正确的是( )
 2Fe(s)+3CO2(g) ΔH=akJ/mol,该反应在不同温度下的平衡常数见右表。下列说法正确的是( )
2Fe(s)+3CO2(g) ΔH=akJ/mol,该反应在不同温度下的平衡常数见右表。下列说法正确的是( )| 温度T/°C | 1000 | 1150 | 1300 |
| 平衡常数K | 4.0 | 3.7 | 3.5 |
| A.a>0 |
| B.当反应达到平衡时,在其他条件不变的情况下,加入少量的Fe2O3,CO的转化率不变 |
| C.为了使该反应的K增大,可以在其他条件不变时,增大c(CO) |
| D.1000°C下Fe2O3与CO反应,tmin达到平衡时c(CO)=2×10-3mol/L,则用CO表示该反应的平均速率为2×10-3/tmol/(L·min) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】Burns和Dainton研究发现Cl2与CO合成COCl2的反应机理如下:
①Cl2(g) 2Cl·(g) 快
2Cl·(g) 快
②CO(g)+Cl·(g) COCl·(g) 快
COCl·(g) 快
③COCl·(g)+Cl2(g) COCl2(g)+Cl·(g) 慢
COCl2(g)+Cl·(g) 慢
其中反应②存在v正=k正c(CO)c(Cl·)、v逆=k逆c(COCl·)k为速率常数,下列说法正确的是
①Cl2(g)
 2Cl·(g) 快
2Cl·(g) 快②CO(g)+Cl·(g)
 COCl·(g) 快
COCl·(g) 快③COCl·(g)+Cl2(g)
 COCl2(g)+Cl·(g) 慢
COCl2(g)+Cl·(g) 慢其中反应②存在v正=k正c(CO)c(Cl·)、v逆=k逆c(COCl·)k为速率常数,下列说法正确的是
A.反应②的平衡常数K= |
| B.反应①的活化能大于反应③的 |
| C.要提高合成COCl2的速率,关键是提高反应①的速率 |
| D.选择合适的催化剂能加快该反应的速率,并提高COCl2的平衡产率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验过程可以达到实验目的的是
| 实验目的 | 实验过程 | |
| A | 检验 和浓硫酸反应之后是否有酸剩余 和浓硫酸反应之后是否有酸剩余 | 取少量反应后的溶液于试管中,依次加入水、 ,观察是否有沉淀生成 ,观察是否有沉淀生成 |
| B | 探究 氧化性比 氧化性比 强 强 | 向 溶液中滴入 溶液中滴入 溶液中观察是否产生气体 溶液中观察是否产生气体 |
| C | 探究淀粉水解产物葡萄糖 | 在试管中加入2 淀粉溶液和少量唾液淀粉酶,温水浴3~5 淀粉溶液和少量唾液淀粉酶,温水浴3~5 ,冷却后加入少量新制 ,冷却后加入少量新制 浊液,加热后观察是否出现砖红色沉淀 浊液,加热后观察是否出现砖红色沉淀 |
| D | 探究乙酰水杨酸样品中是否含有聚合物 | 取少量样品,加入适量 溶液,观察是否有不溶性物质 溶液,观察是否有不溶性物质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】过碳酸钠2Na2CO3·3H2O2,外观为白色结晶,主要用作漂白剂和氧化剂,以及作去污剂、清洗剂、杀菌剂。生产过程的主反应方程式:2Na2CO3+3H2O2=2Na2CO3·3H2O2,下列说法不正确 的是
| A.过碳酸钠具有强氧化性 |
| B.生产过程中采用较低温度,目的是防止产品及反应物的分解 |
| C.在生产过程中酸、铁盐、铜盐等都可能导致产率下降 |
| D.将过碳酸钠溶液和亚硫酸氢钠溶液混合,发生的反应为2Na2CO3·3H2O2 + 3NaHSO3=2Na2CO3 + 3NaHSO4 +3H2O |
您最近一年使用:0次



