Burns和Dainton研究发现Cl2与CO合成COCl2的反应机理如下:
①Cl2(g) 2Cl·(g) 快
2Cl·(g) 快
②CO(g)+Cl·(g) COCl·(g) 快
COCl·(g) 快
③COCl·(g)+Cl2(g) COCl2(g)+Cl·(g) 慢
COCl2(g)+Cl·(g) 慢
其中反应②存在v正=k正c(CO)c(Cl·)、v逆=k逆c(COCl·)k为速率常数,下列说法正确的是
①Cl2(g)
 2Cl·(g) 快
2Cl·(g) 快②CO(g)+Cl·(g)
 COCl·(g) 快
COCl·(g) 快③COCl·(g)+Cl2(g)
 COCl2(g)+Cl·(g) 慢
COCl2(g)+Cl·(g) 慢其中反应②存在v正=k正c(CO)c(Cl·)、v逆=k逆c(COCl·)k为速率常数,下列说法正确的是
A.反应②的平衡常数K= |
| B.反应①的活化能大于反应③的 |
| C.要提高合成COCl2的速率,关键是提高反应①的速率 |
| D.选择合适的催化剂能加快该反应的速率,并提高COCl2的平衡产率 |
22-23高三上·广东梅州·阶段练习 查看更多[4]
广东省梅州市蕉岭县蕉岭中学2022-2023学年高三上学期高二第二次质检化学试题(已下线)专题12 化学反应机理(练)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(选择题1-5)江西省宜春市宜丰中学2022-2023学年高三上学期1月期末考试化学试题
更新时间:2022/11/26 16:42:52
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】如图所示是25℃时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是


| A.该反应为放热反应 |
| B.b曲线是表示加入了催化剂时的能量变化曲线 |
| C.加入催化剂,增加了反应的热效应 |
| D.反应开始通入1 mol N2和3 mol H2,反应后放出的热量一定为92kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:CH4(g)+ O2(g)=CH3OH(g) △H。CH4、O2和H2O(g)(H2O的作用是活化催化剂)按照一定体积比在催化剂表面合成甲醇反应的部分历程如下图所示(吸附在催化剂表面的物种用*标注,TS代表过渡态)。下列说法正确的是
O2(g)=CH3OH(g) △H。CH4、O2和H2O(g)(H2O的作用是活化催化剂)按照一定体积比在催化剂表面合成甲醇反应的部分历程如下图所示(吸附在催化剂表面的物种用*标注,TS代表过渡态)。下列说法正确的是

 O2(g)=CH3OH(g) △H。CH4、O2和H2O(g)(H2O的作用是活化催化剂)按照一定体积比在催化剂表面合成甲醇反应的部分历程如下图所示(吸附在催化剂表面的物种用*标注,TS代表过渡态)。下列说法正确的是
O2(g)=CH3OH(g) △H。CH4、O2和H2O(g)(H2O的作用是活化催化剂)按照一定体积比在催化剂表面合成甲醇反应的部分历程如下图所示(吸附在催化剂表面的物种用*标注,TS代表过渡态)。下列说法正确的是
| A.该反应的△H=-32.51kJ/mol |
| B.在催化剂表面上更容易被吸附的是O2 |
| C.该历程中正反应最大的活化能为21.22kJ/mol |
| D.决定反应速率步骤(慢反应)的化学方程式为:*CH4+*OH+*H=*CH3OH+2*H |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】各可逆反应达平衡后,改变反应条件,其变化趋势正确的是
A.CH3COOH CH3COO-+H+(忽略溶液体积变化) CH3COO-+H+(忽略溶液体积变化)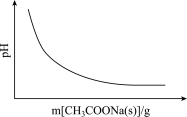 |
B.FeCl3+3KSCN Fe(SCN)3+3KCl(忽略溶液体积变化) Fe(SCN)3+3KCl(忽略溶液体积变化)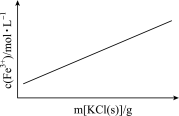 |
C.N2(g)+3H2(g)  2NH3(g)(恒温恒压) 2NH3(g)(恒温恒压) 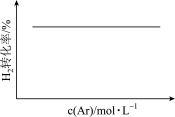 |
D.CH3OCH3(g)+3H2O(g)  6H2(g)+2CO2(g) △H>0(密闭容器,恒压) 6H2(g)+2CO2(g) △H>0(密闭容器,恒压)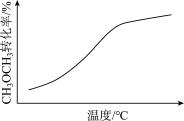 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在密闭容器中,一定量混合气体发生反应: ,达到平衡后,测得C气体的浓度为0.5mol/L。恒温下,将密闭容器的体积缩小至原体积的
,达到平衡后,测得C气体的浓度为0.5mol/L。恒温下,将密闭容器的体积缩小至原体积的 ,再达平衡时测得C气体的浓度为0.9mol/L。则下列叙述正确的是
,再达平衡时测得C气体的浓度为0.9mol/L。则下列叙述正确的是
 ,达到平衡后,测得C气体的浓度为0.5mol/L。恒温下,将密闭容器的体积缩小至原体积的
,达到平衡后,测得C气体的浓度为0.5mol/L。恒温下,将密闭容器的体积缩小至原体积的 ,再达平衡时测得C气体的浓度为0.9mol/L。则下列叙述正确的是
,再达平衡时测得C气体的浓度为0.9mol/L。则下列叙述正确的是| A.C的体积分数增大 | B.平衡向左移动 |
| C.B的转化率提高 | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列方程式不能 准确解释相应实验现象的是
A.MnO2和浓盐酸共热产生黄绿色气体: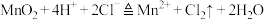 |
B.Na加入滴有酚酞的水中,溶液变红: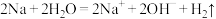 |
C.加热Fe和S的混合物生成黑色固体: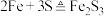 |
D.加热蓝色的CuCl2溶液,溶液变绿: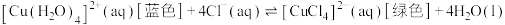 △H>0 △H>0 |
您最近一年使用:0次




