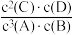在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应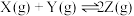
 ,一段时间后达到平衡。反应过程中测定的数据如下表:
,一段时间后达到平衡。反应过程中测定的数据如下表:
下列说法正确的是
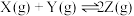
 ,一段时间后达到平衡。反应过程中测定的数据如下表:
,一段时间后达到平衡。反应过程中测定的数据如下表:| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.前4min内反应的平均速率 |
B.其他条件不变,升高温度,反应达到新平衡前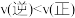 |
| C.该温度下此反应的平衡常数K=1.44 |
| D.其他条件不变,再充入0.2molZ,平衡时X的体积分数增大 |
2022·浙江金华·二模 查看更多[7]
浙江省金华十校2021-2022学年高三下学期4月模拟考试化学试题(已下线)专项12 化学反应速率与化学平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)湖南省衡阳市衡东县第一中学2022届高三下学期期中考试化学试题(已下线)专题10 化学反应速率与平衡-2023年高考化学一轮复习小题多维练(全国通用)(已下线)化学(辽宁B卷)-学易金卷:2023年高考第一次模拟考试卷黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试化学试题(已下线)黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(11-20)
更新时间:2022/04/14 17:29:48
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定温度下,把2.5molA和2.5molB混合盛入容积为2L的密闭容器里,发生如下反应:3A(g)+B(s)⇌ xC(g)+2D(g),经5s反应达平衡,在此5s内C的平均反应速率为0.2mol·L-1·s-1,同时生成1molD,下列叙述中不正确 的是
| A.反应达到平衡状态时A的转化率为60% |
| B.x=4 |
| C.若D的浓度不再变化,则该可逆反应达到化学平衡状态 |
| D.反应达到平衡状态时,相同条件下容器内气体的压强与起始时压强比为6:5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是
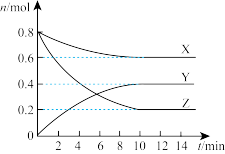
A.反应的化学方程式为: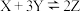 |
| B.6min时反应达到平衡状态 |
| C.X的平衡转化率为25% |
D.10min内,用Z表示的反应速率为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】某反应A(g)+B(g)→C(g)+D(g)的速率方程为v=k•cm(A)•cn(B)。其中,k为速率常数,是指给定温度下,反应物的浓度均为1 mol·L-1 时的反应速率。已知其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为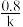 。改变反应物浓度时,反应的瞬时速率如表所示,下列说法
。改变反应物浓度时,反应的瞬时速率如表所示,下列说法不正确 的是
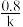 。改变反应物浓度时,反应的瞬时速率如表所示,下列说法
。改变反应物浓度时,反应的瞬时速率如表所示,下列说法| c(A)/(mol•L-1) | 0.25 | 0.50 | 1.00 | 0.50 | 1.00 | c1 |
| c(B)/(mol•L-1) | 0.050 | 0.050 | 0.100 | 0.100 | 0.200 | c2 |
| v/(10-3mol•L-1•min-1) | 1.6 | 3.2 | v1 | 3.2 | v2 | 4.8 |
| A.上述表格中的c1=0.75、v2=6.4 |
| B.该反应的速率常数k=6.4×10-3min-1 |
| C.升温、加入催化剂及缩小容积均可使k增大,反应瞬时速率加快 |
| D.在过量的B存在时,当剩余6.25%的A时,所需的时间是500min |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】反应mX(s)+nY(g) pZ(g);在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
pZ(g);在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是

 pZ(g);在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
pZ(g);在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
| A.T1>T2,P1>P2,m+n<p,ΔH<0 | B.T1<T2,P1>P2,n>p,ΔH>0 |
| C.T1>T2,P1>P2,m+n>p,ΔH>0 | D.T1>T2,P1>P2,n>p,ΔH<0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某温度下,容积一定的密闭容器中进行如下可逆反应:X(g)+Y(g) 2Z(g)+W(s)+Q,下列叙述正确的是( )
2Z(g)+W(s)+Q,下列叙述正确的是( )
 2Z(g)+W(s)+Q,下列叙述正确的是( )
2Z(g)+W(s)+Q,下列叙述正确的是( )| A.加入少量W,v(逆)增大 | B.压强不变时,反应达到平衡状态 |
| C.升高温度,v(逆)、v(正)都增大 | D.平衡后加入X,X转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某1 L恒容密闭容器中,CH4、H2O(g)的起始浓度分别为1.8 mol·L-1和3.6 mol·L-1,二者反应生成CO2和H2,该反应的部分物质的浓度随时间变化的关系如图所示(部分时间段的浓度变化未标出),其中第6 min开始升高温度。下列有关判断正确的是


| A.X是H2 |
| B.增大压强,平衡逆向移动,平衡常数减小 |
| C.第一次平衡时的平衡常数约为0.91 |
| D.若5 min时向容器中再加入0.7 mol的CH4和0.7 mol的CO2,则平衡正向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
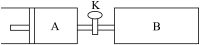
【推荐2】如图,关闭活塞K,向A中充入1molX、1molY,向B中充入2molX、2molY,此时A、B的容积都是a L。在相同温度和催化剂存在的条件下,使两容器中各自发生下述反应:X(g)+Y(g) 2Z(g)+W(g) ΔH<0。A保持恒压,B保持恒容。达平衡时,A的体积为1.4aL。下列说法错误的是
2Z(g)+W(g) ΔH<0。A保持恒压,B保持恒容。达平衡时,A的体积为1.4aL。下列说法错误的是
 2Z(g)+W(g) ΔH<0。A保持恒压,B保持恒容。达平衡时,A的体积为1.4aL。下列说法错误的是
2Z(g)+W(g) ΔH<0。A保持恒压,B保持恒容。达平衡时,A的体积为1.4aL。下列说法错误的是
| A.反应速率:v(B)>v(A) | B.A容器中X的转化率为80% |
| C.平衡时压强:2p(A)=p(B) | D.平衡时Y的体积分数:A<B |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】科学家开发新型Cu-Pd催化剂实现CO还原制备CH3COOH:2CO(g)+2H2(g)⇌CH3COOH(g)。一定温度下,向容积为2L的恒容密闭容器中充入4mol CO和3mol H2发生,上述反应,测得CH3COOH的物质的量(mol)与时间(min)的关系如表所示。
下列说法错误的是
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| n(CH3COOH)/mol | 0.00 | 0.65 | 1.00 | 1.20 | 1.30 | 1.30 |
| A.20min时,H2的正反应速率等于H2的逆反应速率 |
| B.当CO的消耗速率等于乙酸生成速率的2倍时,不能说明反应达到平衡状态 |
| C.0~10min内,v(H2)=0.05mol·L-1·min-1 |
| D.上述条件下CO的最大转化限度为65% |
您最近一年使用:0次

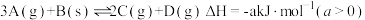 。下列说法正确的是
。下列说法正确的是