下图是s能级和p能级的原子轨道图。试回答下列问题:
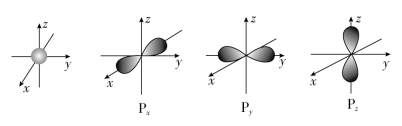
(1)s电子的原子轨道呈___________ 形,每个s能级有___________ 个原子轨道;p电子的原子轨道呈____ 形,每个p能级有___________ 个原子轨道。
(2)元素X的原子最外层电子排布式为nsnnpn+2,原子中能量最高的是___________ 电子,其电子云在空间有3个互相___________ (填“垂直”或“平行”)的伸展方向。元素X的名称是___________ ,它的氢化物中原子个数为1:1的化合物中,其σ键类型为___________ 。
(3)元素Y的原子最外层电子排布式为nsn-1npn+2,Y的元素符号为___________ ,原子的核外电子排布式为___________ 。

(1)s电子的原子轨道呈
(2)元素X的原子最外层电子排布式为nsnnpn+2,原子中能量最高的是
(3)元素Y的原子最外层电子排布式为nsn-1npn+2,Y的元素符号为
更新时间:2021-02-14 19:22:16
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】氮及其化合物在工农业生产、生活中被广泛使用,造福人类。
I.元素 X、Y、Z 位于同一周期且原子序数依次增大,它们和氢元素、硫元素组成的含氮化合物(结构如图)常用作丝绸漂白剂。回答下列问题:
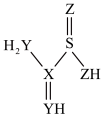
(1)硫元素在元素周期表中的位置为______ ;Y 的元素符号为______ 。
(2)下列说法错误的是______ (选填序号)。
A.原子半径:X>Y>Z
B.简单气态氢化物稳定性:Y<Z
C.该化合物可溶于水
D.该化合物中所有原子均为 8 电子稳定结构
II.工业上用氨气来制造硝酸,NH3转化关系如图所示。
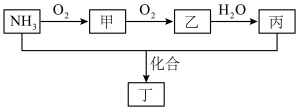
(3)NH3的电子式为______ 。
(4)图中,乙转化为丙的离子方程式为______ 。
(5)检验化合物丁中阳离子的方法:取少量待测液于试管中,______ ,将湿润的 红色石蕊试纸置于试管口,试纸变蓝。
(6)工业上常使用 NH3处理甲,生成无污染的 N2,则 NH3与甲完全反应的物质的量之比为______ 。
I.元素 X、Y、Z 位于同一周期且原子序数依次增大,它们和氢元素、硫元素组成的含氮化合物(结构如图)常用作丝绸漂白剂。回答下列问题:

(1)硫元素在元素周期表中的位置为
(2)下列说法错误的是
A.原子半径:X>Y>Z
B.简单气态氢化物稳定性:Y<Z
C.该化合物可溶于水
D.该化合物中所有原子均为 8 电子稳定结构
II.工业上用氨气来制造硝酸,NH3转化关系如图所示。

(3)NH3的电子式为
(4)图中,乙转化为丙的离子方程式为
(5)检验化合物丁中阳离子的方法:取少量待测液于试管中,
(6)工业上常使用 NH3处理甲,生成无污染的 N2,则 NH3与甲完全反应的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】如表是元素周期表的一部分,参照元素在表中的位置,回答下列问题:
(1)上述元素最高价氧化物对应水化物中,酸性最强的是__________ (填化学式),碱性最强的是__________ (填化学式),显两性的是__________ (填名称)。
(2)气态氢化物中,最稳定的是__________ (填化学式),④⑧形成的氢化物中沸点最高的是__________ (填化学式),原因是__________________ 。
(3)④分别和①、⑥两种元素的原子按1:1组成的常见化合物的电子式分别为__________ 和_______ 。用电子式表示②和④的三原子分子的形成过程____________ 。
(4)④⑥⑦⑨的简单离子半径由大到小的顺序为__________ (用离子符号和“>”表示)。
(5)⑥和⑦的最高价氧化物对应水化物之间发生反应的化学方程式___________ 。
(6)为了证明⑥和⑦两种元素的金属性强弱,下列说法或实验能提供证据的是______ 。
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
主族 周期 | IA | IIA | IIA | IVA | VA | VIA | VIIA | 0族 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)气态氢化物中,最稳定的是
(3)④分别和①、⑥两种元素的原子按1:1组成的常见化合物的电子式分别为
(4)④⑥⑦⑨的简单离子半径由大到小的顺序为
(5)⑥和⑦的最高价氧化物对应水化物之间发生反应的化学方程式
(6)为了证明⑥和⑦两种元素的金属性强弱,下列说法或实验能提供证据的是
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】在元素周期表中处于相邻位置的元素在结构和性质上有许多相似的地方。第二周期的碳、氮、氧、氟都可以形成氢化物,氧元素的氢化物除H2O外,还有H2O2;碳元素的氢化物除CH4外,还有C2H6等;与之相似的氮元素的氢化物除外,还有N2H4等。
(1)碳原子之间可以结合成链状结构,氮原子之间也可以形成链状结构,假设氮原子间只以氮氮单键形式连接成链状,并形成氢化物,则该系列氢化物的通式为_________ 。
(2)该系列中的N2H4是“神六”发射时火箭所用的液体燃料,液态的四氧化二氮作氧化剂,此液态燃料的优点是产生的能量大且无污染。已知40g N2H4在火箭发射时反应中放出710kJ热量,写出火箭发射时该反应的热化学方程式:__________________ 。
(3)该系列物中的NH 对农业、化学、国防工业具有重要意义。其合成原理为:N2(g)+3H2(g)
对农业、化学、国防工业具有重要意义。其合成原理为:N2(g)+3H2(g) 2NH3(g) ∆H=-92kJ/mol
2NH3(g) ∆H=-92kJ/mol
I.在一定温度下,将1.5molN 和6 molH
和6 molH 通入到一个固定容积为VL的密闭容器中,当反应达到平衡时,容器内气体的压强为起始时的80%,则此时反应放出的热量为
通入到一个固定容积为VL的密闭容器中,当反应达到平衡时,容器内气体的压强为起始时的80%,则此时反应放出的热量为______ kJ,H 的转化率=
的转化率=_______ 。该温度下合成氨反应的平衡常数 =
=_______ (只列数字表达式)
II.在保持温度不变,相同体积的密闭容器中,将起始的物质的量改为amolN 、bmolH
、bmolH 、cmolNH
、cmolNH ,平衡时NH
,平衡时NH 的物质的量分数为25%,则达到平衡时,I和II放出的热量
的物质的量分数为25%,则达到平衡时,I和II放出的热量_______ (填字母代号)
I和II合成氨的平衡常数分别为 和
和 ,同
,同
___  (填“﹥”、“﹤”或“=”),欲使开始时反应正向进行,a的取值范围为
(填“﹥”、“﹤”或“=”),欲使开始时反应正向进行,a的取值范围为______ 。
(1)碳原子之间可以结合成链状结构,氮原子之间也可以形成链状结构,假设氮原子间只以氮氮单键形式连接成链状,并形成氢化物,则该系列氢化物的通式为
(2)该系列中的N2H4是“神六”发射时火箭所用的液体燃料,液态的四氧化二氮作氧化剂,此液态燃料的优点是产生的能量大且无污染。已知40g N2H4在火箭发射时反应中放出710kJ热量,写出火箭发射时该反应的热化学方程式:
(3)该系列物中的NH
 对农业、化学、国防工业具有重要意义。其合成原理为:N2(g)+3H2(g)
对农业、化学、国防工业具有重要意义。其合成原理为:N2(g)+3H2(g) 2NH3(g) ∆H=-92kJ/mol
2NH3(g) ∆H=-92kJ/molI.在一定温度下,将1.5molN
 和6 molH
和6 molH 通入到一个固定容积为VL的密闭容器中,当反应达到平衡时,容器内气体的压强为起始时的80%,则此时反应放出的热量为
通入到一个固定容积为VL的密闭容器中,当反应达到平衡时,容器内气体的压强为起始时的80%,则此时反应放出的热量为 的转化率=
的转化率= =
=II.在保持温度不变,相同体积的密闭容器中,将起始的物质的量改为amolN
 、bmolH
、bmolH 、cmolNH
、cmolNH ,平衡时NH
,平衡时NH 的物质的量分数为25%,则达到平衡时,I和II放出的热量
的物质的量分数为25%,则达到平衡时,I和II放出的热量| A.一定相等 |
| B.前者一定小于后者 |
| C.前者等于或小于后者 |
| D.前者等于或大于后者 |
I和II合成氨的平衡常数分别为
 和
和 ,同
,同
 (填“﹥”、“﹤”或“=”),欲使开始时反应正向进行,a的取值范围为
(填“﹥”、“﹤”或“=”),欲使开始时反应正向进行,a的取值范围为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】I.回答下列问题:
(1)Cd与Zn同族且相邻,写出基态Cd原子的价层电子排布式:______ 。
(2)基态C原子中电子占据最高能级的符号是______ ,核外电子的空间运动状态有_____ 种,成对电子数与未成对电子数之比为_____ 。
(3)Mn在周期表中的位置为______ ,其基态原子价层电子轨道表示式为______ 。
II.有六种前四周期元素U、V、W、X、Y、Z,其原子序数依次增大,其部分信息如表所示。请用相应的化学用语回答下列问题:
(4)V、X分别与U形成的简单氢化物的稳定大的是_____ (填化学式);基态Z原子的电子排布式为______ 。
(5)U、V、W三种元素中第一电离能最大的是_____ (填物质名称)。
(6)U、V、W、X、Y、Z六种元素位于周期表中d区的元素是______ (填元素符号,下同);Y(VW3)2中各元素的电负性由大到小的顺序为______ 。
(1)Cd与Zn同族且相邻,写出基态Cd原子的价层电子排布式:
(2)基态C原子中电子占据最高能级的符号是
(3)Mn在周期表中的位置为
II.有六种前四周期元素U、V、W、X、Y、Z,其原子序数依次增大,其部分信息如表所示。请用相应的化学用语回答下列问题:
| U | 原子核外电子只存在一种运动状态 |
| V | 简单氢化物能与最高价氧化物对应的水合物反应生成盐 |
| W | 基态原子的价电子排布为nsnnp2n |
| X | 有同素异形体,其中白色单质需要保存在水中 |
| Y | 主族金属元素;各能层s能级上电子总数与各能层p能级上电子总数之比为2:3 |
| Z | 前四周期的基态原子中核外未成对电子数最多 |
(5)U、V、W三种元素中第一电离能最大的是
(6)U、V、W、X、Y、Z六种元素位于周期表中d区的元素是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】[化学——选修3:物质结构与性质]

根据下列五种
| 元素代号 | I1 | I2 | I3 | I4 | I5 |
| Q | 800.6 | 2427.1 | 3659.7 | 25025.8 | 32826.7 |
| R | 495.8 | 4562 | 6910.3 | 9543 | 13354 |
| S | 577.5 | 1816.7 | 2744.8 | 11577 | 14842 |
| T | 1402.3 | 2856 | 4578.1 | 7475.0 | 9444.9 |
| U | 2080.7 | 3952.3 | 6122 | 9371 | 12177 |
(1)在这五种元素中,最可能处于同一族的两种元素是
(2)基态Q元素原子的价电子排布式是
(3)化合物RT3中化学键类型为
(4)下列元素中,化学性质和物理性质最像U元素的是
A.硼 B.铍 C.锂 D.氦 E.碳
(5)R的某种氧化物X晶胞结构如图所示,晶胞参数a=0.566 nm,X的化学式为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有五种元素,其中A、B、C为短周期主族元素,D、E为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)已知 为离子化合物,写出其电子式:
为离子化合物,写出其电子式:_______ 。
(2)B元素基态原子中能量最高的电子的电子云在空间有_______ 个伸展方向,原子轨道呈_______ 形。
(3)某同学根据上述信息,推断C基态原子的轨道表示式为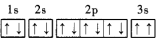 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了_______ 。
(4)E位于第_______ 族、_______ 区,该元素原子的核外电子排布式为_______ 。
(5)检验D元素的方法是_______ ,请用原子结构的知识解释产生此现象的原因:_______ 。
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
C元素的第一至第四电离能如下: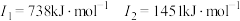 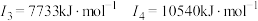 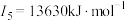 |
| D是前四周期中电负性最小的元素 |
| E在周期表的第七列 |
 为离子化合物,写出其电子式:
为离子化合物,写出其电子式:(2)B元素基态原子中能量最高的电子的电子云在空间有
(3)某同学根据上述信息,推断C基态原子的轨道表示式为
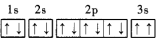 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了(4)E位于第
(5)检验D元素的方法是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】硒( Se )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(AIE)效应以来,AIE 在发光材料、生物医学等领域引起广泛关注。一种含 Se 的新型 AIE 分子Ⅳ的合成路线如下:
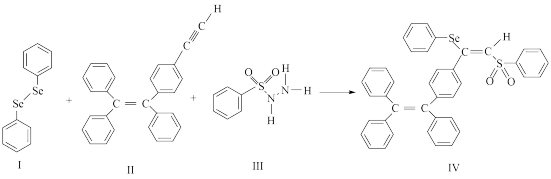
(1)Se 与 S 同族,基态硒原子价电子排布式为___________ 。
(2)H2Se 的键角___________ H2O 的键角(填:大于、小于或等于);H2Se 的沸点低于 H2O,其原因是___________ 。
(3)关于Ⅰ~Ⅲ三种反应物,下列说法正确的有___________ 。
A.Ⅰ中仅有键 B.Ⅰ中的 Se-Se 键为非极性共价键
C.Ⅱ易溶于水 D.Ⅱ中原子的杂化轨道类型只有 sp 与 sp2
E.Ⅰ~Ⅲ含有的元素中,O 电负性最大
(4)Ⅳ中具有孤对电子的原子有___________ 。
(5)硒的两种含氧酸的酸性强弱为 H2SeO4___________ H2SeO3(填“>”或“<”)。研究发现,给小鼠喂食适量 Na2SeO4 可减轻重金属铊引起的中毒。  的立体构型为
的立体构型为___________ 。
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物 X 是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图 1,沿 x、y、z 轴方向的投影均为图 2。
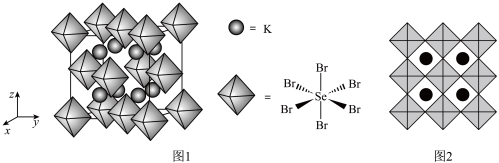
①X 的化学式为___________ 。
②设 X 的最简式的式量为 Mr,晶体密度为g / cm3 ,则 X 中相邻 K 之间的最短距离为___________ pm(10-12m)(列出计算式,NA 为阿伏加德罗常数的值)。

(1)Se 与 S 同族,基态硒原子价电子排布式为
(2)H2Se 的键角
(3)关于Ⅰ~Ⅲ三种反应物,下列说法正确的有
A.Ⅰ中仅有键 B.Ⅰ中的 Se-Se 键为非极性共价键
C.Ⅱ易溶于水 D.Ⅱ中原子的杂化轨道类型只有 sp 与 sp2
E.Ⅰ~Ⅲ含有的元素中,O 电负性最大
(4)Ⅳ中具有孤对电子的原子有
(5)硒的两种含氧酸的酸性强弱为 H2SeO4
 的立体构型为
的立体构型为(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物 X 是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图 1,沿 x、y、z 轴方向的投影均为图 2。

①X 的化学式为
②设 X 的最简式的式量为 Mr,晶体密度为g / cm3 ,则 X 中相邻 K 之间的最短距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】常见的太阳能电池有硅太阳能电池、镓(Ga)砷(As)太阳能电池及铜铟镓硒薄膜太阳能电池等。下列有关它们的化合物的问题,请回答:
(1)基态Ga原子的电子排布式为_______ ;H2O的沸点高于 H2Se的沸点(-42℃),其原因是_______ 。
(2)Na3AsO4中阴离子的空间构型为_______ ,As 原子采取_______ 杂化。
(3)晶体Si、SiC都属于原子晶体,请写出它们的熔点从高到低的顺序排列_______ 。
(4)银与铜位于同一副族。氟化银具有氯化钠型结构,其中的阴离子采用面心立方最密堆积方式,氯化钠的晶胞结构如图所示。则 Ag+周围等距离且最近的F-在空间围成的几何构型为_______ ,已知氟化银的密度为 dg·cm-3,则氟化银晶胞的晶胞参数为_______ nm(不必简化)。

(1)基态Ga原子的电子排布式为
(2)Na3AsO4中阴离子的空间构型为
(3)晶体Si、SiC都属于原子晶体,请写出它们的熔点从高到低的顺序排列
(4)银与铜位于同一副族。氟化银具有氯化钠型结构,其中的阴离子采用面心立方最密堆积方式,氯化钠的晶胞结构如图所示。则 Ag+周围等距离且最近的F-在空间围成的几何构型为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】向硫酸铜溶液中逐滴滴加浓氨水,先出现现象a,继续滴加浓氨水,现象a逐渐消失,得到一种含二价阳离子的深蓝色透明溶液,继续加入乙醇,析出深蓝色的晶体[Cu(NH3)4]SO4•H2O.这种二价阳离子的立体结构如图所示(4个NH3与Cu2+共面,跟H2O-Cu2+-H2O轴线垂直)。请回答以下问题:
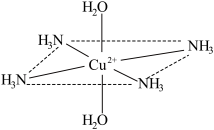
(1)基态Cu原子的价电子轨道表示式__ 。
(2)硫酸铜水溶液滴加浓氨水的变化过程,现象a是__ ;写出生成深蓝色透明溶液的离子方程式: __ 。
(3)NH3与Cu2+可形成[Cu(NH3)4]2+配离子。已知NF3与NH3具有相同的空间构型,但NF3不易与Cu2+形成配离子,其原因是__ 。
(4)请在二价阳离子的立体结构图中用“→”表示出其中的配位键__ 。
(5)已知高温下CuO→Cu2O+O2,从铜原子价层电子结构变化角度来看,能生成Cu2O的原因是__ 。

(1)基态Cu原子的价电子轨道表示式
(2)硫酸铜水溶液滴加浓氨水的变化过程,现象a是
(3)NH3与Cu2+可形成[Cu(NH3)4]2+配离子。已知NF3与NH3具有相同的空间构型,但NF3不易与Cu2+形成配离子,其原因是
(4)请在二价阳离子的立体结构图中用“→”表示出其中的配位键
(5)已知高温下CuO→Cu2O+O2,从铜原子价层电子结构变化角度来看,能生成Cu2O的原因是
您最近一年使用:0次



