为纪念元素周期表诞生 150 周年,IUPAC 等从世界范围征集优秀青年化学家为化学元素代言,我国有8 位化学家成为硫(S)等元素的代言人。回答下列问题:
(1)S 在周期表中的位置是___________
(2)下列有关性质的比较,能用元素周期律解释的是___________ (填字母序号)
a.非金属性:O>S b.离子半径:S2->Cl- c.酸性:H2SO4>H2SO3 d.酸性:H2SO4>H3PO4
(3)Se 与 S 位于同一主族,二者氢化物稳定性较强的是:___________ (用化学式表示),用原子结构解释原因___________
(4)某同学用如下装置探究不同价态硫元素之间的转化。培养皿中 A、B、C 三个塑料瓶盖内盛有不同物质。向 Na2SO3 固体上滴加 70%硫酸,迅速用玻璃片将培养皿盖严,实验记录如下。
能够说明硫元素由+4 价转化为+6 价的证据是___________
(1)S 在周期表中的位置是
(2)下列有关性质的比较,能用元素周期律解释的是
a.非金属性:O>S b.离子半径:S2->Cl- c.酸性:H2SO4>H2SO3 d.酸性:H2SO4>H3PO4
(3)Se 与 S 位于同一主族,二者氢化物稳定性较强的是:
(4)某同学用如下装置探究不同价态硫元素之间的转化。培养皿中 A、B、C 三个塑料瓶盖内盛有不同物质。向 Na2SO3 固体上滴加 70%硫酸,迅速用玻璃片将培养皿盖严,实验记录如下。
| 实验装置 | 瓶盖 | 物质 | 实验现象 |
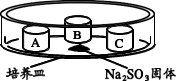 | A | 蘸有品红溶液的棉花 | 品红溶液褪色 |
| B | HCl、BaCl2 的混合溶液 | 无明显变化 | |
| C | HCl、BaCl2、FeCl3 的混合溶液 | 产生白色沉淀 |
能够说明硫元素由+4 价转化为+6 价的证据是
更新时间:2021-02-21 00:02:13
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】下表是元素周期表的一部分,请回答有关问题:
(1)最活泼的非金属元素是________ (用元素符号或化学式表示,下同);碱性最强的是________ ,该物质存在的化学键类型是_________
(2)⑤元素与⑧元素形成化合物的电子式是_______________________
(3)③⑦⑧三种元素原子半径由小到大的顺序是____________________
(4)将⑤⑥两种单质用导线相连后,同时浸入稀硫酸中,⑥这一极发生________ (填“氧化”或“还原”)反应
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)最活泼的非金属元素是
(2)⑤元素与⑧元素形成化合物的电子式是
(3)③⑦⑧三种元素原子半径由小到大的顺序是
(4)将⑤⑥两种单质用导线相连后,同时浸入稀硫酸中,⑥这一极发生
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】把与下列元素有关性质相符的曲线标号填入相应空格中:
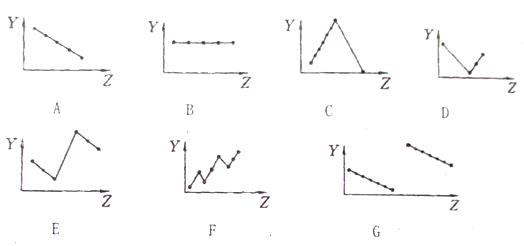
(1)第IIA族元素的价电子数_________ ;
(2)第三周期元素的最高化合价有_______ ;
(3)碱金属单质熔点_______ ;
(4)第三周期离子Na+、Mg2+、A13+、P3-、S2-、Cl-的离子半径_______ ;
(5)第二、三周期元素随原子序数递增原子半径的变化_______ 。

(1)第IIA族元素的价电子数
(2)第三周期元素的最高化合价有
(3)碱金属单质熔点
(4)第三周期离子Na+、Mg2+、A13+、P3-、S2-、Cl-的离子半径
(5)第二、三周期元素随原子序数递增原子半径的变化
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】超重元素的假设预言自然界中可能存在114号的稳定同位素X,请根据原子结构理论和元素周期律预测:
(1)X元素位于周期表中第____ 周期,_____ 族,为_____ 元素(金属或非金属)
(2)写出其最高价氧化物及其水化物的化学式分别为___________ 、__________ ,并估计后者为________ 性(填“酸”或“碱”)
(1)X元素位于周期表中第
(2)写出其最高价氧化物及其水化物的化学式分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素周期表的中元素原子结构与性质的关系
(1)同周期(从左到右)元素性质的递变规律
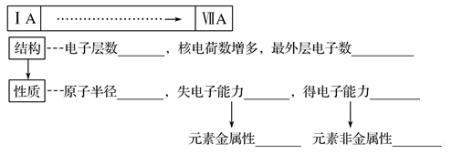
_____ ,_____ ,_____ ,_____ ,_____ ,_____ ,_____ 。
(2)同主族(自上而下)元素性质的递变规律
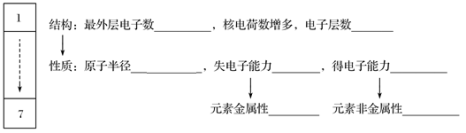
_____ ,_____ ,_____ ,_____ ,_____ ,_____ ,_____ 。
(1)同周期(从左到右)元素性质的递变规律

(2)同主族(自上而下)元素性质的递变规律

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ. 由中科院等离子体物理研究所自主研制的全超导托卡马克实验装置(俗称“人造太阳”)正在接受技术升级。人造太阳是利用氘、氚核聚变反应释放巨大能量原理而实现的。下列说法正确的是________ 。
A.氕、氘、氚三种元素在周期表中的位置不同
B.20 g D2O含有的中子数为6.02×1024个
C.在隔绝空气和高温下LiCl与金属钠反应可获得金属锂
Ⅱ. 部分元素在周期表中的位置如下:
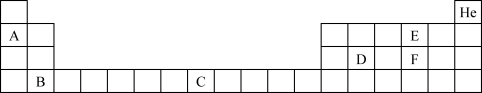
请回答下列问题:
(1)元素C在周期表中的位置为________ 。
(2)判断E和F对应的简单氢化物沸点高低,并解释原因____________ 。
(3)用电子式表示F的氢化物的形成过程:___________ 。
Ⅲ.溴及其化合物广泛用于医药、塑料阻燃剂等,苦卤提溴的工业流程如下:
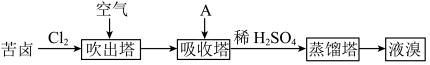
(1)结合元素周期律解释Cl的非金属性强于Br的原因:_______________ 。
(2)吸收塔中,A吸收了Br2后的溶液中含有Br−和BrO3−,则A是________ (填序号)。
A.NaCl溶液 B.Na2CO3溶液 C.SO2气体
(3)从吸收塔出来的溶液中加入稀H2SO4得到Br2的离子方程式是______ 。
A.氕、氘、氚三种元素在周期表中的位置不同
B.20 g D2O含有的中子数为6.02×1024个
C.在隔绝空气和高温下LiCl与金属钠反应可获得金属锂
Ⅱ. 部分元素在周期表中的位置如下:

请回答下列问题:
(1)元素C在周期表中的位置为
(2)判断E和F对应的简单氢化物沸点高低,并解释原因
(3)用电子式表示F的氢化物的形成过程:
Ⅲ.溴及其化合物广泛用于医药、塑料阻燃剂等,苦卤提溴的工业流程如下:

(1)结合元素周期律解释Cl的非金属性强于Br的原因:
(2)吸收塔中,A吸收了Br2后的溶液中含有Br−和BrO3−,则A是
A.NaCl溶液 B.Na2CO3溶液 C.SO2气体
(3)从吸收塔出来的溶液中加入稀H2SO4得到Br2的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】元素周期表的形式多种多样,如图是扇形元素周期表的一部分,对比中学常见元素周期表,思考扇形元素周期表的填充规律,回答下列问题:
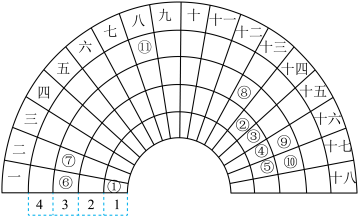
(1)写出⑪在长式周期表中的位置______________ 。
(2)在①~⑪元素中,金属性最强的是___ ,在元素④⑥⑨形成的简单离子半径由小到大的顺序是____ (用离子符号表示)。
(3)①~⑪中元素最高价氧化物对应水化物中酸性最强的是_____________ (填化学式)。写出⑥和⑧的最高价氧化物对应水化物反应的离子方程式______________________________ 。
(4)用电子式表示⑦和⑩形成的化合物的过程______________________________________ 。
(5)表中元素④和⑥可以形成一种淡黄色物质X,0.1 mol X与水反应转移电子数为______ 。
(6)表中元素③和⑤可形成一种相对分子质量为66的共价化合物Y,Y分子中各原子均达到8电子稳定结构,Y的电子式_________________________________ 。

(1)写出⑪在长式周期表中的位置
(2)在①~⑪元素中,金属性最强的是
(3)①~⑪中元素最高价氧化物对应水化物中酸性最强的是
(4)用电子式表示⑦和⑩形成的化合物的过程
(5)表中元素④和⑥可以形成一种淡黄色物质X,0.1 mol X与水反应转移电子数为
(6)表中元素③和⑤可形成一种相对分子质量为66的共价化合物Y,Y分子中各原子均达到8电子稳定结构,Y的电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】元素在周期表中的位置,反映了元素的原子结构和元素的性质。如图是元素周期表的一部分。

(1)N在元素周期表中的位置为第________ 周期第________ 族。根据元素周期律,预测酸性强弱:H3AsO4_______ H3PO4(填“>”或“<”)。
(2)在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的程度比S与H2反应程度__________ (填“更大”、“更小”或“相同”)。
(3)Br2具有较强的氧化性,将适量溴水加入KI-淀粉溶液中,出现的现象为____________________ ,发生的离子方程式为_________________________________ ;

(1)N在元素周期表中的位置为第
(2)在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度),请判断:在相同条件下Se与H2反应的程度比S与H2反应程度
(3)Br2具有较强的氧化性,将适量溴水加入KI-淀粉溶液中,出现的现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白(填写序号不得分):
(1)⑦元素的离子半径__ S2-(填“>”或“<”),比较③与⑥的氢化物,___ 更稳定(填化学式),最不活泼的元素是___ (填元素符号)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是____ ,碱性最强的化合物的化学式是:_____ 。
(3)比较①与⑤的最高价氧化物对应的水化物,_____ 的酸性强(填化学式),能证明两者酸性强弱的离子反应方程式为______
(4)实验室制取②的氢化物的化学方程式________
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(1)⑦元素的离子半径
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)比较①与⑤的最高价氧化物对应的水化物,
(4)实验室制取②的氢化物的化学方程式
您最近一年使用:0次



