元素周期表的第三周期元素,从左到右(稀有气体除外).
(1)原子半径逐渐_______ ,元素的金属性逐渐________ ,非金属性逐渐________ 。
(2)该周期元素中,除稀有气体外,原子半径最大的是______ 。(以下都填元素符号)
(3)其最高价氧化物对应的水化物碱性最强的元素是_________ 。
(4)其最高价氧化物对应的水化物呈两性的元素是__________ 。
(5)其最高价氧化物对应的水化物酸性最强的元素是_________ 。
(1)原子半径逐渐
(2)该周期元素中,除稀有气体外,原子半径最大的是
(3)其最高价氧化物对应的水化物碱性最强的元素是
(4)其最高价氧化物对应的水化物呈两性的元素是
(5)其最高价氧化物对应的水化物酸性最强的元素是
更新时间:2019-06-11 14:58:37
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】U、V、W、X、Y、Z是原子序数依次增大的短周期元素。已知:
①WU4++XU-=WU3+U2X,各种反应物和生成物的电子总数都与Y+相等;
②Z的单质在X2中燃烧的产物可使品红溶液褪色;
③V的单质在X2中燃烧可生成VX和VX2两种气体;
④Y的单质是一种金属,该金属与X2反应可生成Y2X和Y2X2两种固体。
请回答下列问题:
(1)V、W、X形成的10电子氢化物中,沸点最高的是___________________ (写化学式)。
(2)U2X2与FeSO4按物质的量之比1:2溶于稀硫酸中,反应的离子方程式为__________ 。
(3)常温下,向pH=11的Y2VX3溶液中加入过量石灰乳,过滤后所得溶液pH=13,则反应前的溶液中与反应后的滤液中水电离出的c(OH-)的比值是______________________ 。

(4)已知由U、W两种元素组成的共价化合物联氨的球棍模型如图所示,则联氨分子的电子式为____________ 。联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为_______ (已知:N2H4+H+=N2H5+的K=8.7×107;Kw=1.0×10-14)。联氨与过量硫酸形成的酸式盐的化学式为______________ 。
①WU4++XU-=WU3+U2X,各种反应物和生成物的电子总数都与Y+相等;
②Z的单质在X2中燃烧的产物可使品红溶液褪色;
③V的单质在X2中燃烧可生成VX和VX2两种气体;
④Y的单质是一种金属,该金属与X2反应可生成Y2X和Y2X2两种固体。
请回答下列问题:
(1)V、W、X形成的10电子氢化物中,沸点最高的是
(2)U2X2与FeSO4按物质的量之比1:2溶于稀硫酸中,反应的离子方程式为
(3)常温下,向pH=11的Y2VX3溶液中加入过量石灰乳,过滤后所得溶液pH=13,则反应前的溶液中与反应后的滤液中水电离出的c(OH-)的比值是

(4)已知由U、W两种元素组成的共价化合物联氨的球棍模型如图所示,则联氨分子的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】有X、Y、Z三种元素,它们的单质在常温、常压下皆为气体。W单质为固体。
①X单质可在Z单质中燃烧生成XZ,其火焰为苍白色;W单质在Y单质中剧烈燃烧产生黄色火焰,生成淡黄色固体A。
②每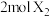 可与
可与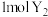 化合生成
化合生成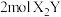 ,
, 在常温下为液体。
在常温下为液体。
③化合物XZ的水溶液可使蓝色石蕊试纸变红;W与水反应后的溶液可使无色酚酞试液变红。
④Z单质溶于化合物 ,所得溶液具有漂白作用;请回答:
,所得溶液具有漂白作用;请回答:
(1)画出W原子的原子结构示意图________________ 。
(2)写出固体A的化学式________________ 。
(3)Z单质与 化学反应方程式:
化学反应方程式:________________ 。
(4)W单质与 化学反应方程式:
化学反应方程式:________________ 。
①X单质可在Z单质中燃烧生成XZ,其火焰为苍白色;W单质在Y单质中剧烈燃烧产生黄色火焰,生成淡黄色固体A。
②每
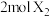 可与
可与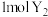 化合生成
化合生成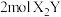 ,
, 在常温下为液体。
在常温下为液体。③化合物XZ的水溶液可使蓝色石蕊试纸变红;W与水反应后的溶液可使无色酚酞试液变红。
④Z单质溶于化合物
 ,所得溶液具有漂白作用;请回答:
,所得溶液具有漂白作用;请回答:(1)画出W原子的原子结构示意图
(2)写出固体A的化学式
(3)Z单质与
 化学反应方程式:
化学反应方程式:(4)W单质与
 化学反应方程式:
化学反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如表是元素周期表的一部分。回答下列问题:
(1)地球上99%的溴元素存在于海水中,因此溴被称为“海洋元素”。
①该表中溴在元素周期表中的位置为____________ 。
②该表中最高价氧化物对应的水化物酸性最强的是______ (填化学式),该元素形成化合物HXO的结构式为______ (X用对应元素符号表示)。
③卤素互化物(如IBr)与卤素单质性质相似。已知IBr能与水发生非氧化还原反应,写出IBr与水反应的化学方程式____________ ,IBr中含有的化学键是______ (填“离子键”、“极性键”或“非极性键”)。
(2) 溶于水形成
溶于水形成 溶液,向所得溶液中通入
溶液,向所得溶液中通入 气体,反应生成Se和
气体,反应生成Se和 。写出
。写出 与
与 反应的化学方程式
反应的化学方程式____________ 。
(3)已知某主族元素离子结构示意图为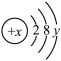 ,其中
,其中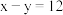 ,此元素与氯元素组成化合物的电子式为
,此元素与氯元素组成化合物的电子式为______ 。
16 S 硫 32.06 | 17 Cl 氯 35.45 |
34 Se 硒 78.96 | 35 Br 溴 79.90 |
53 I 碘 126.9 |
(1)地球上99%的溴元素存在于海水中,因此溴被称为“海洋元素”。
①该表中溴在元素周期表中的位置为
②该表中最高价氧化物对应的水化物酸性最强的是
③卤素互化物(如IBr)与卤素单质性质相似。已知IBr能与水发生非氧化还原反应,写出IBr与水反应的化学方程式
(2)
 溶于水形成
溶于水形成 溶液,向所得溶液中通入
溶液,向所得溶液中通入 气体,反应生成Se和
气体,反应生成Se和 。写出
。写出 与
与 反应的化学方程式
反应的化学方程式(3)已知某主族元素离子结构示意图为
 ,其中
,其中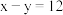 ,此元素与氯元素组成化合物的电子式为
,此元素与氯元素组成化合物的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】用元素符号(或化学式)回答原子序数从1~18的元素的有关问题
(1)与水反应最剧烈的金属是_____________ 。
(2)与水反应最剧烈的非金属是_____________
(3)硬度最大的单质是____________ 。(填名称)
(4)最高正价为+7价的元素是_____________ 。
(1)与水反应最剧烈的金属是
(2)与水反应最剧烈的非金属是
(3)硬度最大的单质是
(4)最高正价为+7价的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】用于金属焊接的某种焊条,其药皮由大理石、水泥、硅铁等配制而成。
(1)Al的原子结构示意图为____________ ;Al与NaOH溶液反应的离子方程式为____________ 。
(2)30Si的原子的中子数为________________________ 。SiO2的晶体类型为_____________ 。
(3)Al3+与Yn-的电子数相同,Y所在族各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是___________________ 。
(4)焊接过程中,药皮在高温下产生了熔渣和使金属不被氧化的气体,该气体是____________ 。
(5)经处理后的熔渣36.0 g(仅含Fe2O3、Al2O3、SiO2),加入足量稀盐酸,分离得到11.0 g固体;滤液中加入过量NaOH溶液,分离得到21.4 g固体;则此熔渣中Al2O3的质量分数为____________ 。
(1)Al的原子结构示意图为
(2)30Si的原子的中子数为
(3)Al3+与Yn-的电子数相同,Y所在族各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是
(4)焊接过程中,药皮在高温下产生了熔渣和使金属不被氧化的气体,该气体是
(5)经处理后的熔渣36.0 g(仅含Fe2O3、Al2O3、SiO2),加入足量稀盐酸,分离得到11.0 g固体;滤液中加入过量NaOH溶液,分离得到21.4 g固体;则此熔渣中Al2O3的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请用元素符号(或化学式)回答原子序数11-18的元素有关问题:
(1)除稀有气体外,原子半径最大的是________________________________ 。
(2)最高价氧化物的水化物中碱性最强的是____________________________ 。
(3)最高价氧化物的水化物中呈两性的是______________________________ 。
(4)最高价氧化物的水化物中酸性最强的是____________________________ 。
(5)气态氢化物中最稳定的是________________________________________ 。
(1)除稀有气体外,原子半径最大的是
(2)最高价氧化物的水化物中碱性最强的是
(3)最高价氧化物的水化物中呈两性的是
(4)最高价氧化物的水化物中酸性最强的是
(5)气态氢化物中最稳定的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下图是元素周期表的一部分,表中所列字母a、b、c、d、e、f、g、h分别代表某种化学元素。请依据这8种元素回答下列问题。
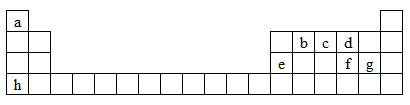
(1)上述8种元素的单质中常温下为气态,且密度最小的是______ (填化学式)。
(2)f元素的原子结构示意图为_______ 。
(3)c的最高价氧化物对应水化物的化学式为______ 。
(4)hg的电子式为_______ 。
(5)b、c、d三种元素的最简单氢化物的沸点由高到低的顺序是______ (填化学式)。
(6)元素e的单质与h的最高价氧化物对应的水化物反应的化学方程式为__________ 。
(7)f元素的最简单氢化物的水溶液显____ 性(填“酸”或“碱”),请写出该氢化物久置在空气中变质的化学方程式________ 。
(8)gd-常用作消毒剂,单质砷(As)在碱性溶液中可被gd-氧化为AsO43-,该反应的离子方程式为__________ 。

(1)上述8种元素的单质中常温下为气态,且密度最小的是
(2)f元素的原子结构示意图为
(3)c的最高价氧化物对应水化物的化学式为
(4)hg的电子式为
(5)b、c、d三种元素的最简单氢化物的沸点由高到低的顺序是
(6)元素e的单质与h的最高价氧化物对应的水化物反应的化学方程式为
(7)f元素的最简单氢化物的水溶液显
(8)gd-常用作消毒剂,单质砷(As)在碱性溶液中可被gd-氧化为AsO43-,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据你所学习的元素周期律和周期表知识回答下列相关问题:
(1)现有部分短周期元素的性质或原子结构如下表:
(i)元素Y的氢化物的电子式为____ ,其水溶液呈碱性的原因是(用电离方程式表示):____ ;
(ii)元素Z与元素T相比,非金属性较强的是___ (填元素符号);
(iii)探寻物质的性质差异性是学习的重要方法之一,T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是___ (填化学式)。
(2)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质),把与下面元素有关的性质相符的曲线标号填入相应的空格中:

(i)IIA族元素的最外层电子数(填字母)____ ;
(ii)第三周期元素的最高化合价(填字母)____ ;
(iii)N3、O2、F、Na、Mg2、Al3的离子半径(填字母)___ 。
(3)周期表中某些元素化合物的易燃性、毒性变化有一定规律性,例如:
(i)氢化物的易燃性:第二周期___ >__ >H2O>HF,第三周期SiH4>PH3>___ >___ (填化学式);
(ii)化合物的毒性:PH3>NH3,H2S___ H2O,CS2_ CO2(选填“<”、“>”或“=”)。
(1)现有部分短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| T | 单质是一种淡黄色固体,是黑火药成分之一 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(i)元素Y的氢化物的电子式为
(ii)元素Z与元素T相比,非金属性较强的是
(iii)探寻物质的性质差异性是学习的重要方法之一,T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是
(2)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质),把与下面元素有关的性质相符的曲线标号填入相应的空格中:

(i)IIA族元素的最外层电子数(填字母)
(ii)第三周期元素的最高化合价(填字母)
(iii)N3、O2、F、Na、Mg2、Al3的离子半径(填字母)
(3)周期表中某些元素化合物的易燃性、毒性变化有一定规律性,例如:
(i)氢化物的易燃性:第二周期
(ii)化合物的毒性:PH3>NH3,H2S
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,针对所给的10种元素,完成下列各小题。
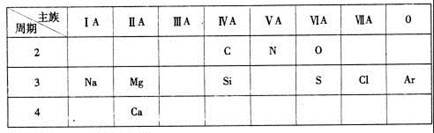
(1)第3周期中金属性最强的元素是_______ (填元素名称);
(2)S原子结构示意图为_______ ;
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是_______ (填化学式);
(4)C、N和O原子半径由小到大的顺序的是_______ ;
(5)第3周期中气态氢化物最稳定的是_______ ;
(6)Si是带来人类文明的重要元素之一,其氧化物化学式是_______ ,常用于制造_______ (填一种高性能的现代通讯材料的名称);
(7)铝是大自然赐予人类的宝物。它其中的一个用途是作为铝热剂,该反应的化学方程式为_______
(8)N元素形成的一种氢化物的化学式是_______ ,俗话说“雷雨发庄稼”,请写出二氧化氮溶于水的反应为:_______ 。

(1)第3周期中金属性最强的元素是
(2)S原子结构示意图为
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是
(4)C、N和O原子半径由小到大的顺序的是
(5)第3周期中气态氢化物最稳定的是
(6)Si是带来人类文明的重要元素之一,其氧化物化学式是
(7)铝是大自然赐予人类的宝物。它其中的一个用途是作为铝热剂,该反应的化学方程式为
(8)N元素形成的一种氢化物的化学式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,表中的每个字母代表一种短周期元素。请写下列空白:
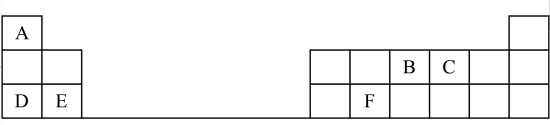
(1)A与B形成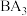 的化学式为
的化学式为___________ ;C的原子结构示意图为___________ 。
(2)B的最高价氧化物对应的水化物的化学式为___________ ;D、E的最高价氧化物对应的水化物中碱性较弱的是___________ (用化学式表示),元素C、D、E的原子半径由大到小的顺序是___________ (用元素符号表示)。
(3)E位于周期表的第三周期第___________ 族;F的氧化物与氢氧化钠溶液反应的离子方程式为___________ 。

(1)A与B形成
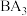 的化学式为
的化学式为(2)B的最高价氧化物对应的水化物的化学式为
(3)E位于周期表的第三周期第
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36 号元素),对 比中学常见元素周期表思考扇形元素周期表的 填充规律,并用化学用语.回答下列问题:
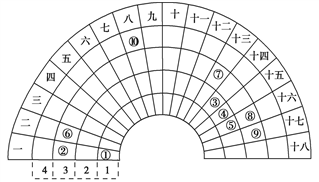
(1)若①~⑩分别代表十种元素,则⑧代表的元素在常见周期表中的位置是____________
(2)比较元素最高价氧化物对应水化物的碱性:②_____________ ⑥(填“>”或“<”)
(3)写出一种由①、④、⑤三种元素形成的常见离子化合物:___________ ,设计一个简单的实验检验其阳离子的存在:___________________ 。
(4)用电子式表示⑥、⑨形成化合物的过程:_______________ 。
(5)①、③、⑤三种元素形成的18 电子结构的化合物是近年来燃料电池研究领域的新宠,写出用它作燃料,②的最高价氧化物对应的水化物作电解质的燃料电池的负极反应式:_________ 。

(1)若①~⑩分别代表十种元素,则⑧代表的元素在常见周期表中的位置是
(2)比较元素最高价氧化物对应水化物的碱性:②
(3)写出一种由①、④、⑤三种元素形成的常见离子化合物:
(4)用电子式表示⑥、⑨形成化合物的过程:
(5)①、③、⑤三种元素形成的18 电子结构的化合物是近年来燃料电池研究领域的新宠,写出用它作燃料,②的最高价氧化物对应的水化物作电解质的燃料电池的负极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,A的单质为密度最小的气体,B、W同周期,A、D同主族,A与W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置为___ 。写出E的最高价氧化物的水化物与D的最高价氧化物的水化物反应的离子方程式___ 。
(2)由A、W元素组成的18电子分子的结构式为__ 。
(3)D的一种氧化物可与B的最高价氧化物反应生成W的单质,试写出反应的化学方程式___ 。
(4)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,DA能与水反应放氢气,若将1mol DA和1mol E单质混合加入足量的水,充分反应后生成气体的体积是___ L(标准状况下)。
(5)若要比较D和E的金属性强弱,下列实验方法可行的是__ 。
a.将D单质置于E的盐溶液中,若单质D不能置换出单质E,说明D的金属性弱
b.将少量D、E的单质分别投入到水中,若D反应而E不反应,说明D的金属性强
c.比较相同条件下D和E的最高价氧化物对应水化物的溶解性若前者比后者溶解度大,说明D的金属性强
(1)E元素在周期表中的位置为
(2)由A、W元素组成的18电子分子的结构式为
(3)D的一种氧化物可与B的最高价氧化物反应生成W的单质,试写出反应的化学方程式
(4)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,DA能与水反应放氢气,若将1mol DA和1mol E单质混合加入足量的水,充分反应后生成气体的体积是
(5)若要比较D和E的金属性强弱,下列实验方法可行的是
a.将D单质置于E的盐溶液中,若单质D不能置换出单质E,说明D的金属性弱
b.将少量D、E的单质分别投入到水中,若D反应而E不反应,说明D的金属性强
c.比较相同条件下D和E的最高价氧化物对应水化物的溶解性若前者比后者溶解度大,说明D的金属性强
您最近一年使用:0次



