用于金属焊接的某种焊条,其药皮由大理石、水泥、硅铁等配制而成。
(1)Al的原子结构示意图为____________ ;Al与NaOH溶液反应的离子方程式为____________ 。
(2)30Si的原子的中子数为________________________ 。SiO2的晶体类型为_____________ 。
(3)Al3+与Yn-的电子数相同,Y所在族各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是___________________ 。
(4)焊接过程中,药皮在高温下产生了熔渣和使金属不被氧化的气体,该气体是____________ 。
(5)经处理后的熔渣36.0 g(仅含Fe2O3、Al2O3、SiO2),加入足量稀盐酸,分离得到11.0 g固体;滤液中加入过量NaOH溶液,分离得到21.4 g固体;则此熔渣中Al2O3的质量分数为____________ 。
(1)Al的原子结构示意图为
(2)30Si的原子的中子数为
(3)Al3+与Yn-的电子数相同,Y所在族各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是
(4)焊接过程中,药皮在高温下产生了熔渣和使金属不被氧化的气体,该气体是
(5)经处理后的熔渣36.0 g(仅含Fe2O3、Al2O3、SiO2),加入足量稀盐酸,分离得到11.0 g固体;滤液中加入过量NaOH溶液,分离得到21.4 g固体;则此熔渣中Al2O3的质量分数为
更新时间:2016-12-09 11:22:07
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分:
(1)最高价氧化物对应的水化物中,碱性最强的是_______ ,酸性最强的是_______ 。
(2)f、g和h的气态氢化物的稳定性由强到弱的顺序是_______ 。
(3)研究发现,在元素周期表中左上方与右下方相邻元素也存在某些性质的相似性,这一规律通常称对角线规则或对角线相似,则与c呈对角线相似的元素是铍,元素符号是“Be”,如:Be与Al一样,也能与NaOH溶液反应,反应的化学方程式是:Be+2NaOH→Na2BeO2+H2↑。请根据以上信息,结合已学知识,尝试写出Be的最高价氧化物对应水化物与NaOH溶液反应的离子方程式:_______ 。
| 周期/族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | a | |||||||
| 2 | d | e | h | |||||
| 3 | b | c | f | g |
(1)最高价氧化物对应的水化物中,碱性最强的是
(2)f、g和h的气态氢化物的稳定性由强到弱的顺序是
(3)研究发现,在元素周期表中左上方与右下方相邻元素也存在某些性质的相似性,这一规律通常称对角线规则或对角线相似,则与c呈对角线相似的元素是铍,元素符号是“Be”,如:Be与Al一样,也能与NaOH溶液反应,反应的化学方程式是:Be+2NaOH→Na2BeO2+H2↑。请根据以上信息,结合已学知识,尝试写出Be的最高价氧化物对应水化物与NaOH溶液反应的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】磷精矿湿法制备磷酸的一种工艺流程如图所示:
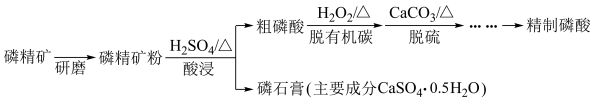
已知:磷精矿主要成分为Ca5(PO4)3(OH),还含有Ca5(PO4)3F和有机碳等。溶解度:Ca5(PO4)3(OH)<CaSO4·0.5H2O;磷精矿粉酸浸时发生反应:2Ca5(PO4)3(OH)+3H2O+10H2SO4 10CaSO4·0.5H2O+6H3PO4
10CaSO4·0.5H2O+6H3PO4
(1)该反应体现出酸性关系:H3PO4________ H2SO4(填“>”或“<”)。
(2)结合元素周期律解释(1)中结论:P和S电子层数相同,________ 。

已知:磷精矿主要成分为Ca5(PO4)3(OH),还含有Ca5(PO4)3F和有机碳等。溶解度:Ca5(PO4)3(OH)<CaSO4·0.5H2O;磷精矿粉酸浸时发生反应:2Ca5(PO4)3(OH)+3H2O+10H2SO4
 10CaSO4·0.5H2O+6H3PO4
10CaSO4·0.5H2O+6H3PO4(1)该反应体现出酸性关系:H3PO4
(2)结合元素周期律解释(1)中结论:P和S电子层数相同,
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】为纪念元素周期表诞生 150 周年,IUPAC 等从世界范围征集优秀青年化学家为化学元素代言,我国有8 位化学家成为硫(S)等元素的代言人。回答下列问题:
(1)S 在周期表中的位置是___________
(2)下列有关性质的比较,能用元素周期律解释的是___________ (填字母序号)
a.非金属性:O>S b.离子半径:S2->Cl- c.酸性:H2SO4>H2SO3 d.酸性:H2SO4>H3PO4
(3)Se 与 S 位于同一主族,二者氢化物稳定性较强的是:___________ (用化学式表示),用原子结构解释原因___________
(4)某同学用如下装置探究不同价态硫元素之间的转化。培养皿中 A、B、C 三个塑料瓶盖内盛有不同物质。向 Na2SO3 固体上滴加 70%硫酸,迅速用玻璃片将培养皿盖严,实验记录如下。
能够说明硫元素由+4 价转化为+6 价的证据是___________
(1)S 在周期表中的位置是
(2)下列有关性质的比较,能用元素周期律解释的是
a.非金属性:O>S b.离子半径:S2->Cl- c.酸性:H2SO4>H2SO3 d.酸性:H2SO4>H3PO4
(3)Se 与 S 位于同一主族,二者氢化物稳定性较强的是:
(4)某同学用如下装置探究不同价态硫元素之间的转化。培养皿中 A、B、C 三个塑料瓶盖内盛有不同物质。向 Na2SO3 固体上滴加 70%硫酸,迅速用玻璃片将培养皿盖严,实验记录如下。
| 实验装置 | 瓶盖 | 物质 | 实验现象 |
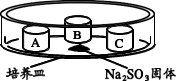 | A | 蘸有品红溶液的棉花 | 品红溶液褪色 |
| B | HCl、BaCl2 的混合溶液 | 无明显变化 | |
| C | HCl、BaCl2、FeCl3 的混合溶液 | 产生白色沉淀 |
能够说明硫元素由+4 价转化为+6 价的证据是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】硒(Se)和铬(Cr)元素都是人体必需的微量元素,请回答下列问题:
(1)硒与氧为同主族元素,属于第四周期元素,画出硒的原子结构示意图为______________ ;
(2)已知核内有48个中子的硒的同位素,下列表示该核素的符号正确的是________
(3)由硒在周期表中的位置分析判断下列说法正确的是________
(4)二硫化硒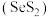 具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。
具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。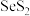 中硫元素的化合价为负价,请从元素周期律角度解释原因:
中硫元素的化合价为负价,请从元素周期律角度解释原因:_________________ 。
(5)人体内产生的活性氧能加速人体衰老,被称为“生命杀手”,化学家尝试用 及其他富硒物质清除人体内的活性氧,此时
及其他富硒物质清除人体内的活性氧,此时 表现出
表现出____________ 性。
(1)硒与氧为同主族元素,属于第四周期元素,画出硒的原子结构示意图为
(2)已知核内有48个中子的硒的同位素,下列表示该核素的符号正确的是________
A.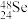 | B. | C.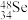 | D.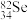 |
A.热稳定性: | B.还原性: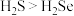 |
C.酸性: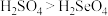 | D.原子半径: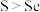 |
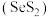 具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。
具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。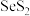 中硫元素的化合价为负价,请从元素周期律角度解释原因:
中硫元素的化合价为负价,请从元素周期律角度解释原因:(5)人体内产生的活性氧能加速人体衰老,被称为“生命杀手”,化学家尝试用
 及其他富硒物质清除人体内的活性氧,此时
及其他富硒物质清除人体内的活性氧,此时 表现出
表现出
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)已知阳离子M2+的原子核内有n个中子,M原子的质量数为A,则a克M2+中所含电子的物质的量是____ mol。
(2)向1L1mol/L的NaOH溶液中通入0.6molCO2,所得溶液中Na2CO3与NaHCO3物质的量浓度之比为____ 。
(1)已知阳离子M2+的原子核内有n个中子,M原子的质量数为A,则a克M2+中所含电子的物质的量是
(2)向1L1mol/L的NaOH溶液中通入0.6molCO2,所得溶液中Na2CO3与NaHCO3物质的量浓度之比为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求用合适的化学用语回答下列问题:
(1)写出含有8个质子、10个中子的原子化学符号___________ 。
(2)相同质量的D2O和H2O中质子数之比是___________ 。
(3)第ⅦA族上下相邻的两种元素X、Y(X在上),X元素所在周期含m,Y元素所在周期含n种元素,若X的原子序数为x,则Y的原子序数为___________ 。
(4)金属Li与氧气加热生成物质的化学式___________ 。
(5)向NaHSO4溶液中滴加Ba(OH)2溶液至溶液呈中性的离子方程式:___________ 。
(6)“洁厕灵”和“84消毒液”混合发生氯气中毒的离子方程式:___________ 。
(7)标况下,VL NH3溶于1L水中所形成的氨水的密度为dg/cm3,该溶液的物质的量浓度为___________ 。
(8)—种固体管道疏通剂的主要成分是NaOH和Al粉,试解释其疏通原理(用化学方程式回答):___________ 。
(1)写出含有8个质子、10个中子的原子化学符号
(2)相同质量的D2O和H2O中质子数之比是
(3)第ⅦA族上下相邻的两种元素X、Y(X在上),X元素所在周期含m,Y元素所在周期含n种元素,若X的原子序数为x,则Y的原子序数为
(4)金属Li与氧气加热生成物质的化学式
(5)向NaHSO4溶液中滴加Ba(OH)2溶液至溶液呈中性的离子方程式:
(6)“洁厕灵”和“84消毒液”混合发生氯气中毒的离子方程式:
(7)标况下,VL NH3溶于1L水中所形成的氨水的密度为dg/cm3,该溶液的物质的量浓度为
(8)—种固体管道疏通剂的主要成分是NaOH和Al粉,试解释其疏通原理(用化学方程式回答):
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】填空。
(1)常温下,CrO2Cl2为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是___________ (填“极性”或“非极性”)分子。
(2)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4,呈正四面体结构。Ni(CO)4易溶于下列物质中的___________ (填字母)。
a.水 b.CCl4 c.苯 d.NiSO4溶液
(3)甲醛、甲醇和甲酸等碳原子个数较少的醛、醇和羧酸均易溶于水,而甲烷、甲酸甲酯难溶于水,试解释其原因:___________ 。
(4)下列分子中若有手性分子,请用“*”标出其手性碳原子___________ ;若无手性分子,此小题不必作答。
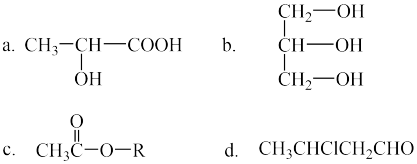
(1)常温下,CrO2Cl2为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是
(2)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4,呈正四面体结构。Ni(CO)4易溶于下列物质中的
a.水 b.CCl4 c.苯 d.NiSO4溶液
(3)甲醛、甲醇和甲酸等碳原子个数较少的醛、醇和羧酸均易溶于水,而甲烷、甲酸甲酯难溶于水,试解释其原因:
(4)下列分子中若有手性分子,请用“*”标出其手性碳原子
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】某物质可溶于水、乙醇,熔点为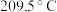 ,其结构简式如图所示,根据该物质结构回答下列问题:
,其结构简式如图所示,根据该物质结构回答下列问题:

(1) 元素在周期表的位置
元素在周期表的位置_______ , 原子的核外电子排布式为
原子的核外电子排布式为_______ , 元素位于周期表的
元素位于周期表的_______ 区。
(2)图中结构中 原子的杂化方式为
原子的杂化方式为_______ ;最外层达到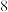 电子稳定结构的原子有
电子稳定结构的原子有_______ 个;。 键和
键和 键的个数比为
键的个数比为_______
(3)该物质的晶体类型为_______ ,该有机物可溶于水的原因是_______ 。
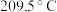 ,其结构简式如图所示,根据该物质结构回答下列问题:
,其结构简式如图所示,根据该物质结构回答下列问题:
(1)
 元素在周期表的位置
元素在周期表的位置 原子的核外电子排布式为
原子的核外电子排布式为 元素位于周期表的
元素位于周期表的(2)图中结构中
 原子的杂化方式为
原子的杂化方式为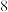 电子稳定结构的原子有
电子稳定结构的原子有 键和
键和 键的个数比为
键的个数比为(3)该物质的晶体类型为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】H与O可以形成 和
和 两种化合物。请回答:
两种化合物。请回答:
(1) 可与
可与 形成
形成 ,
, 的空间构型名称为
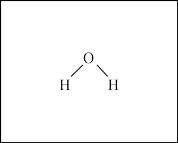
的空间构型名称为___________ 。根据 的成键特点,画出与下图中
的成键特点,画出与下图中 分子直接相连的所有氢键
分子直接相连的所有氢键_____ (用O—H…O表示)。
(2) 分子结构如图所示,
分子结构如图所示,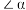 、
、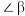 、
、 中相等的角是
中相等的角是___________ , 是
是___________ 分子(填“极性”或“非极性”)。 晶体中有4种作用力:①
晶体中有4种作用力:① 键、②
键、② 键、③范德华力、④氢键,这4种作用力由强到弱依次为:
键、③范德华力、④氢键,这4种作用力由强到弱依次为:___________ 。
(3)哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。根据以上原理,下列金属离子不能催化双氧水分解的是___________
A. B.
B. C.
C. D.
D. E.
E.
(4)实验测得,25℃时 的
的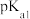 小于
小于 的
的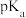 ,原因是
,原因是___________ (运用物质结构原理解释)。
 和
和 两种化合物。请回答:
两种化合物。请回答:(1)
 可与
可与 形成
形成 ,
, 的空间构型名称为
的空间构型名称为 的成键特点,画出与下图中
的成键特点,画出与下图中 分子直接相连的所有氢键
分子直接相连的所有氢键
(2)
 分子结构如图所示,
分子结构如图所示,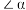 、
、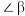 、
、 中相等的角是
中相等的角是 是
是 晶体中有4种作用力:①
晶体中有4种作用力:① 键、②
键、② 键、③范德华力、④氢键,这4种作用力由强到弱依次为:
键、③范德华力、④氢键,这4种作用力由强到弱依次为:
(3)哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。根据以上原理,下列金属离子不能催化双氧水分解的是
A.
 B.
B. C.
C. D.
D. E.
E.
(4)实验测得,25℃时
 的
的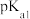 小于
小于 的
的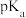 ,原因是
,原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)某学习小组研究1L某待测液,已知该待测液中除含有0.2mol•L-1的Na+外,还可能含有下列离子中的一种或几种:
现进行如图实验操作(每次实验所加试剂均过量):

①由气体B可确定待测液中含有的离子是_______ 。
②由沉淀D和沉淀E可以判断待测液中一定含有的离子是________ 。
③由白色沉淀B可确定待测液中含有的离子是________ ,请写出溶液A反应生成沉淀B的离子方程式_______ 。
④综合分析,待测液中K+的最小浓度为________ 。
(2)该小组将26.3gNiSO4•nH2O样品在900℃下煅烧,样品受热过程的热重曲线(样品质量随温度变化的曲线)如图所示。

已知:L→N时失掉全部的结晶水。请回答下列问题。
①n的值是______ 。
②固体Q的化学式为_______ 。
(1)某学习小组研究1L某待测液,已知该待测液中除含有0.2mol•L-1的Na+外,还可能含有下列离子中的一种或几种:
| 阳离子 | K+、NH 、Mg2+、Ba2+、Fe3+ 、Mg2+、Ba2+、Fe3+ |
| 阴离子 | Cl-、Br-、CO 、HCO 、HCO 、SO 、SO |

①由气体B可确定待测液中含有的离子是
②由沉淀D和沉淀E可以判断待测液中一定含有的离子是
③由白色沉淀B可确定待测液中含有的离子是
④综合分析,待测液中K+的最小浓度为
(2)该小组将26.3gNiSO4•nH2O样品在900℃下煅烧,样品受热过程的热重曲线(样品质量随温度变化的曲线)如图所示。

已知:L→N时失掉全部的结晶水。请回答下列问题。
①n的值是
②固体Q的化学式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】二氧化氯(ClO2)是一种广谱杀菌消毒剂。某工厂以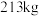
 固体、若干NaCl固体和876 kg一定溶质质量分数的稀硫酸为原料制取ClO2。反应的方程式如下:
固体、若干NaCl固体和876 kg一定溶质质量分数的稀硫酸为原料制取ClO2。反应的方程式如下: ,假设反应物均恰好完全反应。试计算:[已知:相对分子质量为
,假设反应物均恰好完全反应。试计算:[已知:相对分子质量为 106.5
106.5  142
142  98]
98]
(1)ClO2中氯、氧元素质量比为_______ (填最简整数比)。
(2)反应后所得溶液中Na2SO4的质量分数是_______ 。
(3)30℃时,将所得的硫酸钠溶液蒸发多少千克水可以恰好形成该温度下的饱和溶液_______ 。(已知:30℃时,Na2SO4的溶解度为40 g。)
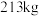
 固体、若干NaCl固体和876 kg一定溶质质量分数的稀硫酸为原料制取ClO2。反应的方程式如下:
固体、若干NaCl固体和876 kg一定溶质质量分数的稀硫酸为原料制取ClO2。反应的方程式如下: ,假设反应物均恰好完全反应。试计算:[已知:相对分子质量为
,假设反应物均恰好完全反应。试计算:[已知:相对分子质量为 106.5
106.5  142
142  98]
98](1)ClO2中氯、氧元素质量比为
(2)反应后所得溶液中Na2SO4的质量分数是
(3)30℃时,将所得的硫酸钠溶液蒸发多少千克水可以恰好形成该温度下的饱和溶液
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】以Al(OH)3、H2SO4、工业(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如右图所示:
回答下列问题:
(1)氧化步骤中发生的主要反应的离子方程式为________________ 。
(2)当25℃时,Kw=1.0×10-14,Kb(NH3·H2O)=1.75×105。(NH4)2SO4溶液呈酸性,其原因是(用力方程式解释):__________ ;该离子方程式的平衡常数K约为______ (填具体数字)。
(3)如何检验中和液中的杂质离子已完全除尽_________ 。
(4)NH4Al(SO4)2溶液与过量NaOH溶液混合加热,反应的化学方程式为__________ 。
(5)综上分析,流程图中M的主要成分的化学式为________ ,M可用一种物质吸收以实现循环利用,该物质的名称是_________ 。
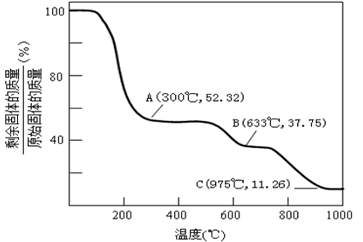
(6)固体NH4Al(SO4)2.12H2O在加热时,固体残留率随温度的变化如图所示。633℃时剩余固体成分的化学式为_____________ 。

回答下列问题:
(1)氧化步骤中发生的主要反应的离子方程式为
(2)当25℃时,Kw=1.0×10-14,Kb(NH3·H2O)=1.75×105。(NH4)2SO4溶液呈酸性,其原因是(用力方程式解释):
(3)如何检验中和液中的杂质离子已完全除尽
(4)NH4Al(SO4)2溶液与过量NaOH溶液混合加热,反应的化学方程式为
(5)综上分析,流程图中M的主要成分的化学式为
(6)固体NH4Al(SO4)2.12H2O在加热时,固体残留率随温度的变化如图所示。633℃时剩余固体成分的化学式为
您最近半年使用:0次



