H与O可以形成 和
和 两种化合物。请回答:
两种化合物。请回答:
(1) 可与
可与 形成
形成 ,
, 的空间构型名称为
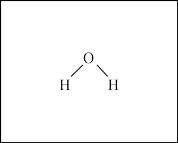
的空间构型名称为___________ 。根据 的成键特点,画出与下图中
的成键特点,画出与下图中 分子直接相连的所有氢键
分子直接相连的所有氢键_____ (用O—H…O表示)。
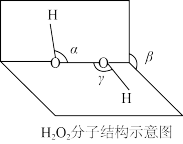
(2) 分子结构如图所示,
分子结构如图所示,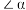 、
、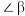 、
、 中相等的角是
中相等的角是___________ , 是
是___________ 分子(填“极性”或“非极性”)。 晶体中有4种作用力:①
晶体中有4种作用力:① 键、②
键、② 键、③范德华力、④氢键,这4种作用力由强到弱依次为:
键、③范德华力、④氢键,这4种作用力由强到弱依次为:___________ 。
(3)哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。根据以上原理,下列金属离子不能催化双氧水分解的是___________
A. B.
B. C.
C. D.
D. E.
E.
(4)实验测得,25℃时 的
的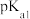 小于
小于 的
的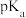 ,原因是
,原因是___________ (运用物质结构原理解释)。
 和
和 两种化合物。请回答:
两种化合物。请回答:(1)
 可与
可与 形成
形成 ,
, 的空间构型名称为
的空间构型名称为 的成键特点,画出与下图中
的成键特点,画出与下图中 分子直接相连的所有氢键
分子直接相连的所有氢键
(2)
 分子结构如图所示,
分子结构如图所示,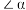 、
、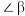 、
、 中相等的角是
中相等的角是 是
是 晶体中有4种作用力:①
晶体中有4种作用力:① 键、②
键、② 键、③范德华力、④氢键,这4种作用力由强到弱依次为:
键、③范德华力、④氢键,这4种作用力由强到弱依次为:
(3)哈勃-韦斯(Haber-Weiss)原理表明,某些金属离子可以催化双氧水分解的原因是:其次外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。根据以上原理,下列金属离子不能催化双氧水分解的是
A.
 B.
B. C.
C. D.
D. E.
E.
(4)实验测得,25℃时
 的
的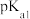 小于
小于 的
的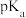 ,原因是
,原因是
更新时间:2022-07-06 08:44:18
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氯吡苯脲是一种常用的膨大剂,其结构简式为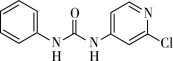 ,它是经国家批准使用的植物生长调节剂。
,它是经国家批准使用的植物生长调节剂。
(1)氯元素基态原子核外电子的未成对电子数为___________ 。
(2)氯吡苯脲晶体中,氮原子的杂化轨道类型为___________ ,羰基碳原子的杂化轨道类型为___________ 。
(3)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲,其反应方程式如下:
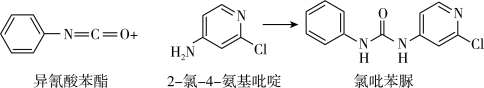
反应过程中,每生成1mol氯吡苯脲,断裂___________ 个σ键,断裂___________ 个π键。
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①请用共价键知识解释H2O分子比NH3分子稳定的原因为___________ 。
②H2O、NH3、CO2分子的空间结构分别是______ ,中心原子的杂化类型分别是______ 。
 ,它是经国家批准使用的植物生长调节剂。
,它是经国家批准使用的植物生长调节剂。(1)氯元素基态原子核外电子的未成对电子数为
(2)氯吡苯脲晶体中,氮原子的杂化轨道类型为
(3)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲,其反应方程式如下:

反应过程中,每生成1mol氯吡苯脲,断裂
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①请用共价键知识解释H2O分子比NH3分子稳定的原因为
②H2O、NH3、CO2分子的空间结构分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)A元素原子次外层电子数是最外层电子数的 ,其最外层电子的轨道表示式为
,其最外层电子的轨道表示式为_______ 。
(2)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,在元素周期表中的位置是_______ 。
(3)C元素基态原子的轨道表示式是图中的_______ (填序号),另一轨道表示式不能作为基态原子的轨道表示式是因为它不符合_______ (填序号)。
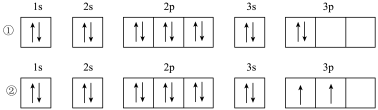
A.能量最低原理 B.泡利不相容原理 C.洪特规则
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量称为第一电离能(设为E)。如图所示:
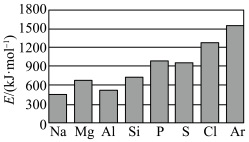
①根据图中提供的信息,可推断出E(氧)_______ (填“>”“<”或“=”,下同)E(氟);
②根据第一电离能的含义和元素周期律可推断出E(镁)_______ E(钙)。
(1)A元素原子次外层电子数是最外层电子数的
 ,其最外层电子的轨道表示式为
,其最外层电子的轨道表示式为(2)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,在元素周期表中的位置是
(3)C元素基态原子的轨道表示式是图中的

A.能量最低原理 B.泡利不相容原理 C.洪特规则
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量称为第一电离能(设为E)。如图所示:

①根据图中提供的信息,可推断出E(氧)
②根据第一电离能的含义和元素周期律可推断出E(镁)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】纳米微晶碱式碳酸锌是一种新型的碱式碳酸锌,在医药行业可用作皮肤保护剂。工业级硫酸锌(主要成分为ZnSO4·7H2O,含少量Fe2+、Cu2+、Cd2+、Co2+、Ni2+)制备纳米微晶碱式碳酸锌[Zn4CO3(OH)6]。回答下列各步转化涉及的问题:
(1)氧化除杂:向ZnSO4溶液中加H2O2除去溶液中Fe2+。Fe2+的电子排布式为___________ 。
(2)还原除杂:除Cu2+、Cd2+后,再加入Zn粉和少量Sb2S3,形成锑锌微电池,提高除Co2+、Ni2+的反应速率。则该条件下Zn2+、Ni2+、Sb3+的氧化性强弱顺序:___________ (用离子符号表示)。
(3)沉锌:加入NH4HCO3溶液、MgSO4·7H2O(只用于控制晶粒大小),过滤、洗涤得纳米微晶。
①生成纳米微晶碱式碳酸锌的离子方程式为___________ 。
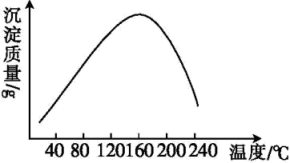
②实验测得在一段时间内加入等量NH4HCO3所得纳米微晶质量随反应温度的变化如图所示,分析曲线下降可能的原因:___________ 。
(4)用乙二胺四乙酸(俗称EDTA,H2Y2-表示乙二胺四乙酸根离子)滴定法测样品中锌的含量,反应原理为Zn2++H2Y2-=ZnY2-+2H+。取1.840g纳米微晶碱式碳酸锌样品,溶于pH为5~6的乙酸-乙酸钠缓冲溶液中配成100mL溶液,滴入少量的铬黑T作指示剂,取25.00mL置于锥形瓶中,向锥形瓶中加入过量的10.00mL2.000mol·L-1EDTA,振荡。用1.000mol·L-1锌标准溶液滴定过量的EDTA至终点,消耗锌标准溶液16.00mL。则样品中Zn元素的含量为___________ (写出计算过程)。
(1)氧化除杂:向ZnSO4溶液中加H2O2除去溶液中Fe2+。Fe2+的电子排布式为
(2)还原除杂:除Cu2+、Cd2+后,再加入Zn粉和少量Sb2S3,形成锑锌微电池,提高除Co2+、Ni2+的反应速率。则该条件下Zn2+、Ni2+、Sb3+的氧化性强弱顺序:
(3)沉锌:加入NH4HCO3溶液、MgSO4·7H2O(只用于控制晶粒大小),过滤、洗涤得纳米微晶。
①生成纳米微晶碱式碳酸锌的离子方程式为
②实验测得在一段时间内加入等量NH4HCO3所得纳米微晶质量随反应温度的变化如图所示,分析曲线下降可能的原因:

(4)用乙二胺四乙酸(俗称EDTA,H2Y2-表示乙二胺四乙酸根离子)滴定法测样品中锌的含量,反应原理为Zn2++H2Y2-=ZnY2-+2H+。取1.840g纳米微晶碱式碳酸锌样品,溶于pH为5~6的乙酸-乙酸钠缓冲溶液中配成100mL溶液,滴入少量的铬黑T作指示剂,取25.00mL置于锥形瓶中,向锥形瓶中加入过量的10.00mL2.000mol·L-1EDTA,振荡。用1.000mol·L-1锌标准溶液滴定过量的EDTA至终点,消耗锌标准溶液16.00mL。则样品中Zn元素的含量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】科学家开发出了多种太阳能电池,除晶体硅太阳能电池外,还有GaAs太阳能电池、铜铟镓硒薄膜太阳能电池等。
(1)基态Ga原子的电子排布式为________ 。
(2)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因________________ 。
(3)H2Se分子的键角_______ H2O分子的键角(选填“>”、“=”或“<”)。写出与SeO3互为等电子体的一种阴离子_____________ (写化学式)。
(4) AsF3分子的立体构型为__________ ;AsF3是极性分子,理由是_________________ 。
(5)Ga(OH)3与NaOH溶液反应生成Na[Ga(OH)4]。Na[Ga(OH)4]溶液中含有的化学键有__________________ 。
A.共价键 B.离子键 C.金属键 D.配位键 E.氢键
(6)金刚砂(SiC)晶胞如图所示:
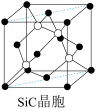
金刚砂中硅原子的杂化轨道类型为_______ ,沿晶胞图中虚线方向的切面图为__________ (填标号)。

(1)基态Ga原子的电子排布式为
(2)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因
(3)H2Se分子的键角
(4) AsF3分子的立体构型为
(5)Ga(OH)3与NaOH溶液反应生成Na[Ga(OH)4]。Na[Ga(OH)4]溶液中含有的化学键有
A.共价键 B.离子键 C.金属键 D.配位键 E.氢键
(6)金刚砂(SiC)晶胞如图所示:

金刚砂中硅原子的杂化轨道类型为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求回答以下内容。
(1)Cu基态原子的价电子排布式_______ ; 它位于周期表的_______ 区。
(2)基态S原子电子占据最高能级的电子云轮廓图为_______ 形; SO2分子中的中心原子杂化方式为_______ ,SO 的空间结构为
的空间结构为_______ 。
(3)近期我国科学家对嫦娥五号月球土壤样品进行了分析,研究表明每吨月壤样品的钛含量是地球土壤平均含量的6倍多。Ti 在元素周期表的位置_______ ; 基态Ti原子的电子排布式 _______ 。
(4)H2O2的空间结构示意图如下。
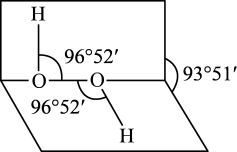
①下列关于H2O2的说法中正确的是_______ (填字母)。
A.分子中有极性键 B.分子中有非极性键
C.氧原子的轨道发生了sp2 杂化 D.分子是非极性分子
②H2O2可使酸性K2Cr2O7溶液由橙黄色变为绿色,铬元素被还原为+3价,该反应的离子方程式是_______ 。
(1)Cu基态原子的价电子排布式
(2)基态S原子电子占据最高能级的电子云轮廓图为
 的空间结构为
的空间结构为(3)近期我国科学家对嫦娥五号月球土壤样品进行了分析,研究表明每吨月壤样品的钛含量是地球土壤平均含量的6倍多。Ti 在元素周期表的位置
(4)H2O2的空间结构示意图如下。

①下列关于H2O2的说法中正确的是
A.分子中有极性键 B.分子中有非极性键
C.氧原子的轨道发生了sp2 杂化 D.分子是非极性分子
②H2O2可使酸性K2Cr2O7溶液由橙黄色变为绿色,铬元素被还原为+3价,该反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在①HF、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ 、⑦
、⑦ 分子中:(填序号)
分子中:(填序号)
(1)以非极性键结合的非极性分子是___________ ;
(2)以极性键结合的具有直线形结构的非极性分子是___________ ;
(3)以极性键结合的具有正四面体形结构的非极性分子是___________ ;
(4)以极性键结合的具有三角锥形结构的极性分子是___________ ;
(5)以极性键结合的具有 杂化轨道和V形结构的分子是
杂化轨道和V形结构的分子是___________ ;
(6)以极性键结合的具有 杂化轨道结构的分子是
杂化轨道结构的分子是___________ 。
 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ 、⑦
、⑦ 分子中:(填序号)
分子中:(填序号)(1)以非极性键结合的非极性分子是
(2)以极性键结合的具有直线形结构的非极性分子是
(3)以极性键结合的具有正四面体形结构的非极性分子是
(4)以极性键结合的具有三角锥形结构的极性分子是
(5)以极性键结合的具有
 杂化轨道和V形结构的分子是
杂化轨道和V形结构的分子是(6)以极性键结合的具有
 杂化轨道结构的分子是
杂化轨道结构的分子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】水是地球上最常见的物质之一,是所有生命生存的重要资源。
(1)水溶液中存在H3O+离子,写出该微粒的结构式____________________ (标出配位键)。
(2)科学家发现在特殊条件下,水能表现出许多种有趣的结构和性质
①一定条件下给水施加一个弱电场,常温常压下水结成冰,俗称“热冰”,其计算机模拟图如下:
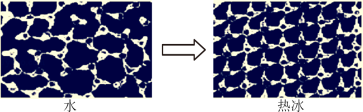
使水结成“热冰”采用“弱电场”的条件,说明水分子是______ 分子(填“极性”或“非极性”)。下列物质熔化时,所克服的微粒间的作用与“热冰”熔化时所克服的作用力类型完全相同的是______ 。
A.固态氨 B.食盐 C.干冰 D.金刚石
②用高能射线照射液态水时,一个水分子能释放出一个电子,同时产生一种阳离子。产生的阳离子具有较强的氧化性,试写出该阳离子与SO2的水溶液反应的离子方程式____________ ;该阳离子还能与水作用生成羟基,经测定此时的水具有酸性,写出该过程的离子方程式____ 。
(3)水的性质中的一些特殊现象对于生命的存在意义非凡,请解释水的分解温度远高于其沸点的原____________
(1)水溶液中存在H3O+离子,写出该微粒的结构式
(2)科学家发现在特殊条件下,水能表现出许多种有趣的结构和性质
①一定条件下给水施加一个弱电场,常温常压下水结成冰,俗称“热冰”,其计算机模拟图如下:

使水结成“热冰”采用“弱电场”的条件,说明水分子是
A.固态氨 B.食盐 C.干冰 D.金刚石
②用高能射线照射液态水时,一个水分子能释放出一个电子,同时产生一种阳离子。产生的阳离子具有较强的氧化性,试写出该阳离子与SO2的水溶液反应的离子方程式
(3)水的性质中的一些特殊现象对于生命的存在意义非凡,请解释水的分解温度远高于其沸点的原
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】2022年9月,中国科学家首次在嫦娥五号带回的月壤中发现新矿物,并命名为“嫦娥石”。“嫦娥石”属于陨磷钠镁钙石族,其中一种物质的化学式为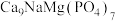 。请回答下列问题:
。请回答下列问题:
(1)钠在火焰上灼烧的黄光是一种_______ (填字母)。
a.吸收光谱 b.发射光谱
(2)某同学把O原子价电子的轨道表示式写成了以下形式: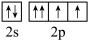 ,这种写法违背了
,这种写法违背了_______ 。
(3)P原子最高能级电子的电子云轮廓形状为_______ ,其价电子排布式为_______ ,电负性P_______ O(填“>”或“<”)。
(4)PCl3分子空间结构为_______ ,PCl3与Cl2反应生成PCl5,PCl5结构为 ,PCl5是
,PCl5是_______ 分子(填“极性”或“非极性”),其中P原子的杂化类型是_______ (填字母序号)。
a.sp b.sp2 c.sp3 d.sp3d
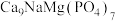 。请回答下列问题:
。请回答下列问题:(1)钠在火焰上灼烧的黄光是一种
a.吸收光谱 b.发射光谱
(2)某同学把O原子价电子的轨道表示式写成了以下形式:
 ,这种写法违背了
,这种写法违背了(3)P原子最高能级电子的电子云轮廓形状为
(4)PCl3分子空间结构为
 ,PCl5是
,PCl5是a.sp b.sp2 c.sp3 d.sp3d
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】形形色色的物质,构成了我们这个五彩缤纷的世界。学习物质结构和性质的知识,能使你想象的翅膀变得更加有力。
(1)下列物质中既有极性键,又有非极性键的极性分子是_______。
(2)BF3的电子式_______ ,F—B—F的键角是_______ 。BF3和过量的NaF作用可生成NaBF4,BF 的立体构型为
的立体构型为_______ 。
(3)CCl3COOH、C2H5COOH、CF3COOH的酸性由强到弱的顺序为_______ ,请解释酸性大小的原因_______ 。
(1)下列物质中既有极性键,又有非极性键的极性分子是_______。
| A.SO2 | B.CCl4 | C.H2O2 | D.C2H2 |
 的立体构型为
的立体构型为(3)CCl3COOH、C2H5COOH、CF3COOH的酸性由强到弱的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】物质的结构与性质之间有密切的关系。请回答下列问题:
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于_______ 晶体;镍原子和碳原子之间存在_______ 键。
(2)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是_______ (填“极性”或“非极性”)分子。
(3)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有_______ (填序号),CS2分子的空间结构是_______ 。
(4)已知苯酚(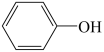 )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子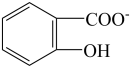 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)_______ Ka(苯酚)(填“>”或“<”),其原因是_______ 。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于
(2)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是
(3)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有
(4)已知苯酚(
 )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列空白处
(1)热的 溶液可用于清洗油污,请用离子方程式解释原因
溶液可用于清洗油污,请用离子方程式解释原因___________ 。
(2)下列三种共价晶体:①金刚石、②晶体硅、③碳化硅,熔点从高到低的顺序是___________ (用序号表示)。
(3)对羟基苯甲醛(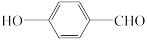 )沸点比邻羟基苯甲醛(
)沸点比邻羟基苯甲醛(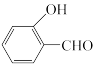 )高的原因是
)高的原因是___________ 。
(4)元素Mn与Fe的部分电离能数据如下表所示:
根据表中数据可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,其原因是
再失去1个电子难,其原因是___________ 。
(1)热的
 溶液可用于清洗油污,请用离子方程式解释原因
溶液可用于清洗油污,请用离子方程式解释原因(2)下列三种共价晶体:①金刚石、②晶体硅、③碳化硅,熔点从高到低的顺序是
(3)对羟基苯甲醛(
 )沸点比邻羟基苯甲醛(
)沸点比邻羟基苯甲醛( )高的原因是
)高的原因是(4)元素Mn与Fe的部分电离能数据如下表所示:
| 元素 | Mn | Fe | |
电离能/( ) ) |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
根据表中数据可知,气态
 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,其原因是
再失去1个电子难,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮及其化合物在生产、生活和科技等方面有重要的应用。请回答下列问题:
(1)氮元素基态原子的价电子排布图为______________ 。
(2)在氮分子中,氮原子之间存在着______ 个σ键和______ 个π键。
(3)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3﹣,请写出两种与N3﹣互为等电子体的分子_______ 、_______ 。
(4)氮元素的氢化物(NH3)是一种易液化的气体,请阐述原因是_____________________ 。
(5)NF3、NCl3、NBr3的沸点由高到低的顺序是___________________________ 。
(6)Mg3N2遇水发生剧烈反应,生成一种有刺激性气味的气体.该反应的化学方程式为_______ 。
(1)氮元素基态原子的价电子排布图为
(2)在氮分子中,氮原子之间存在着
(3)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3﹣,请写出两种与N3﹣互为等电子体的分子
(4)氮元素的氢化物(NH3)是一种易液化的气体,请阐述原因是
(5)NF3、NCl3、NBr3的沸点由高到低的顺序是
(6)Mg3N2遇水发生剧烈反应,生成一种有刺激性气味的气体.该反应的化学方程式为
您最近一年使用:0次



