氯吡苯脲是一种常用的膨大剂,其结构简式为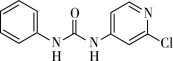 ,它是经国家批准使用的植物生长调节剂。
,它是经国家批准使用的植物生长调节剂。
(1)氯元素基态原子核外电子的未成对电子数为___________ 。
(2)氯吡苯脲晶体中,氮原子的杂化轨道类型为___________ ,羰基碳原子的杂化轨道类型为___________ 。
(3)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲,其反应方程式如下:
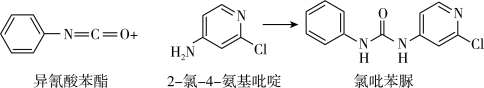
反应过程中,每生成1mol氯吡苯脲,断裂___________ 个σ键,断裂___________ 个π键。
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①请用共价键知识解释H2O分子比NH3分子稳定的原因为___________ 。
②H2O、NH3、CO2分子的空间结构分别是______ ,中心原子的杂化类型分别是______ 。
 ,它是经国家批准使用的植物生长调节剂。
,它是经国家批准使用的植物生长调节剂。(1)氯元素基态原子核外电子的未成对电子数为
(2)氯吡苯脲晶体中,氮原子的杂化轨道类型为
(3)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲,其反应方程式如下:

反应过程中,每生成1mol氯吡苯脲,断裂
(4)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等。
①请用共价键知识解释H2O分子比NH3分子稳定的原因为
②H2O、NH3、CO2分子的空间结构分别是
20-21高二·全国·课时练习 查看更多[12]
(人教版2019)选择性必修2 第二章 分子结构与性质 第二节 分子的空间结构 课时2 杂化轨道理论(已下线)2.2 分子的空间结构(C级检测练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)(已下线)考点34 分子结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)2.2.2 杂化轨道理论简介-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)(已下线)2.2 分子的空间结构(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)第2章 章末综合测评B-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)(已下线)考点47 分子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)专题4 分子空间结构与物质性质 本专题达标检测第二章 本章达标检测2(已下线)【知识图鉴】单元讲练测选择性必修2第二章03单元测(已下线)【知识图鉴】单元讲练测选择性必修2第二章02练基础湖南省衡阳市衡阳县第四中学2022-2023学年高二下学期期中考试化学试题
更新时间:2022-02-07 19:38:24
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答问题
(1)2020年12月17日,“嫦娥五号”首次成功实现地外天体采样返回,标志着我国航天向前迈出了一大步。其制作材料中包含了Al、Cr、Cu、C、N、O、Si等多种元素。上述元素中基态原子未成对电子数与Al相同的有___________ 。
(2)元素铋主要用于制造易熔金属合金,元素Bi位于第6周期VA族,其基态原子的价电子排布式为___________ 。Bi(NO3)3∙5H2O中各元素电负性从大到小的顺序为___________ 。
(3)N、P、As均为氮族元素,这些元素与人们的生活息息相关。回答下列问题:
①下列状态的N原子或离子在跃迁时,用光谱仪可捕捉到发射光谱的是___________ (填序号,下同),未成对电子最多的是___________ 。
a. 1s22s22p3 b. 1s22s2 c. 1s22s12p4 d. 1s2s12p3
②Si、P与S是同周期中相邻的元素,Si、P、S的电负性由大到小的顺序是___________ ,第一电离能由大到小的顺序是___________ 。
(1)2020年12月17日,“嫦娥五号”首次成功实现地外天体采样返回,标志着我国航天向前迈出了一大步。其制作材料中包含了Al、Cr、Cu、C、N、O、Si等多种元素。上述元素中基态原子未成对电子数与Al相同的有
(2)元素铋主要用于制造易熔金属合金,元素Bi位于第6周期VA族,其基态原子的价电子排布式为
(3)N、P、As均为氮族元素,这些元素与人们的生活息息相关。回答下列问题:
①下列状态的N原子或离子在跃迁时,用光谱仪可捕捉到发射光谱的是
a. 1s22s22p3 b. 1s22s2 c. 1s22s12p4 d. 1s2s12p3
②Si、P与S是同周期中相邻的元素,Si、P、S的电负性由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】表为周期表的一部分,其中的编号代表对应的元素。
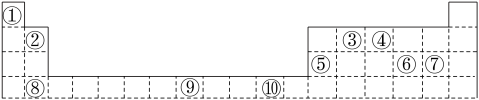
请回答下列问题:
(1)表中属于d区的元素是________ (填编号)。
(2)写出元素⑧的基态原子的电子排布式__________________________ 。
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子为________ 对。
(4)元素④的氢化物的分子构型为________ ,中心原子的杂化形式为________ 。
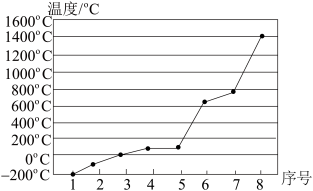
(5)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表________ (填元素符号);其中电负性最大的是________ (填图中的序号)。

请回答下列问题:
(1)表中属于d区的元素是
(2)写出元素⑧的基态原子的电子排布式
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子为
(4)元素④的氢化物的分子构型为

(5)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】[化学―选修3:物质结构与性质]
研究物质的微观结构,有助于人们理解物质变化的本质。请根据已学习的物质结构知识,回答下列问题:
(l)基态Mn原子的价电子排布式为___ ,气态Mn2+再失去l个电子比Fe2+再失去1个电子更难,其原因是________ 。
(2)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有_____ 。写出难溶物溶于氨水时的离子方程式__________ 。实验过程中加入C2H5OH 后可观察到析出深蓝色Cu(NH3)4SO4·5H2O晶体。实验中所加C2H5OH 的作用是______ 。
(3) HClO2、HClO3为氯元素的含氧酸,试推测ClO2-的空间结构:________ ;HClO3分子中,Cl原子的杂化方式为______ ;两种酸酸性较强的是_______ .
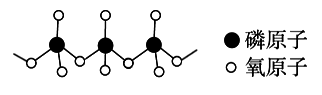
(4)多磷酸盐的酸根阴离子是由两个或两个以上磷氧四面体通过共用角顶氧原子而连接起来的,部分结构如图所示,多磷酸根离子的通式为______ 。(磷原子数目用n表示)
(5)金属Pt采用“…ABCABC…”型堆积方式,抽出一个晶胞,其正确的是________ 。

已知金属Pt的密度为21.4 g/cm3,则Pt原子半径的计算式为______ pm (只列式,不必计算结果,Pt的相对原子质量为M,阿伏伽德罗常数为6.02×1023mol-1)。
研究物质的微观结构,有助于人们理解物质变化的本质。请根据已学习的物质结构知识,回答下列问题:
(l)基态Mn原子的价电子排布式为
(2)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有
(3) HClO2、HClO3为氯元素的含氧酸,试推测ClO2-的空间结构:
(4)多磷酸盐的酸根阴离子是由两个或两个以上磷氧四面体通过共用角顶氧原子而连接起来的,部分结构如图所示,多磷酸根离子的通式为

(5)金属Pt采用“…ABCABC…”型堆积方式,抽出一个晶胞,其正确的是

已知金属Pt的密度为21.4 g/cm3,则Pt原子半径的计算式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】三乙酸锰([Mn(CH3COO)3])是一种锰的配合物,在有机合成中有重要的应用价值。CH3COO―为该配合物的配体,其所含元素的电负性最大的是___________ ;FCH2COO-、ClCH2COO-也可作为配体使用,相同条件下,FCH2COO-、ClCH2COO-结合H+的能力较强的是___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据所学内容填空:
(1)有下列物质:①HF、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,其中属于极性分子的是
,其中属于极性分子的是_______ (填序号,下同),既有 键又有
键又有 键的是
键的是_______ 。
(2)下列分子中,空间构型为正四面体且键角为109°28′的是_______ 。
a. b.
b. c.
c.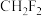 d.
d. e.
e. f.
f.
(3) 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是_______ 。
(4)丙烯腈分子( )中碳原子杂化轨道类型为
)中碳原子杂化轨道类型为_______ 。
(5)ⅥA族元素氧、硫、硒(Se)的化合物在研究和生产中有许多重要用途。
① 的酸性比
的酸性比
_______ (填“强”或“弱”)。 离子的空间构型为
离子的空间构型为_______ 。
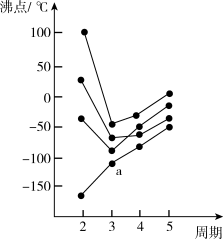
②如图所示,每条折线表示周期表ⅣA—ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是_______ (化学式)。
(1)有下列物质:①HF、②
 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,其中属于极性分子的是
,其中属于极性分子的是 键又有
键又有 键的是
键的是(2)下列分子中,空间构型为正四面体且键角为109°28′的是
a.
 b.
b. c.
c.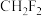 d.
d. e.
e. f.
f.
(3)
 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是(4)丙烯腈分子(
 )中碳原子杂化轨道类型为
)中碳原子杂化轨道类型为(5)ⅥA族元素氧、硫、硒(Se)的化合物在研究和生产中有许多重要用途。
①
 的酸性比
的酸性比
 离子的空间构型为
离子的空间构型为②如图所示,每条折线表示周期表ⅣA—ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)氨易溶于水的原因是__________________ ;________________ (写出两点即可)。
(2)化学上有一种见解,认为含氧酸的通式可写成(HO)mROn,如果成酸元素R相同,则n值越大,酸性越________ (填“强”或“弱”)。以下各种含氧酸①H3RO4、②(HO)RO3、③H4RO4、④(HO)2RO2的酸性由强到弱的顺序排列为________________ (填序号)。
(3)为了减缓温室效应,科学家设计反应CO2+4H2===CH4+2H2O以减少空气中CO2的排放量。若有1 mol CH4生成,则有________ mol σ键和________ mol π键断裂。
(2)化学上有一种见解,认为含氧酸的通式可写成(HO)mROn,如果成酸元素R相同,则n值越大,酸性越
(3)为了减缓温室效应,科学家设计反应CO2+4H2===CH4+2H2O以减少空气中CO2的排放量。若有1 mol CH4生成,则有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠檬酸铁铵((NH4)3Fe(C6H5O7)2)。
(1)Fe基态核外电子排布式为________ ;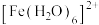 中与Fe2+配位的原子是
中与Fe2+配位的原子是______ (填元素符号)。
(2)H2O2是________ 分子(填“极性”“非极性”),电子式为_______ 。
(3)NH3分子中氮原子的轨道杂化类型是_______ ;C、N、O元素的第一电离能由大到小的顺序为___________ 。
(4)与 互为等电子体的一种分子为
互为等电子体的一种分子为_______ (填化学式)。
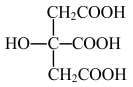
(5)柠檬酸的结构简式如下图。1mol柠檬酸分子中碳原子与氧原子形成的σ键为_________ mol。
(1)Fe基态核外电子排布式为
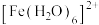 中与Fe2+配位的原子是
中与Fe2+配位的原子是(2)H2O2是
(3)NH3分子中氮原子的轨道杂化类型是
(4)与
 互为等电子体的一种分子为
互为等电子体的一种分子为(5)柠檬酸的结构简式如下图。1mol柠檬酸分子中碳原子与氧原子形成的σ键为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表为长式周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于d区的元素是___________ (填编号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为_________ 。
(3)④ ⑤ ⑥ ⑦四种元素的第一电离能由大到小的顺序是___________ (用元素符号表示)。
(4)按原子轨道的重叠方式,③与⑥形成的化合物中σ键有______ 个,π键有______ 个。
(5)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为_______ ;该元素与元素①形成的分子X的空间构形为___________ 。
(6)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:__________________ 。

请回答下列问题:
(1)表中属于d区的元素是
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为
(3)④ ⑤ ⑥ ⑦四种元素的第一电离能由大到小的顺序是
(4)按原子轨道的重叠方式,③与⑥形成的化合物中σ键有
(5)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为
(6)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
您最近一年使用:0次



