根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)A元素原子次外层电子数是最外层电子数的 ,其最外层电子的轨道表示式为
,其最外层电子的轨道表示式为_______ 。
(2)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,在元素周期表中的位置是_______ 。
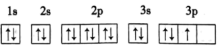
(3)C元素基态原子的轨道表示式是图中的_______ (填序号),另一轨道表示式不能作为基态原子的轨道表示式是因为它不符合_______ (填序号)。
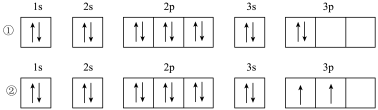
A.能量最低原理 B.泡利不相容原理 C.洪特规则
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量称为第一电离能(设为E)。如图所示:
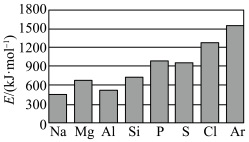
①根据图中提供的信息,可推断出E(氧)_______ (填“>”“<”或“=”,下同)E(氟);
②根据第一电离能的含义和元素周期律可推断出E(镁)_______ E(钙)。
(1)A元素原子次外层电子数是最外层电子数的
 ,其最外层电子的轨道表示式为
,其最外层电子的轨道表示式为(2)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,在元素周期表中的位置是
(3)C元素基态原子的轨道表示式是图中的

A.能量最低原理 B.泡利不相容原理 C.洪特规则
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量称为第一电离能(设为E)。如图所示:

①根据图中提供的信息,可推断出E(氧)
②根据第一电离能的含义和元素周期律可推断出E(镁)
更新时间:2023-09-08 19:04:06
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】注意:电离能的影响因素及特例
(1)电离能数值的大小主要取决于原子的_______ 、原子半径及原子的电子构型。
(2)具有全充满、半充满及全空的电子构型的元素稳定性较高,其电离能数值_______ ,如稀有气体的电离能在同周期元素中_______ ,N为半充满、Mg为全充满状态,其电离能均比同周期相邻元素大。一般情况,第一电离能:ⅡA_______ ⅢA,ⅤA_______ ⅥA。
(1)电离能数值的大小主要取决于原子的
(2)具有全充满、半充满及全空的电子构型的元素稳定性较高,其电离能数值
您最近一年使用:0次
【推荐2】洪特规则
(1)内容:基态原子中,填入_______ 的电子总是先单独分占,且自旋平行。
(2)特例:在简并轨道上的电子排布处于全充满、半充满和全空状态时,具有_______ 的能量和_______ 的稳定性。

如:24Cr的电子排布式为_______ ,为半充满状态,易错写为1s22s22p63s23p63d44s2。
(1)内容:基态原子中,填入
(2)特例:在简并轨道上的电子排布处于全充满、半充满和全空状态时,具有

如:24Cr的电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求填空:
(1)Si的价电子层的电子排布式为_____ 。
(2)基态硫原子价电子排布式为_____ 。
(3)在KH2PO4的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是_____ (填离子符号)。
(4)基态硅原子最外层的电子排布图为_____ 。
(1)Si的价电子层的电子排布式为
(2)基态硫原子价电子排布式为
(3)在KH2PO4的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是
(4)基态硅原子最外层的电子排布图为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】黄铁矿是制取硫酸的主要原料,其主要成分为FeS2,其中铁元素显+2价,FeS2晶体的晶胞形状为立方体,晶胞结构如图所示。___________ 。
(2)制取硫酸过程中会产生SO3,SO3分子的空间构型为___________ 。
(3)晶胞中与每个S 距离最近且相等的Fe2+有
距离最近且相等的Fe2+有___________ 个。
(4)FeS2晶体的晶胞边长为anm,FeS2的摩尔质量为120g·mol-1,阿伏加德罗常数的值为NA,该FeS2晶体的密度ρ=___________ g·cm-3(1nm=10-7cm,用含a、NA的代数式表示)

(2)制取硫酸过程中会产生SO3,SO3分子的空间构型为
(3)晶胞中与每个S
 距离最近且相等的Fe2+有
距离最近且相等的Fe2+有(4)FeS2晶体的晶胞边长为anm,FeS2的摩尔质量为120g·mol-1,阿伏加德罗常数的值为NA,该FeS2晶体的密度ρ=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】白铜是以镍为主要添加元素的铜基合金,呈银白色,有金属光泽,故名白铜。云南镍白铜(铜镍合金)文明中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1) 的核外电子排布式为
的核外电子排布式为_______ ,3d能级上的未成对的电子数为_______ 。
(2)硫酸镍溶于氨水形成蓝色的 溶液。
溶液。
①在 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为_______ ,提供孤电子对的成键原子是_______ (用元素符表示)。
②氨极易溶于 ,除因为它们都是极性分子外,还因为
,除因为它们都是极性分子外,还因为_______ 。
(3)单质铜及镍都是由_______ 键形成的晶体;元素铜与镍的第二电离能分别为: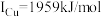 ,
,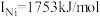 ,
,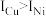 的原因是
的原因是_______ 。
(1)
 的核外电子排布式为
的核外电子排布式为(2)硫酸镍溶于氨水形成蓝色的
 溶液。
溶液。①在
 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为②氨极易溶于
 ,除因为它们都是极性分子外,还因为
,除因为它们都是极性分子外,还因为(3)单质铜及镍都是由
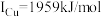 ,
,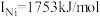 ,
,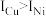 的原因是
的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
(2)Fe成为阳离子时首先失去___________ 轨道电子,Sm的价层电子排布式为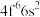 ,
,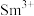 价层电子排布式为
价层电子排布式为___________ 。
(3) 基态核外电子排布式为
基态核外电子排布式为___________ 。
(4)Mn位于元素周期表中第四周期___________ 族,基态Mn原子核外未成对电子有___________ 个。
(5)下列 原子电子排布图表示的状态中,能量最高的为___________(填标号)。
原子电子排布图表示的状态中,能量最高的为___________(填标号)。
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
A. | B. | C.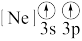 | D. |
(2)Fe成为阳离子时首先失去
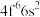 ,
,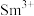 价层电子排布式为
价层电子排布式为(3)
 基态核外电子排布式为
基态核外电子排布式为(4)Mn位于元素周期表中第四周期
(5)下列
 原子电子排布图表示的状态中,能量最高的为___________(填标号)。
原子电子排布图表示的状态中,能量最高的为___________(填标号)。A.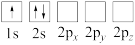 | B. | C. | D.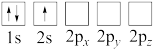 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电负性与电离能是两种定量描述元素原子得失电子能力的参数,请根据下列数据回答问题。
(1)非金属性:S___________ (填“>”、“=”或“<”)F。
(2)依据电负性数值,上述元素中最容易形成离子键的是___________ 和___________ 。
(3)已知某主族元素Y,其基态原子核外有2个电子层,3个未成对电子,Y元素基态原子的轨道表示式为___________ ,通过分析电负性的变化规律,确定Y元素电负性的取值范围是___________ 。
(4)由电负性数据推断:化合物PBr3中P的化合价为___________ 。已知PBr3与水反应是非氧化还原反应,写出PBr3与水反应的化学方程式___________ 。
| 元素符号 | Li | Be | C | O | F | Na | Al | P | S | Br |
| 电负性 | 1.0 | 1.5 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 2.2 | 2.5 | 2.8 |
(2)依据电负性数值,上述元素中最容易形成离子键的是
(3)已知某主族元素Y,其基态原子核外有2个电子层,3个未成对电子,Y元素基态原子的轨道表示式为
(4)由电负性数据推断:化合物PBr3中P的化合价为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据原子结构与性质的相关知识,请回答下列问题:
(1)基态S原子电子占据最高能层的符号是___________ ,最高能级的电子云轮廓图为___________ 形。
(2)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为_____ 、_____ (填标号)。

(3)Fe3+基态核外电子排布式为___________
(4)根据元素周期律,原子半径As________ Se,电负性As________ Se (填“大于”或“小于”)
(5)元素铜与镍的第二电离能分别为:ICu=1958kJ·mol-1、INi=1753kJ·mol-1, ICu>INi的原因是___________
(1)基态S原子电子占据最高能层的符号是
(2)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为

(3)Fe3+基态核外电子排布式为
(4)根据元素周期律,原子半径As
(5)元素铜与镍的第二电离能分别为:ICu=1958kJ·mol-1、INi=1753kJ·mol-1, ICu>INi的原因是
您最近一年使用:0次
【推荐2】回答下列问题:
(1)下列原子或离子的电子排布式或轨道表示式正确的是___________ (填序号)
①K+: ②F:
②F: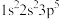
③P: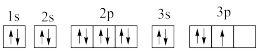
④Cu: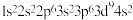
⑤Fe2+: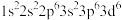
⑥Mg:
⑦O: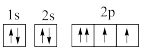
(2)基态原子的核外电子填充在6个轨道中的元素有___________ 种;
(3)C、N、O第一电离能从大到小的顺序为:___________ ;
(4)第四周期元素中,未成对电子数最多的元素是:___________ (写元素符号)。
(1)下列原子或离子的电子排布式或轨道表示式正确的是
①K+:
 ②F:
②F: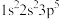
③P:
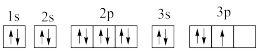
④Cu:
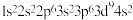
⑤Fe2+:
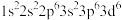
⑥Mg:

⑦O:
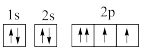
(2)基态原子的核外电子填充在6个轨道中的元素有
(3)C、N、O第一电离能从大到小的顺序为:
(4)第四周期元素中,未成对电子数最多的元素是:
您最近一年使用:0次

 :
: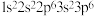
 :
: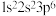
 :
:
 :
: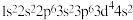
 :
:
 :
:
 :
: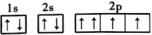
 能级,该能层有
能级,该能层有 、
、 均为短周期金属元素。依据下表数据,写出
均为短周期金属元素。依据下表数据,写出






