物质的结构与性质之间有密切的关系。请回答下列问题:
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于_______ 晶体;镍原子和碳原子之间存在_______ 键。
(2)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是_______ (填“极性”或“非极性”)分子。
(3)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有_______ (填序号),CS2分子的空间结构是_______ 。
(4)已知苯酚(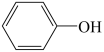 )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子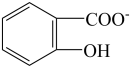 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)_______ Ka(苯酚)(填“>”或“<”),其原因是_______ 。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于
(2)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是
(3)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有
(4)已知苯酚(
 )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)
更新时间:2022-04-24 19:47:05
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】利用“杯酚”从C60和C70的混合物中纯化C70的过程如下图所示。

(1)“杯酚”的官能团是___________ 。
(2)“杯酚”分子内官能团之间通过___________ (填作用力类型)形成“杯底”。
(3)对叔丁基苯酚[ ]与
]与 反应,生成“杯酚”和一种无机物。
反应,生成“杯酚”和一种无机物。
①该无机物是___________ 。
②关于对叔丁基苯酚的叙述,正确的是___________ (填序号)。
a.分子式为 b.分子中所有碳原子均为
b.分子中所有碳原子均为 杂化
杂化
c.易被空气中的氧气氧化 d.1mol对叔丁基苯酚最多能与1mol 发生反应
发生反应
(4) 不溶于氯仿(化学式为
不溶于氯仿(化学式为 ),“杯酚”溶于氯仿,可能的原因是
),“杯酚”溶于氯仿,可能的原因是___________ 。

(1)“杯酚”的官能团是
(2)“杯酚”分子内官能团之间通过
(3)对叔丁基苯酚[
 ]与
]与 反应,生成“杯酚”和一种无机物。
反应,生成“杯酚”和一种无机物。①该无机物是
②关于对叔丁基苯酚的叙述,正确的是
a.分子式为
 b.分子中所有碳原子均为
b.分子中所有碳原子均为 杂化
杂化c.易被空气中的氧气氧化 d.1mol对叔丁基苯酚最多能与1mol
 发生反应
发生反应(4)
 不溶于氯仿(化学式为
不溶于氯仿(化学式为 ),“杯酚”溶于氯仿,可能的原因是
),“杯酚”溶于氯仿,可能的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象地称为“液态阳光”计划。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。回答下列问题:
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为___ 。SiCl4可发生水解反应,机理如图:
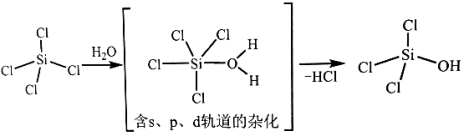
含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为___ (填标号)。
(2)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是___ 。
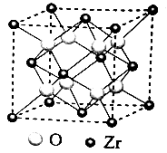
(3)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO2固溶体。四方ZrO2晶胞如图所示。Zr4+离子在晶胞中的配位数是__ ,晶胞参数为apm、apm、cpm,该晶体密度为__ g·cm-3(写出表达式)。在ZrO2中掺杂少量ZnO后形成的催化剂,化学式可表示为ZnxZr1-xOy,则y=___ (用x表达)。
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为

含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为
(2)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是
(3)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO2固溶体。四方ZrO2晶胞如图所示。Zr4+离子在晶胞中的配位数是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】2023年5月30日,搭载神舟十六号载人飞船的长征二号F遥十六运载火箭在酒泉卫星发射中心成功发射,标志着中国航天事业的又一重大进展。长征系列运载火箭使用偏二甲肼作燃料, 作氧化剂,既能在短时间内产生巨大能量,产物又不污染空气(产物都是空气成分)。
作氧化剂,既能在短时间内产生巨大能量,产物又不污染空气(产物都是空气成分)。
(1)偏二甲肼的分子式是___________ 。
(2)有关偏二甲肼说法正确的是___________。(不定项)
(3)偏二甲肼与四氧化二氮的化学反应方程式是___________ 。
(4)偏二甲肼可用肼( )来制备,
)来制备, 的结构式是
的结构式是___________ 。
(5)肼也可作为火箭发功机的燃料,与氧化剂 反位生成氮气和水蒸气。
反位生成氮气和水蒸气。
已知①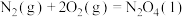
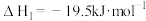
②
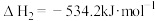
则肼和 反应的热化学方程式是
反应的热化学方程式是___________ 。
 作氧化剂,既能在短时间内产生巨大能量,产物又不污染空气(产物都是空气成分)。
作氧化剂,既能在短时间内产生巨大能量,产物又不污染空气(产物都是空气成分)。(1)偏二甲肼的分子式是
(2)有关偏二甲肼说法正确的是___________。(不定项)
A.碳原子采用 杂化 杂化 | B.分子中既有极性键又有非极性键 |
| C.偏二甲肼分子是非极性分子 | D.偏二甲肼的沸点低于异丁烷 |
(4)偏二甲肼可用肼(
 )来制备,
)来制备, 的结构式是
的结构式是(5)肼也可作为火箭发功机的燃料,与氧化剂
 反位生成氮气和水蒸气。
反位生成氮气和水蒸气。已知①
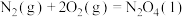
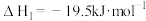
②

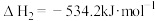
则肼和
 反应的热化学方程式是
反应的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】水是地球上最常见的物质之一,是所有生命生存的重要资源。
(1)水溶液中存在H3O+离子,写出该微粒的结构式____________________ (标出配位键)。
(2)科学家发现在特殊条件下,水能表现出许多种有趣的结构和性质
①一定条件下给水施加一个弱电场,常温常压下水结成冰,俗称“热冰”,其计算机模拟图如下:
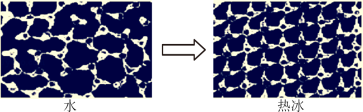
使水结成“热冰”采用“弱电场”的条件,说明水分子是______ 分子(填“极性”或“非极性”)。下列物质熔化时,所克服的微粒间的作用与“热冰”熔化时所克服的作用力类型完全相同的是______ 。
A.固态氨 B.食盐 C.干冰 D.金刚石
②用高能射线照射液态水时,一个水分子能释放出一个电子,同时产生一种阳离子。产生的阳离子具有较强的氧化性,试写出该阳离子与SO2的水溶液反应的离子方程式____________ ;该阳离子还能与水作用生成羟基,经测定此时的水具有酸性,写出该过程的离子方程式____ 。
(3)水的性质中的一些特殊现象对于生命的存在意义非凡,请解释水的分解温度远高于其沸点的原____________
(1)水溶液中存在H3O+离子,写出该微粒的结构式
(2)科学家发现在特殊条件下,水能表现出许多种有趣的结构和性质
①一定条件下给水施加一个弱电场,常温常压下水结成冰,俗称“热冰”,其计算机模拟图如下:

使水结成“热冰”采用“弱电场”的条件,说明水分子是
A.固态氨 B.食盐 C.干冰 D.金刚石
②用高能射线照射液态水时,一个水分子能释放出一个电子,同时产生一种阳离子。产生的阳离子具有较强的氧化性,试写出该阳离子与SO2的水溶液反应的离子方程式
(3)水的性质中的一些特殊现象对于生命的存在意义非凡,请解释水的分解温度远高于其沸点的原
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有下列微粒:①CH4 ②CH2=CH2 ③CH≡CH ④NH3 ⑤NH4+ ⑥BF3 ⑦P4 ⑧H2O ⑨H2O2
(1)呈正四面体的是________ .
(2)中心原子轨道为sp3杂化的是________ ,为sp2杂化的是________ ,为sp杂化的是____ 。
(3)所有原子共平面的是________ ,共线的是________ 。
(4)含有极性键的极性分子是________ 。
(1)呈正四面体的是
(2)中心原子轨道为sp3杂化的是
(3)所有原子共平面的是
(4)含有极性键的极性分子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列几种常见物质:①CH3Cl、②O3、③P4、④C60、⑤CO2、⑥HCN、⑦H2O、⑧NH3、⑨BF3、⑩CH4。
(1)这几种物质中,含非极性共价键形成的是______________ (填序号,下同);属于非极性分子的是_______________ 。
(2)属于极性键形成的非极性分子是_______________ ;
(3)将 溶于水,破坏
溶于水,破坏 中的
中的_______________ 键,写出其电离方程式_______________ 。
(4)已知铁的电离能数据如下:
则,铁的第四电离能( )大于第三电离能(
)大于第三电离能( )的可能原因是:
)的可能原因是:_______________ 。
(1)这几种物质中,含非极性共价键形成的是
(2)属于极性键形成的非极性分子是
(3)将
 溶于水,破坏
溶于水,破坏 中的
中的(4)已知铁的电离能数据如下:
电离能/( |
|
|
|
| …… |
Fe | 759 | 1561 | 2597 | 5290 | …… |
 )大于第三电离能(
)大于第三电离能( )的可能原因是:
)的可能原因是:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氢键
(1)氢键是一种_____ 的分子间作用力。水分子之间的氢键是一个水分子中的____ 原子与另一个水分子的_____ 原子间形成的_____ 。
(2)水分子之间的氢键对水的物理性质的影响:①水的熔、沸点____ ;②水的比热容____ ;③水结成冰后,密度____ 。
(1)氢键是一种
(2)水分子之间的氢键对水的物理性质的影响:①水的熔、沸点
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】白铜是以镍为主要添加元素的铜基合金,呈银白色,有金属光泽,故名白铜。公元4世纪时东晋常璩的《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)文明中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)Ni2+的核外电子排布式为___________ ,3d能级上的未成对的电子数为___________ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是___________ 。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为___________ ,提供孤电子对的成键原子是___________ 。(用元素符号表示)
③与氨互为等电子体的一种阳离子为___________ (填化学式);氨极易溶于H2O,除因为它们都是极性分子外,还因为___________ 。
(3)单质铜及镍都是由___________ 键形成的晶体,元素铜与镍的第二电离能分别为:Icu=1959kJ/mol,INi=1753kJ/mol,Icu> INi的原因是___________ 。
(1)Ni2+的核外电子排布式为
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为
③与氨互为等电子体的一种阳离子为
(3)单质铜及镍都是由
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】有E、Q、T、X、Z五种前四周期元素,原子序数:E<Q<T<X<Z。E、Q、T三种元素的基态原子具有相同的能层和能级,且第一电离能I1(E)<I1(T)<I1(Q),其中基态Q原子的2p轨道处于半充满状态,且QT 与ET2具有相同的原子数和价电子数。X为周期表前四周期中电负性最小的元素,Z的原子序数为28。请回答下列问题(答题时如需表示具体元素,请用相应的元素符号):
与ET2具有相同的原子数和价电子数。X为周期表前四周期中电负性最小的元素,Z的原子序数为28。请回答下列问题(答题时如需表示具体元素,请用相应的元素符号):
(1)基态Z原子的核外电子排布式为_____ 。
(2)Q的简单氢化物极易溶于T的简单氢化物,其主要原因是_____ 、_____ 。
(3)化合物甲由T、X两种元素组成,其晶胞如图所示,则甲的化学式为_____ ,晶体类型为_____ 。

(4)化合物乙的晶胞如图所示,乙由E、Q两种元素组成,硬度超过金刚石。
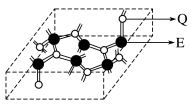
①乙的晶体硬度超过金刚石的原因是_____ 。
②乙的晶体中E、Q两种元素原子的杂化方式均为_____ 。
 与ET2具有相同的原子数和价电子数。X为周期表前四周期中电负性最小的元素,Z的原子序数为28。请回答下列问题(答题时如需表示具体元素,请用相应的元素符号):
与ET2具有相同的原子数和价电子数。X为周期表前四周期中电负性最小的元素,Z的原子序数为28。请回答下列问题(答题时如需表示具体元素,请用相应的元素符号):(1)基态Z原子的核外电子排布式为
(2)Q的简单氢化物极易溶于T的简单氢化物,其主要原因是
(3)化合物甲由T、X两种元素组成,其晶胞如图所示,则甲的化学式为

(4)化合物乙的晶胞如图所示,乙由E、Q两种元素组成,硬度超过金刚石。

①乙的晶体硬度超过金刚石的原因是
②乙的晶体中E、Q两种元素原子的杂化方式均为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】过渡晶体
(1)四类典型晶体是___________ 、___________ 、___________ 、___________ 。
(2)离子晶体和共价晶体的过渡标准是化学键中离子键成分的百分数,离子键成分的百分数大,作为___________ 处理,离子键成分的百分数小,作为___________ 处理。
(3)Na2O、MgO、Al2O3、SiO2、P2O5、SO3、Cl2O7七种氧化物中从左到右,离子键成分的百分数越来越___________ ,其中作为离子晶体处理的是___________ ;作为共价晶体处理的是___________ ;作为分子晶体处理的是___________ 。
(1)四类典型晶体是
(2)离子晶体和共价晶体的过渡标准是化学键中离子键成分的百分数,离子键成分的百分数大,作为
(3)Na2O、MgO、Al2O3、SiO2、P2O5、SO3、Cl2O7七种氧化物中从左到右,离子键成分的百分数越来越
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】聚合氯化铝晶体([Al2(OH)nCl(6-n)•XH2O]m)是一种高效无机水处理剂。它的制备原理是调节AlCl3溶液的pH,通过促进其水解而结晶析出。
回答下列问题:
(1)铝原子核外能量最高的电子有_____ 个。分析AlCl3熔点较低的原因(熔点:AlCl3—194℃,Al2O3—2054℃,NaCl—801℃)。____________________________________________________
(2)比较聚合氯化铝晶体中同周期两种元素的原子半径,并用原子结构知识说明理由。___________
(3)铝灰(主要成分为Al、Al2O3,另有少量CuO、SiO2、FeO和Fe2O3杂质)可制备AlCl3,如果先除去铝灰中的金属氧化物杂质可选用__________ (选填:“强碱”或“强酸”)。写出其中Al发生反应的离子方程式_______________________________ 。
(4)制备聚合氯化铝晶体,需严格控制溶液的pH在4.0~4.5才能使产率达到最大。结合AlCl3水解的离子方程式,用化学平衡移动原理解释控制pH在4.0~4.5之间的原因_______________________________
回答下列问题:
(1)铝原子核外能量最高的电子有
(2)比较聚合氯化铝晶体中同周期两种元素的原子半径,并用原子结构知识说明理由。
(3)铝灰(主要成分为Al、Al2O3,另有少量CuO、SiO2、FeO和Fe2O3杂质)可制备AlCl3,如果先除去铝灰中的金属氧化物杂质可选用
(4)制备聚合氯化铝晶体,需严格控制溶液的pH在4.0~4.5才能使产率达到最大。结合AlCl3水解的离子方程式,用化学平衡移动原理解释控制pH在4.0~4.5之间的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】请回答下列问题:
(1)由磷原子核形成的三种微粒:① 、②
、② 、③
、③ ,半径由大到小的顺序为
,半径由大到小的顺序为_______ (填标号,下同);再失去一个电子所需最低能量由大到小的顺序为_______ 。
(2)比较H-O-H键角大小;H3O+_______ H2O(填“>”、“<”或“=”)。
(3)胍(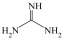 )分子中所有原子共平面,胍中N杂化方式为
)分子中所有原子共平面,胍中N杂化方式为_______ 。
(4)干冰晶体中,每个CO2周围等距离且紧邻的CO2有_______ 个;在冰晶体结构中,每个水分子最多与相邻的_______ 个水分子相连接。同为分子晶体,但干冰中CO2的配位数大于冰中水分子的配位数,其原因是_______ 。
(1)由磷原子核形成的三种微粒:①
 、②
、② 、③
、③ ,半径由大到小的顺序为
,半径由大到小的顺序为(2)比较H-O-H键角大小;H3O+
(3)胍(
 )分子中所有原子共平面,胍中N杂化方式为
)分子中所有原子共平面,胍中N杂化方式为(4)干冰晶体中,每个CO2周围等距离且紧邻的CO2有
您最近一年使用:0次

 )
)



