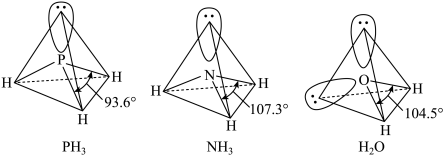
某物质可溶于水、乙醇,熔点为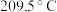 ,其结构简式如图所示,根据该物质结构回答下列问题:
,其结构简式如图所示,根据该物质结构回答下列问题:

(1) 元素在周期表的位置
元素在周期表的位置_______ , 原子的核外电子排布式为
原子的核外电子排布式为_______ , 元素位于周期表的
元素位于周期表的_______ 区。
(2)图中结构中 原子的杂化方式为
原子的杂化方式为_______ ;最外层达到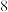 电子稳定结构的原子有
电子稳定结构的原子有_______ 个;。 键和
键和 键的个数比为
键的个数比为_______
(3)该物质的晶体类型为_______ ,该有机物可溶于水的原因是_______ 。
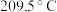 ,其结构简式如图所示,根据该物质结构回答下列问题:
,其结构简式如图所示,根据该物质结构回答下列问题:
(1)
 元素在周期表的位置
元素在周期表的位置 原子的核外电子排布式为
原子的核外电子排布式为 元素位于周期表的
元素位于周期表的(2)图中结构中
 原子的杂化方式为
原子的杂化方式为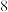 电子稳定结构的原子有
电子稳定结构的原子有 键和
键和 键的个数比为
键的个数比为(3)该物质的晶体类型为
更新时间:2021-02-03 11:45:42
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】盐酸氯丙嗪是一种多巴胺受体的阻断剂,临床有多种用途。化合物 是盐酸氯丙嗪制备的原料,可由化合物
是盐酸氯丙嗪制备的原料,可由化合物 和
和 在铜作催化剂条件下反应制得。
在铜作催化剂条件下反应制得。___________ 。
(2)1mol化合物 分子中含有σ键数目为
分子中含有σ键数目为___________ 。
(3)化合物 分子中sp3方式杂化的原子数目是
分子中sp3方式杂化的原子数目是___________ 。
(4)已知[Cu(NH3)4]SO4中[Cu(NH3)4]2+具有对称的空间构型,且当两个NH3被两个Cl-取代时,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为___________ (填序号)。
a.平面正方形 b.正四面体 c.三角锥型 d.V型
(5)已知在[Cu(NH3)4]SO4中溶液中加入少量NiSO4,会立即转化为[Ni(NH3)6]SO4中,由此可知Ni2+与NH3之间形成的化学键键能___________ (填“大于”或“小于”)Cu2+与NH3之间形成的化学键键能。[Cu(NH3)4]2+中存在的化学键类型有___________ 。
 是盐酸氯丙嗪制备的原料,可由化合物
是盐酸氯丙嗪制备的原料,可由化合物 和
和 在铜作催化剂条件下反应制得。
在铜作催化剂条件下反应制得。 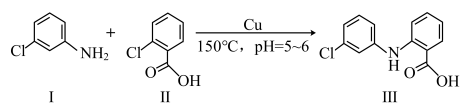
(2)1mol化合物
 分子中含有σ键数目为
分子中含有σ键数目为(3)化合物
 分子中sp3方式杂化的原子数目是
分子中sp3方式杂化的原子数目是(4)已知[Cu(NH3)4]SO4中[Cu(NH3)4]2+具有对称的空间构型,且当两个NH3被两个Cl-取代时,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为
a.平面正方形 b.正四面体 c.三角锥型 d.V型
(5)已知在[Cu(NH3)4]SO4中溶液中加入少量NiSO4,会立即转化为[Ni(NH3)6]SO4中,由此可知Ni2+与NH3之间形成的化学键键能
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】各题中的物质均由核电荷数为1~10的元素组成,按要求填写化学式:
(1)只有两个原子核和两个电子组成的分子是_______ ;
(2)最外层有5个电子的原子所形成的氢化物_______ ;
(3)由3个原子组成的电子总数为10的化合物是_______ ;
(4)离子化合物AB中阴阳离子的电子层结构相同,则化合物AB是_______ 。
(1)只有两个原子核和两个电子组成的分子是
(2)最外层有5个电子的原子所形成的氢化物
(3)由3个原子组成的电子总数为10的化合物是
(4)离子化合物AB中阴阳离子的电子层结构相同,则化合物AB是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】 (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(1)氨硼烷的结构
①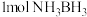 中
中 键的数目为
键的数目为___________ 。
② 熔点104℃,
熔点104℃, 熔点
熔点 ℃。两者熔点差异较大的原因是
℃。两者熔点差异较大的原因是___________ 。
(2)氨硼烷水解释氢
①氨硼烷水解释氢需要在金属型催化剂(如Cr、Pt等)催化下进行。写出基态Cr原子的价电子排布式:___________ 。
②铬的甲、乙两种晶胞(所示图形为正方体)结构示意如题图所示。甲、乙晶胞所含铬原子个数比为___________ 。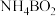 ,写出水解释氢的化学方程式
,写出水解释氢的化学方程式___________ 。
(3)氨硼烷热分解释氢
①氨硼烷受热时固体残留率随温度的变化如题图所示。110℃时残留固体的化学式可能为___________ 。 键∶
键∶ 键=
键=___________ 。
 (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。(1)氨硼烷的结构
| 元素 | H | B | N |
| 电负性 | 2.1 | 2.0 | 3.0 |
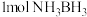 中
中 键的数目为
键的数目为②
 熔点104℃,
熔点104℃, 熔点
熔点 ℃。两者熔点差异较大的原因是
℃。两者熔点差异较大的原因是(2)氨硼烷水解释氢
①氨硼烷水解释氢需要在金属型催化剂(如Cr、Pt等)催化下进行。写出基态Cr原子的价电子排布式:
②铬的甲、乙两种晶胞(所示图形为正方体)结构示意如题图所示。甲、乙晶胞所含铬原子个数比为
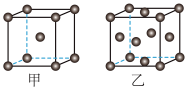
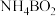 ,写出水解释氢的化学方程式
,写出水解释氢的化学方程式(3)氨硼烷热分解释氢
①氨硼烷受热时固体残留率随温度的变化如题图所示。110℃时残留固体的化学式可能为
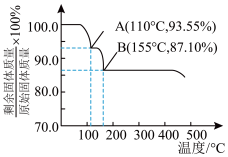
 键∶
键∶ 键=
键=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据要求回答下列问题:
(1) 是有机合成中常用的还原剂,
是有机合成中常用的还原剂, 中阴离子的空间构型是
中阴离子的空间构型是_______ ,中心原子的杂化类型为_______ , 中,存在
中,存在_______ (填标号)。
A.离子键 B. 键 C.
键 C. 键 D.配位键
键 D.配位键
(2)碳氧化物、氨氧化物、二氧化硫的处理和应用是世界各国研究的热点问题。 的VSEPR模型为
的VSEPR模型为_______ ; 的中心原子的杂化类型为
的中心原子的杂化类型为_______ ; 与
与 互为等电子体,且
互为等电子体,且 中O只与一个N相连,则
中O只与一个N相连,则 的空间构型为
的空间构型为_______ ,分子中的 键和
键和 键数目之比是
键数目之比是_______ 。
(3)某研究小组将平面形的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如图所示。
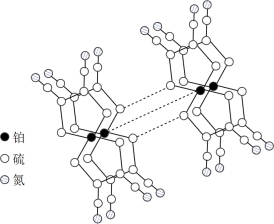
①“分子金属”可以导电,是因为_______ 能沿着其中的金属原子链流动。
②“分子金属”中,铂原子不是采取 杂化,其理由是
杂化,其理由是_______ 。
(1)
 是有机合成中常用的还原剂,
是有机合成中常用的还原剂, 中阴离子的空间构型是
中阴离子的空间构型是 中,存在
中,存在A.离子键 B.
 键 C.
键 C. 键 D.配位键
键 D.配位键(2)碳氧化物、氨氧化物、二氧化硫的处理和应用是世界各国研究的热点问题。
 的VSEPR模型为
的VSEPR模型为 的中心原子的杂化类型为
的中心原子的杂化类型为 与
与 互为等电子体,且
互为等电子体,且 中O只与一个N相连,则
中O只与一个N相连,则 的空间构型为
的空间构型为 键和
键和 键数目之比是
键数目之比是(3)某研究小组将平面形的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如图所示。

①“分子金属”可以导电,是因为
②“分子金属”中,铂原子不是采取
 杂化,其理由是
杂化,其理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】共价键的分类(以碳原子之间成键为例)
| 分类依据 | 成键结构 |  键与 键与 键 键 | 说明 |
| 单键 | 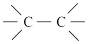 | 碳碳之间形成一个 键 键 | 所有的单键都是 键 键 |
| 双键 |  | 碳碳之间形成1个 键、1个 键、1个 键 键 | 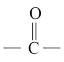 、 、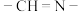 等双键中形成1个 等双键中形成1个 键、1个 键、1个 键 键 |
| 三键 | 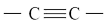 | 碳碳之间形成1个 键、2个 键、2个 键 键 |  等三键之间形成1个 等三键之间形成1个 键、2个 键、2个 键 键 |
| 拓展 | 分子中大 键可用符号Ⅱm表示,其中m代表参与形成大 键可用符号Ⅱm表示,其中m代表参与形成大 键的原子数,n代表参与形成大 键的原子数,n代表参与形成大 键的电子数(如苯分子中的大 键的电子数(如苯分子中的大 键可表示为 键可表示为 ),则 ),则   : : : : : : | ||
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】水是地球上最常见的物质之一,是所有生命生存的重要资源。
(1)水溶液中存在H3O+离子,写出该微粒的结构式____________________ (标出配位键)。
(2)科学家发现在特殊条件下,水能表现出许多种有趣的结构和性质
①一定条件下给水施加一个弱电场,常温常压下水结成冰,俗称“热冰”,其计算机模拟图如下:
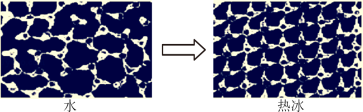
使水结成“热冰”采用“弱电场”的条件,说明水分子是______ 分子(填“极性”或“非极性”)。下列物质熔化时,所克服的微粒间的作用与“热冰”熔化时所克服的作用力类型完全相同的是______ 。
A.固态氨 B.食盐 C.干冰 D.金刚石
②用高能射线照射液态水时,一个水分子能释放出一个电子,同时产生一种阳离子。产生的阳离子具有较强的氧化性,试写出该阳离子与SO2的水溶液反应的离子方程式____________ ;该阳离子还能与水作用生成羟基,经测定此时的水具有酸性,写出该过程的离子方程式____ 。
(3)水的性质中的一些特殊现象对于生命的存在意义非凡,请解释水的分解温度远高于其沸点的原____________
(1)水溶液中存在H3O+离子,写出该微粒的结构式
(2)科学家发现在特殊条件下,水能表现出许多种有趣的结构和性质
①一定条件下给水施加一个弱电场,常温常压下水结成冰,俗称“热冰”,其计算机模拟图如下:

使水结成“热冰”采用“弱电场”的条件,说明水分子是
A.固态氨 B.食盐 C.干冰 D.金刚石
②用高能射线照射液态水时,一个水分子能释放出一个电子,同时产生一种阳离子。产生的阳离子具有较强的氧化性,试写出该阳离子与SO2的水溶液反应的离子方程式
(3)水的性质中的一些特殊现象对于生命的存在意义非凡,请解释水的分解温度远高于其沸点的原
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
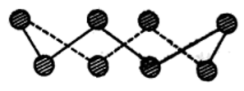
【推荐1】(1)S单质的常见形式为 ,其环状结构如图所示,S原子采用的轨道杂化方式是
,其环状结构如图所示,S原子采用的轨道杂化方式是_______ 。
(2)现有H、N、O、S、Cu几种元素,回答下列问题。
①氢元素和N、O、S、Cu形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为_______ ;分子中既含有极性共价键又含有非极性共价键的化合物是_______ (填化学式,写出两种)。
②这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是_______ (填化学式,下同);酸根呈三角锥形的酸是_______ 。
 ,其环状结构如图所示,S原子采用的轨道杂化方式是
,其环状结构如图所示,S原子采用的轨道杂化方式是
(2)现有H、N、O、S、Cu几种元素,回答下列问题。
①氢元素和N、O、S、Cu形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为
②这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素X的原子最外层电子排布式为nsnnpn+1。试解答下列各题:
(1)元素X的原子最外层电子排布式中的n=_______ ;原子中能量最高的是_______ 电子,其电子云在空间有_______ 种伸展方向,原子轨道呈_______ 形。
(2)元素X的名称是_______ ;它的氢化物的电子式是_______ ;该氢化物分子结构呈_______ 形,其中X原子的VSEPR模型为_______ ;该氢化物分子可以与H+以_______ 结合成阳离子,该阳离子与Cl-可以形成_______ 化合物。
(1)元素X的原子最外层电子排布式中的n=
(2)元素X的名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】X、Y、Z、W、Q为元素周期表中前四周期的元素,其元素性质和原子结构如表所述。
回答下列问题:
(1)Y位于元素周期表的___________ 区,基态Z原子的价层电子排布图为___________ 。
(2)与W同周期且第一电离能比其大的元素为___________ (填元素符号),W与X形成的简单化合物分子中,中心原子的VSEPR模型为___________ 。
(3)基态Q原子有___________ 种空间运动状态,Q与X形成的简单化合物和W与X形成的简单化合物在水中溶解度较大的为___________ (写分子式),原因为___________ 。
(4)W和Q形成的某种分子的空间构型为三角锥形,其中心原子的杂化轨道类型为___________ ,该分子为___________ (填“极性”或“非极性”)分子。
| 元素 | 元素性质或原子结构 |
| X | 基态原子只有一种形状的轨道填有电子,且易形成共价键 |
| Y | 基态原子核外的M层中只有两对成对电子 |
| Z | 前四周期元素中基态原子的未成对电子数最多 |
| W | 与Y同周期,且在该周期元素中第一电离能由大到小排第三位 |
| Q | 元素周期表中电负性最大的元素 |
回答下列问题:
(1)Y位于元素周期表的
(2)与W同周期且第一电离能比其大的元素为
(3)基态Q原子有
(4)W和Q形成的某种分子的空间构型为三角锥形,其中心原子的杂化轨道类型为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氧的常见氢化物有H2O与H2O2。
(1)纯净H2O2为浅蓝色粘稠液体,除相对分子质量的影响外,其沸点(423K)明显高于水的原因为_______ 。
(2) H2O2既有氧化性也有还原性,写出一个离子方程式其中H2O2在反应中仅体现还原性_______ 。
(1)纯净H2O2为浅蓝色粘稠液体,除相对分子质量的影响外,其沸点(423K)明显高于水的原因为
(2) H2O2既有氧化性也有还原性,写出一个离子方程式其中H2O2在反应中仅体现还原性
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)1g CH4充分燃烧生成液态水,放出55.625kJ的热,写出CH4燃烧的热化学方程式:
__________________________________________ 。
(2)比较下列物质的性质,(填“>”或“<”)
①非金属性 C____ S。
②沸点 H2O____ H2S。
(2)比较下列物质的性质,(填“>”或“<”)
①非金属性 C
②沸点 H2O
您最近一年使用:0次