[Cr(NH3)3(H2O)2Cl]2+中配体分子NH3、H2O以及分子PH3的空间结构和相应的键角如图所示。
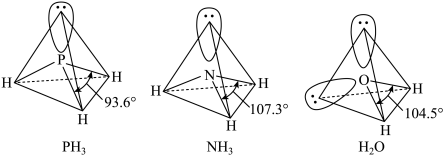
PH3中P的杂化类型为_______ ,NH3的沸点比PH3的_______ ,原因是_______ ;H2O的键角小于NH3的键角,分析原因_______ 。

PH3中P的杂化类型为
2022高三·全国·专题练习 查看更多[3]
(已下线)第30讲 分子结构与性质(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第五章 物质结构与性质 元素周期律 第30讲 配合物 分子间作用力 超分子(已下线)考点42 分子结构与性质(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
更新时间:2022-10-17 22:20:06
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】O3分子的立体构型为________ 。根据表中数据判断氧原子之间的共价键最稳定的粒子是______ 。
| 粒子 | O2 | O | O3 |
| 键长/pm | 121 | 126 | 128 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】2022年以来,全球化石能源价格一路飙升,对全球经济复苏产生巨大影响。氢能源是一种不依赖化石燃料的储量丰富的清洁能源。
(1)电解水产氢是目前较为理想的制氢技术,这项技术的广泛应用一直被高价的贵金属催化剂所制约。我国科学家开发了一种负载氧化镍纳米晶粒的聚合物氮化碳二维纳米材料,大幅提高了催化效率。
①基态Ni原子的价电子排布式为_______ ,该元素在元素周期表中的位置是_______ 。
②C、N、O的电负性的由大到小的顺序是_______ 。
③为寻找更多的金属催化剂,科学家从众多金属元素中选取Co、Fe、Cu进行了相关研究,并取得了成功。选取这三种金属进行相关研究的原因可能是_______ 。
(2)开发新型储氢材料是氢能利用的重要研究方向。氨硼烷(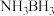 )是一种潜在的储氢材料,可由
)是一种潜在的储氢材料,可由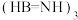 (俗称无机苯,结构为平面六元环状,如图所示:
(俗称无机苯,结构为平面六元环状,如图所示: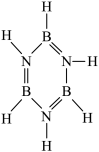 )通过如下反应制得:
)通过如下反应制得: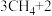
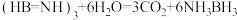 。
。
①请解释 、
、 、
、 的键角大小顺序
的键角大小顺序_______ 。
②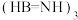 中B、N原子的杂化轨道类型分别为
中B、N原子的杂化轨道类型分别为_______ 。
(1)电解水产氢是目前较为理想的制氢技术,这项技术的广泛应用一直被高价的贵金属催化剂所制约。我国科学家开发了一种负载氧化镍纳米晶粒的聚合物氮化碳二维纳米材料,大幅提高了催化效率。
①基态Ni原子的价电子排布式为
②C、N、O的电负性的由大到小的顺序是
③为寻找更多的金属催化剂,科学家从众多金属元素中选取Co、Fe、Cu进行了相关研究,并取得了成功。选取这三种金属进行相关研究的原因可能是
(2)开发新型储氢材料是氢能利用的重要研究方向。氨硼烷(
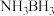 )是一种潜在的储氢材料,可由
)是一种潜在的储氢材料,可由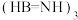 (俗称无机苯,结构为平面六元环状,如图所示:
(俗称无机苯,结构为平面六元环状,如图所示: )通过如下反应制得:
)通过如下反应制得: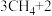
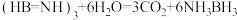 。
。①请解释
 、
、 、
、 的键角大小顺序
的键角大小顺序②
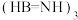 中B、N原子的杂化轨道类型分别为
中B、N原子的杂化轨道类型分别为
您最近一年使用:0次
【推荐3】火药的爆炸反应原理为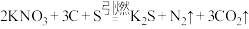 。请回答下列问题:
。请回答下列问题:
(1)基态 原子核外有
原子核外有___________ 种空间运动状态的电子。
(2)原子核外运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数可能的代数和为
表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数可能的代数和为_______ 。
(3)基态钾离子的电子占据的最高能层符号是___________ ; 与
与 具有相同的核外电子排布,
具有相同的核外电子排布,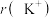 小于
小于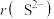 ,原因是
,原因是___________ 。
(4)元素的气态基态原子得到一个电子形成气态负一价离子时所放出的能量称为第一电子亲和能( )。MgO的Born-Haber循环(原理为盖斯定律)如图所示。
)。MgO的Born-Haber循环(原理为盖斯定律)如图所示。

由图可知,Mg原子的第二电离能为___________ kJ/mol;O=O键的键能为___________ kJ/mol;氧原子的第一电子亲和能为___________ kJ/mol(取正值)。
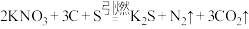 。请回答下列问题:
。请回答下列问题:(1)基态
 原子核外有
原子核外有(2)原子核外运动的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数可能的代数和为
表示称为电子的自旋磁量子数。对于基态的N原子,其价电子自旋磁量子数可能的代数和为(3)基态钾离子的电子占据的最高能层符号是
 与
与 具有相同的核外电子排布,
具有相同的核外电子排布,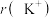 小于
小于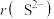 ,原因是
,原因是(4)元素的气态基态原子得到一个电子形成气态负一价离子时所放出的能量称为第一电子亲和能(
 )。MgO的Born-Haber循环(原理为盖斯定律)如图所示。
)。MgO的Born-Haber循环(原理为盖斯定律)如图所示。
由图可知,Mg原子的第二电离能为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上可以用NaCl溶液制取重要的化工原料纯碱,此化工流程还需要一定量的CO2和NH3。
(1)NH3的分子构型是_______ ,用电子式表示NH3分子的形成过程_______ 。
(2)工业上合成氨气需要使用氮气,氮原子的结构示意图是_______ ,氮气分子的结构式是_______ 。
(3)羰基硫COS的分子构型与CO2分子相似,可以看作CO2分子中的1个氧原子被硫原子取代。COS的电子式是_______ ,它是_______ (填“极性”或“非极性”)分子。
(1)NH3的分子构型是
(2)工业上合成氨气需要使用氮气,氮原子的结构示意图是
(3)羰基硫COS的分子构型与CO2分子相似,可以看作CO2分子中的1个氧原子被硫原子取代。COS的电子式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)在 分子中,
分子中,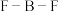 的键角是
的键角是______ ,硼原子的杂化轨道类型为______ , 和过量
和过量 作用可生成
作用可生成 ,
, 的空间结构为
的空间结构为______ 。
(2)肼( )分子可视为
)分子可视为 分子中的1个氢原子被
分子中的1个氢原子被 (氨基)取代形成的另一种氮的氢化物。
(氨基)取代形成的另一种氮的氢化物。 分子的空间结构是
分子的空间结构是______ ; 分子中氮原子的杂化轨道类型是
分子中氮原子的杂化轨道类型是______ 。
(3) 可与
可与 形成
形成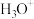 ,
,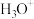 中氧原子采用
中氧原子采用______ 杂化。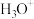 中
中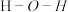 键角比
键角比 中
中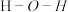 键角大,原因为
键角大,原因为__________________ 。
(4) 的空间结构是
的空间结构是______ ,其中硫原子的杂化轨道类型是______ 。
 分子中,
分子中,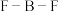 的键角是
的键角是 和过量
和过量 作用可生成
作用可生成 ,
, 的空间结构为
的空间结构为(2)肼(
 )分子可视为
)分子可视为 分子中的1个氢原子被
分子中的1个氢原子被 (氨基)取代形成的另一种氮的氢化物。
(氨基)取代形成的另一种氮的氢化物。 分子的空间结构是
分子的空间结构是 分子中氮原子的杂化轨道类型是
分子中氮原子的杂化轨道类型是(3)
 可与
可与 形成
形成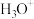 ,
,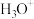 中氧原子采用
中氧原子采用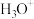 中
中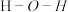 键角比
键角比 中
中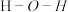 键角大,原因为
键角大,原因为(4)
 的空间结构是
的空间结构是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】请按要求回答下列问题:
(1)符号“3px”没有给出的信息是___________。
(2)某元素基态原子4s轨道上有1个电子,则该元素基态原子价电子排布不可能是___________。
(3)X元素的原子最外层电子排布式为(n+1)sn(n+1)pn+1,则X的氢化物的化学式是___________。
(4)下列比较正确的是___________ 。
A.酸性:H3PO4<H3AsO4 B.键角:H2O<NH3 C.离子半径:r(Al3+)>r(O2-)
(5)下列实验事实不能用氢键来解释的是___________。
(1)符号“3px”没有给出的信息是___________。
| A.能层 | B.能级 | C.电子云在空间的伸展方向 | D.电子的自旋方向 |
| A.4s1 | B.3p64s1 | C.3d54s1 | D.3d104s1 |
| A.HX | B.H2X | C.XH3 | D.XH4 |
A.酸性:H3PO4<H3AsO4 B.键角:H2O<NH3 C.离子半径:r(Al3+)>r(O2-)
(5)下列实验事实不能用氢键来解释的是___________。
| A.CH4比SiH4稳定 |
| B.乙醇能与水以任意比互溶 |
| C.邻羟基苯甲醛的沸点低于对羟基苯甲醛 |
| D.接近沸点的水蒸气的相对分子质量测量值大于18 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1)A元素次外层电子数是最外层电子数的 ,其外围电子排布图是
,其外围电子排布图是__________ 。
(2)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是____ ,价层电子排布式_________ ,在元素周期表中的位置是____________ 。
(3)C元素基态原子的电子排布图是下图中的____ (填序号),另一个不能作为基态原子的电子排布图因为它不符合__ (填序号)。
①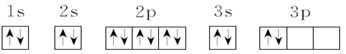
②
A.能量最低原理 B.泡利原理 C.洪特规则
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能(设为E)。如图所示:
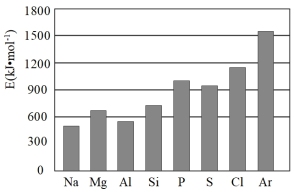
①同周期内,随着原子序数的增大,E值变化的总趋势是____ ;
②根据图中提供的信息,可推断出E氧____ E氟(填“>”“<”或“=”,下同);
③根据第一电离能的含义和元素周期律,可推断出E镁___ E钙。
(5)判断BCl3分子的空间构型、中心原子成键时采取的杂化轨道类型及分子中共价键的键角:________ 、___________ 、____________ 。
(1)A元素次外层电子数是最外层电子数的
 ,其外围电子排布图是
,其外围电子排布图是(2)B是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是
(3)C元素基态原子的电子排布图是下图中的
①

②

A.能量最低原理 B.泡利原理 C.洪特规则
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能(设为E)。如图所示:

①同周期内,随着原子序数的增大,E值变化的总趋势是
②根据图中提供的信息,可推断出E氧
③根据第一电离能的含义和元素周期律,可推断出E镁
(5)判断BCl3分子的空间构型、中心原子成键时采取的杂化轨道类型及分子中共价键的键角:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知:硫酸铜溶液中滴入氨基乙酸钠(H2N-CH2-COONa)即可得到配合物A。其结构如图所示:
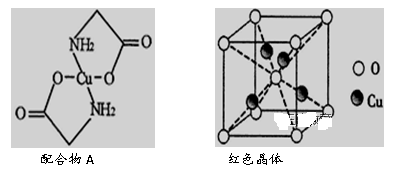
(1)Cu元素基态原子的外围电子排布式为______________ 。
(2)元素C、N、O的第一电离能由大到小排列顺序为_______________ 。
(3)配合物A中碳原子的轨道杂化类型为_______________________ 。
(4)1mol氨基乙酸钠(H2N-CH2-COONa)含有 键的数目为
键的数目为____________ mol。
(5)氨基乙酸钠分解产物之一为二氧化碳。写出二氧化碳的一种等电子体:____________ (写化学式)。
(6)已知:硫酸铜灼烧可以生成一种红色晶体,其结构如图所示,则该化合物的化学式是_________ 。

(1)Cu元素基态原子的外围电子排布式为
(2)元素C、N、O的第一电离能由大到小排列顺序为
(3)配合物A中碳原子的轨道杂化类型为
(4)1mol氨基乙酸钠(H2N-CH2-COONa)含有
 键的数目为
键的数目为(5)氨基乙酸钠分解产物之一为二氧化碳。写出二氧化碳的一种等电子体:
(6)已知:硫酸铜灼烧可以生成一种红色晶体,其结构如图所示,则该化合物的化学式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1) 是一种常用溶剂,每个
是一种常用溶剂,每个 分子中存在
分子中存在___________ 个 键。在H-S、H-Cl两种共价键中,化学键的极性较大的是
键。在H-S、H-Cl两种共价键中,化学键的极性较大的是___________ ,键长较长的是___________ 。
(2)水与 中,分子极性较小的是
中,分子极性较小的是___________ (填分子式)。
(3) 与
与 分子的空间结构分别是
分子的空间结构分别是___________ 和___________ ;相同条件下两者在水中的溶解度较大的是___________ (写分子式),理由是___________ 。
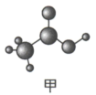
(4)醋酸分子的球棍模型如图甲所示。在醋酸分子中,碳原子的轨道杂化类型有___________ 。
 是一种常用溶剂,每个
是一种常用溶剂,每个 分子中存在
分子中存在 键。在H-S、H-Cl两种共价键中,化学键的极性较大的是
键。在H-S、H-Cl两种共价键中,化学键的极性较大的是(2)水与
 中,分子极性较小的是
中,分子极性较小的是(3)
 与
与 分子的空间结构分别是
分子的空间结构分别是(4)醋酸分子的球棍模型如图甲所示。在醋酸分子中,碳原子的轨道杂化类型有

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】CH3CH2OH、CH3COOH和NaOH都是中学化学的常用试剂。请回答下列问题:
⑴①乙酸和甲酸甲酯互为同分异构体,但前者的熔点高于后者。原因是____________ 。
②在油脂的皂化反应中,加入乙醇能加快反应的速率。原因是________________ 。
③将在空气中灼烧成红热的铜丝伸入无水乙醇中,铜丝立即变为红色。请用化学方程式表示铜丝变红的原因______________________________________ 。
⑵用0.1mol/LNaOH溶液测定CH3COOH的物质的量浓度,碱式滴定管用标准溶液润洗后即加入标准溶液,经“必要”操作后,进行滴定。
①此处的“必要”操作是指____________________________________________ 。
②选用的指示剂是________ 。
③滴点终点时溶液中离子浓度由大到小的顺序是__________________ 。
⑶无水醋酸钠和NaOH固体混合加热时能生成CH4,反应的化学方程式是___ ,利用此反应制备CH4的装置与制备___ 相同。
⑷乙醇和乙酸在浓硫酸存在下反应生成具有香味的物质,反应的化学方程式是____ 。反应类型是_______ ,用浓硫酸作催化剂可能造成_____________________ 等问题(答两条即可)。
⑴①乙酸和甲酸甲酯互为同分异构体,但前者的熔点高于后者。原因是
②在油脂的皂化反应中,加入乙醇能加快反应的速率。原因是
③将在空气中灼烧成红热的铜丝伸入无水乙醇中,铜丝立即变为红色。请用化学方程式表示铜丝变红的原因
⑵用0.1mol/LNaOH溶液测定CH3COOH的物质的量浓度,碱式滴定管用标准溶液润洗后即加入标准溶液,经“必要”操作后,进行滴定。
①此处的“必要”操作是指
②选用的指示剂是
③滴点终点时溶液中离子浓度由大到小的顺序是
⑶无水醋酸钠和NaOH固体混合加热时能生成CH4,反应的化学方程式是
⑷乙醇和乙酸在浓硫酸存在下反应生成具有香味的物质,反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请回答:
(1)标准状况下,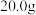 氟化氢气体的体积明显小于
氟化氢气体的体积明显小于 ,其原因是
,其原因是_______ 。
(2)碳元素的单质性质差异很大,金刚石硬度大,可用于研磨和切割;足球烯( )硬度小,是制作高级润滑剂的重要原料。两种碳单质性能差异明显的原因是
)硬度小,是制作高级润滑剂的重要原料。两种碳单质性能差异明显的原因是_______ 。
(1)标准状况下,
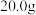 氟化氢气体的体积明显小于
氟化氢气体的体积明显小于 ,其原因是
,其原因是(2)碳元素的单质性质差异很大,金刚石硬度大,可用于研磨和切割;足球烯(
 )硬度小,是制作高级润滑剂的重要原料。两种碳单质性能差异明显的原因是
)硬度小,是制作高级润滑剂的重要原料。两种碳单质性能差异明显的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下列各物质或微粒.A、H2SO4 B、SO3 C、35Cl D、C60 E、H2O F、Ba(OH)2 G、C70 H、37Cl I、NH3 J、CCl4 K、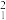 H2 L、HF M、
H2 L、HF M、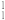 H2 N、Cl2 P、盐酸
H2 N、Cl2 P、盐酸
(1)属于强电解质的是_________________________ ;
(2)属于非电解质的是_________________________ ;
(3)属于同素异形体的是_______________________ ;
(4)互为同位素的是___________________________ ;
(5)自身分子间可形成氢键的是_________________ ;
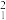 H2 L、HF M、
H2 L、HF M、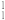 H2 N、Cl2 P、盐酸
H2 N、Cl2 P、盐酸(1)属于强电解质的是
(2)属于非电解质的是
(3)属于同素异形体的是
(4)互为同位素的是
(5)自身分子间可形成氢键的是
您最近一年使用:0次



