氧的常见氢化物有H2O与H2O2。
(1)纯净H2O2为浅蓝色粘稠液体,除相对分子质量的影响外,其沸点(423K)明显高于水的原因为_______ 。
(2) H2O2既有氧化性也有还原性,写出一个离子方程式其中H2O2在反应中仅体现还原性_______ 。
(1)纯净H2O2为浅蓝色粘稠液体,除相对分子质量的影响外,其沸点(423K)明显高于水的原因为
(2) H2O2既有氧化性也有还原性,写出一个离子方程式其中H2O2在反应中仅体现还原性
2021·浙江绍兴·二模 查看更多[2]
更新时间:2021-04-11 19:27:00
|
相似题推荐
填空题
|
适中
(0.64)
【推荐1】已知:氧化性:KMnO4>HNO3;Bi位于周期表中ⅤA族,+3价较稳定,Bi2O3为碱性氧化物,Bi3+的溶液为无色。取一定量硝酸酸化的Mn(NO3)2溶液依次进行下列实验,现象记录如下:
①向其中加入适量的NaBiO3,溶液变为紫红色。②继续滴加适量H2O2,紫红色褪去,并有气泡产生。③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
回答下列问题:
(1)写出实验①反应的离子方程式:________________________________________ 。
(2)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为________________________________ 。
(3)向反应③得到的溶液中通入SO2气体,看到的现象是____________________________________________________________ 。
(4)若实验②放出了336 mL气体(标准状况),则反应①被氧化的Mn(NO3)2为_______ mol。
①向其中加入适量的NaBiO3,溶液变为紫红色。②继续滴加适量H2O2,紫红色褪去,并有气泡产生。③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
回答下列问题:
(1)写出实验①反应的离子方程式:
(2)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为
(3)向反应③得到的溶液中通入SO2气体,看到的现象是
(4)若实验②放出了336 mL气体(标准状况),则反应①被氧化的Mn(NO3)2为
您最近一年使用:0次
【推荐2】(1)从氧化还原的角度分析水在下列化学反应中的作用(从氧化剂、还原剂角度分析)。
①电解水:_____________________________________________________ 。
②钠和水的反应(2Na+2H2O=2NaOH+H2↑):_______________________________ 。
③氟气和水反应(2F2+2H2O=4HF+O2):_______________________________ 。
④氯气和水反应(Cl2+H2O=HCl+HClO):______________________________ 。
(2)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应体系中还原产物是________ ;若反应中转移了0.3 mol电子,则氧化产物的质量是________ g。
(3)将少量Cl2通入FeBr2的溶液中,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl−,这个事实说明具有还原性的粒子还原性强弱顺序为____________ 。足量Cl2通入FeBr2溶液中发生反应的离子方程式为________________ 。
①电解水:
②钠和水的反应(2Na+2H2O=2NaOH+H2↑):
③氟气和水反应(2F2+2H2O=4HF+O2):
④氯气和水反应(Cl2+H2O=HCl+HClO):
(2)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应体系中还原产物是
(3)将少量Cl2通入FeBr2的溶液中,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl−,这个事实说明具有还原性的粒子还原性强弱顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)氮元素在元素周期表中的位置为_______ 。
(2)氮元素原子核外电子排布式为_______ ,有_______ 种形状的电子云。
(3)氮元素气态氢化物的电子式为_______ 。
与氮元素同主族的磷元素化合物有如下反应,其中反应物有:PH3、H2SO4、KClO3;生成物有:K2SO4、H3PO4、H2O 和一种未知物质 X。
(4)已知 KClO3 在反应中得到电子,则该反应的还原剂是_______ 。
(5)已知 0.2mol KClO3 在反应中得到 1mol 电子生成 X,则 X 的化学式为_______ 。
(6)完成并配平上述反应的化学方程式,标出电子转移方向和数目:_______ 。
(7)根据上述反应可推知_______ 。(填序号)
A.氧化性:KClO3 > H3PO4 B.氧化性:KClO3 > H2O
C.还原性:PH3 > X D.还原性:PH3 > K2SO4
(8)在该反应中转移电子 2mol 时,生成H3PO4_______ mol。
(2)氮元素原子核外电子排布式为
(3)氮元素气态氢化物的电子式为
与氮元素同主族的磷元素化合物有如下反应,其中反应物有:PH3、H2SO4、KClO3;生成物有:K2SO4、H3PO4、H2O 和一种未知物质 X。
(4)已知 KClO3 在反应中得到电子,则该反应的还原剂是
(5)已知 0.2mol KClO3 在反应中得到 1mol 电子生成 X,则 X 的化学式为
(6)完成并配平上述反应的化学方程式,标出电子转移方向和数目:
(7)根据上述反应可推知
A.氧化性:KClO3 > H3PO4 B.氧化性:KClO3 > H2O
C.还原性:PH3 > X D.还原性:PH3 > K2SO4
(8)在该反应中转移电子 2mol 时,生成H3PO4
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)已知:用毛笔蘸取少量30%的FeCl3溶液在铜片上写一个“Cu”,放置片刻后用少量蒸馏水冲洗铜片后,在铜片上会出现凹凸的“Cu”,写出该反应的离子方程式:___________ 。
(2)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,其反应可表示为:Fe(OH)3+ClO-+OH-= +Cl-+□请将该方程补充并配平,并在方程式上面用“双线桥”标出电子转移的方向与数目
+Cl-+□请将该方程补充并配平,并在方程式上面用“双线桥”标出电子转移的方向与数目________ 。
(3)某同学在做Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的一次实验中,用过量的稀硝酸(其密度为1.05 g/mL,HNO3的质量分数为12%)跟一定量的铁片反应,产生了标准状况下0.56 L的一氧化氮,该稀硝酸的物质的量浓度为___________ ,被还原的HNO3的物质的量为___________ ,转移电子的数目为___________ 。
(2)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,其反应可表示为:Fe(OH)3+ClO-+OH-=
 +Cl-+□请将该方程补充并配平,并在方程式上面用“双线桥”标出电子转移的方向与数目
+Cl-+□请将该方程补充并配平,并在方程式上面用“双线桥”标出电子转移的方向与数目(3)某同学在做Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的一次实验中,用过量的稀硝酸(其密度为1.05 g/mL,HNO3的质量分数为12%)跟一定量的铁片反应,产生了标准状况下0.56 L的一氧化氮,该稀硝酸的物质的量浓度为
您最近一年使用:0次
【推荐2】I、某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是_________________ 。
II、下列三个氧化还原反应中,氧化性最强的物质是________ 。
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③ KMnO4+ HCl(浓) → KCl+ MnCl2+ Cl2↑+ H2O(未配平)
请配平③的化学反应方程式:
__ KMnO4+__ HCl(浓)=__ KCl+__ MnCl2+__ Cl2↑+__ H2O
III、已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO↑+ 4H2O
(1)用双线桥 法分析上述反应(只需标出电子得失的方向和数目)_______
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO↑+ 4H2O
(2)上述反应中氧化剂是___________ ,氧化产物是_____________ 。硝酸没有全部参加氧化还原反应,没有参加氧化还原反应的硝酸占总硝酸的_______ 。
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是
II、下列三个氧化还原反应中,氧化性最强的物质是
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③ KMnO4+ HCl(浓) → KCl+ MnCl2+ Cl2↑+ H2O(未配平)
请配平③的化学反应方程式:
III、已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO↑+ 4H2O
(1)用
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO↑+ 4H2O
(2)上述反应中氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求写方程式。
(1)完成以下氧化还原反应的离子方程式:_______

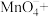

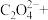
 ______=
______=
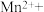

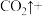
 ______
______
(2) 可以作为水溶液中
可以作为水溶液中 歧化反应的催化剂,可能的催化过程如下。将ⅱ补充完整。
歧化反应的催化剂,可能的催化过程如下。将ⅱ补充完整。
ⅰ.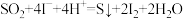
ⅱ.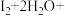 ______= ______+______
______= ______+______ ,
,________
(3)高铁酸钾( )是一种强氧化剂,可作为水处理剂和高容量电池材料。
)是一种强氧化剂,可作为水处理剂和高容量电池材料。 和KClO在强碱性条件下反应可制取
和KClO在强碱性条件下反应可制取 ,其反应的离子方程式为:
,其反应的离子方程式为:______ 。
(4)往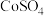 溶液中滴加
溶液中滴加 制备
制备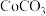 固体,写出该过程中发生反应的离子方程式
固体,写出该过程中发生反应的离子方程式______ 。
(5)NaH在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为 ),脱锈过程发生反应的化学方程式
),脱锈过程发生反应的化学方程式______ 。
(6)元素镍(Ni)在溶液中 价极不稳定,主要以
价极不稳定,主要以 (绿色)、
(绿色)、 (蓝色)、
(蓝色)、 (橙黄色)、
(橙黄色)、 (深红色)等形式存在。
(深红色)等形式存在。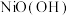 为难溶于水的黑色固体,其溶于浓盐酸并形成绿色溶液,其离子方程式为
为难溶于水的黑色固体,其溶于浓盐酸并形成绿色溶液,其离子方程式为___________________ 。
(1)完成以下氧化还原反应的离子方程式:

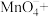

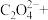
 ______=
______=
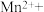

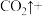
 ______
______(2)
 可以作为水溶液中
可以作为水溶液中 歧化反应的催化剂,可能的催化过程如下。将ⅱ补充完整。
歧化反应的催化剂,可能的催化过程如下。将ⅱ补充完整。ⅰ.
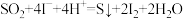
ⅱ.
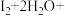 ______= ______+______
______= ______+______ ,
,(3)高铁酸钾(
 )是一种强氧化剂,可作为水处理剂和高容量电池材料。
)是一种强氧化剂,可作为水处理剂和高容量电池材料。 和KClO在强碱性条件下反应可制取
和KClO在强碱性条件下反应可制取 ,其反应的离子方程式为:
,其反应的离子方程式为:(4)往
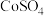 溶液中滴加
溶液中滴加 制备
制备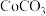 固体,写出该过程中发生反应的离子方程式
固体,写出该过程中发生反应的离子方程式(5)NaH在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为
 ),脱锈过程发生反应的化学方程式
),脱锈过程发生反应的化学方程式(6)元素镍(Ni)在溶液中
 价极不稳定,主要以
价极不稳定,主要以 (绿色)、
(绿色)、 (蓝色)、
(蓝色)、 (橙黄色)、
(橙黄色)、 (深红色)等形式存在。
(深红色)等形式存在。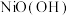 为难溶于水的黑色固体,其溶于浓盐酸并形成绿色溶液,其离子方程式为
为难溶于水的黑色固体,其溶于浓盐酸并形成绿色溶液,其离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】有机物是一类重要的化合物,不仅种类繁多,而且与我们的日常生活密切相关。
Ⅰ.下列有机物:_______ 、⑦_______ 。
(2)⑧被酸性高锰酸钾氧化的产物为_______ 。
(3)所有原子一定共面的是_______ (填序号,下同)。
(4)⑨的二氯代物有_______ 种同分异构体。
(5)水溶性最好的是_______ ,原因_______ 。
Ⅱ.烷烃主要来源是石油和天然气,是重要的化工原料和能源物资。
(6)表中烷烃的氢原子的化学环境只有一种,分析下表中各项的排布规律,按此规律排布第6项X应为_______ (选填编号)。
a.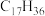 b.
b.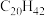 c.
c.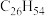 d.
d.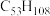
Ⅰ.下列有机物:
① ;②
;②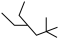 ;③
;③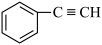 ;④
;④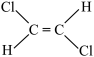 ;⑤
;⑤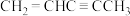 ;
;
⑥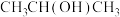 ;⑦
;⑦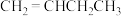 ;⑧
;⑧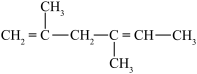 ;⑨
;⑨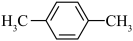 ;
;
(2)⑧被酸性高锰酸钾氧化的产物为
(3)所有原子一定共面的是
(4)⑨的二氯代物有
(5)水溶性最好的是
Ⅱ.烷烃主要来源是石油和天然气,是重要的化工原料和能源物资。
(6)表中烷烃的氢原子的化学环境只有一种,分析下表中各项的排布规律,按此规律排布第6项X应为
| 1 | 2 | 3 | 4 | 5 | 6 | … |
 |  | 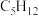 | 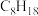 | X |
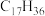 b.
b.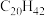 c.
c.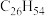 d.
d.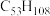
您最近一年使用:0次
【推荐2】回答下列问题:
(1)下列分子中若有手性原子,请用“*”标出其手性碳原子___________ 。
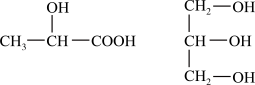
(2)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4___________ H2SO3;HClO3___________ HClO4;
(3)NaBrO、NaBrO2、NaBrO3、NaBrO4四种钠盐中,Br的杂化方式均为___________ ;
(4)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于___________ ;H2O比H2S更稳定,这是由于___________ 。
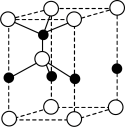
(5)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,下图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为___________ ,该功能陶瓷的化学式为___________ 。
(1)下列分子中若有手性原子,请用“*”标出其手性碳原子
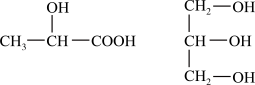
(2)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):H2SO4
(3)NaBrO、NaBrO2、NaBrO3、NaBrO4四种钠盐中,Br的杂化方式均为
(4)H2O的沸点(100℃)比H2S的沸点(-61℃)高,这是由于
(5)利用“卤化硼法”可合成含B和N两种元素的功能陶瓷,下图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下列说法正确的是________ 。
①CO2、H2S都属于含极性键的非极性分子
②S2Cl2(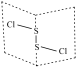 )为含有极性键和非极性键的非极性分子
)为含有极性键和非极性键的非极性分子
③SF6(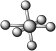 )是由极性键构成的非极性分子
)是由极性键构成的非极性分子
④SO2和NH3均易溶于水,原因之一是它们都是极性分子
⑤CCl4是非极性分子,C原子处在4个Cl原子所组成的正方形的中心
⑥卤素单质、卤素氢化物、卤素碳化物(即CX4)的熔、沸点均随着相对分子质量的增大而增大
⑦H2O比H2S稳定是因为水分子间存在氢键
⑧极性分子中可能含有非极性键
⑨HClO2、H2SeO3、H3BO3、HMnO4四种含氧酸中酸性最强的是H3BO3
⑩BF3和NH3化学键的类型和分子的极性(极性或非极性)皆相同
⑪H2O的沸点比HF的沸点高,是由于水中氢键键能大
⑫邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点高
①CO2、H2S都属于含极性键的非极性分子
②S2Cl2(
 )为含有极性键和非极性键的非极性分子
)为含有极性键和非极性键的非极性分子③SF6(
 )是由极性键构成的非极性分子
)是由极性键构成的非极性分子④SO2和NH3均易溶于水,原因之一是它们都是极性分子
⑤CCl4是非极性分子,C原子处在4个Cl原子所组成的正方形的中心
⑥卤素单质、卤素氢化物、卤素碳化物(即CX4)的熔、沸点均随着相对分子质量的增大而增大
⑦H2O比H2S稳定是因为水分子间存在氢键
⑧极性分子中可能含有非极性键
⑨HClO2、H2SeO3、H3BO3、HMnO4四种含氧酸中酸性最强的是H3BO3
⑩BF3和NH3化学键的类型和分子的极性(极性或非极性)皆相同
⑪H2O的沸点比HF的沸点高,是由于水中氢键键能大
⑫邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点高
您最近一年使用:0次



