“84消毒液”是日常生活中常用的消毒液,有效成分是NaClO。在抗击新冠肺炎中广泛应用。
(1)用“84”消毒液漂白衣物时,在空气中放置一段时间漂白效果更好,结合离子方程式解释原因_ ;(已知酸性:H2CO3>HClO> )
)
(2)“84消毒液”与适量醋酸混合使用可增强消毒能力,某消毒组成员欲用盐酸代替醋酸,是否可行__ (填“是”或“否”),原因是________ ;
(3)Cl2是最早用于饮用水消毒的物质,ClO2是一种广谱消毒剂,Cl2和ClO2消毒效率(消毒效率是指单位质量的氧化剂转移电子数,转移电子数越多,消毒效率越高)高的是___ (填化学式),工业上ClO2常用NaClO3和Na2SO3溶液混合酸化反应制得,请写出此过程的离子方程式_____ ;
(4)实验室常用烧碱溶液吸收Cl2,若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为15:2时,混合液中NaClO和NaClO3的物质的量之比为_ ;
(5)已知:3Cl2+8NH3=6NH4Cl+N2,化工厂可用浓氨水来检验Cl2是否泄漏,该反应中被氧化和未被氧化的NH3的物质的量之比为______ 。
(1)用“84”消毒液漂白衣物时,在空气中放置一段时间漂白效果更好,结合离子方程式解释原因
 )
)(2)“84消毒液”与适量醋酸混合使用可增强消毒能力,某消毒组成员欲用盐酸代替醋酸,是否可行
(3)Cl2是最早用于饮用水消毒的物质,ClO2是一种广谱消毒剂,Cl2和ClO2消毒效率(消毒效率是指单位质量的氧化剂转移电子数,转移电子数越多,消毒效率越高)高的是
(4)实验室常用烧碱溶液吸收Cl2,若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当NaCl和NaClO3的物质的量之比为15:2时,混合液中NaClO和NaClO3的物质的量之比为
(5)已知:3Cl2+8NH3=6NH4Cl+N2,化工厂可用浓氨水来检验Cl2是否泄漏,该反应中被氧化和未被氧化的NH3的物质的量之比为
更新时间:2021-01-28 23:51:25
|
相似题推荐
【推荐1】Ⅰ.有如图所示各步变化(部分产物未写出),A为单质,B为淡黄色固体,物质A~E均含有钠元素。

(1)写出下列物质的名称:B.___________ ,D.___________ 。
(2)写出A→E的化学方程式并用双线桥标出电子转移的方向和数目:___________ 。
(3)物质B常用来作为潜水艇和呼吸面具中氧气来源,该物质与CO2反应的化学方程式为___________ 。
Ⅱ.完成下列问题
(4)唐代是我国古代炼丹术的鼎盛时期,皇帝、王公贵族、士大夫均热衷于此,其中用的铅丹与硝酸反应方程式是:X(铅丹)+4HNO3=PbO2+2Pb(NO3)2+2H2O,则铅丹的化学式为___________ ,铅丹可以由一氧化铅在空气中加热至500℃制备,则制备方程式为___________ 。
(2)砒霜(As2O3)与Zn可以发生反应:____As2O3+____Zn+___H2SO4=____AsH3+____ZnSO4+____H2O
①AsH3中非金属元素As(砷)的化合价为___________ 。
②配平上述方程式。___________
③在上述反应中As2O3体现出来的性质是___________ 。(填“还原性”或“氧化性”)
④若生成0.2molAsH3,则转移的电子数目为___________ NA。

(1)写出下列物质的名称:B.
(2)写出A→E的化学方程式并用双线桥标出电子转移的方向和数目:
(3)物质B常用来作为潜水艇和呼吸面具中氧气来源,该物质与CO2反应的化学方程式为
Ⅱ.完成下列问题
(4)唐代是我国古代炼丹术的鼎盛时期,皇帝、王公贵族、士大夫均热衷于此,其中用的铅丹与硝酸反应方程式是:X(铅丹)+4HNO3=PbO2+2Pb(NO3)2+2H2O,则铅丹的化学式为
(2)砒霜(As2O3)与Zn可以发生反应:____As2O3+____Zn+___H2SO4=____AsH3+____ZnSO4+____H2O
①AsH3中非金属元素As(砷)的化合价为
②配平上述方程式。
③在上述反应中As2O3体现出来的性质是
④若生成0.2molAsH3,则转移的电子数目为
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】(1)在常温下,发生下列几种反应:
①16H++10Z-+2XO4-===2X2++5Z2+8H2O
②2A2++B2===2A3++2B- ③2B-+Z2===B2+2Z-
根据上述反应,XO4-、Z2、B2、A3+氧化性从强到弱的顺序为:___________
(2)已知KMnO4与浓盐酸发生如下反应:
2KMnO4 + 16HCl(浓) ="==" 2KCl + 2MnCl2 + 5Cl2↑+8H2O。
在上述反应中,氧化产物和还原产物物质的量之比是___________ 。用单线桥法标出此反应的电子转移方向和数目_______________ 。
(3)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:
①将这6种物质分别填入下面对应的横线上,组成一个配平的化学方程式:
________ +________ + H2SO4→ ________ +________ +________ (填化学式)
②反应中1mol氧化剂得到______ mol电子。
①16H++10Z-+2XO4-===2X2++5Z2+8H2O
②2A2++B2===2A3++2B- ③2B-+Z2===B2+2Z-
根据上述反应,XO4-、Z2、B2、A3+氧化性从强到弱的顺序为:
(2)已知KMnO4与浓盐酸发生如下反应:
2KMnO4 + 16HCl(浓) ="==" 2KCl + 2MnCl2 + 5Cl2↑+8H2O。
在上述反应中,氧化产物和还原产物物质的量之比是
(3)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:
①将这6种物质分别填入下面对应的横线上,组成一个配平的化学方程式:
②反应中1mol氧化剂得到
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氧化还原反应是一类重要的反应,请按要求完成下列题目。
(1)对反应NH3+O2——NO+H2O(未配平)作分析,并用单线桥法标出电子转移的方向和数目:_____________ 。该反应中,________ 是还原剂,________ 是还原产物,被还原的物质是________ 。
(2)在一定条件下,反应2NH3+3CuO 3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是
3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是_____ (填序号)。
A.该反应是置换反应
B.反应中NH3被氧化为N2
C.在反应中体现了金属铜的还原性
D.在反应中每生成1 mol H2O转移1 mol电子
(3)在反应H2SO3+2H2S===3H2O+3S↓中被氧化的元素与被还原的元素的质量比为________ 。
(1)对反应NH3+O2——NO+H2O(未配平)作分析,并用单线桥法标出电子转移的方向和数目:
(2)在一定条件下,反应2NH3+3CuO
 3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是
3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是A.该反应是置换反应
B.反应中NH3被氧化为N2
C.在反应中体现了金属铜的还原性
D.在反应中每生成1 mol H2O转移1 mol电子
(3)在反应H2SO3+2H2S===3H2O+3S↓中被氧化的元素与被还原的元素的质量比为
您最近一年使用:0次
【推荐1】已知氧化性强弱:Cl2>Br2>Fe3+;还原性强弱:Fe2+>Br->Cl-
(1)下列反应能够发生的是:___ (可多选);
A.Cl2+2Fe2+=2Cl-+2Fe3+ B.2Cl-+Br2=Cl2+2Br-
C.Br2+2Fe2+=2Br-+2Fe3+ D.2Fe3++2Br-=2Fe2++Br2
(2)把少量的氯气通入FeBr2溶液中时,氯气可以氧化Fe2+和Br-,请问氯气先氧化哪一种离子?___ (填写离子符号);
(3)往250mLFeBr2溶液中通入8.96LCl2(标准状况),反应完成后,溶液中1/2的Br-被氧化为溴单质,则原FeBr2溶液的物质的量浓度为多少?___
(1)下列反应能够发生的是:
A.Cl2+2Fe2+=2Cl-+2Fe3+ B.2Cl-+Br2=Cl2+2Br-
C.Br2+2Fe2+=2Br-+2Fe3+ D.2Fe3++2Br-=2Fe2++Br2
(2)把少量的氯气通入FeBr2溶液中时,氯气可以氧化Fe2+和Br-,请问氯气先氧化哪一种离子?
(3)往250mLFeBr2溶液中通入8.96LCl2(标准状况),反应完成后,溶液中1/2的Br-被氧化为溴单质,则原FeBr2溶液的物质的量浓度为多少?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
Ⅰ.有下10物质:①钠,②纯醋酸,③ ,④
,④ ,⑤NaOH,⑥漂白粉,⑦HCl,⑧
,⑤NaOH,⑥漂白粉,⑦HCl,⑧ ,⑨碳酸氢钠,⑩乙醇。
,⑨碳酸氢钠,⑩乙醇。
(1)上述物质中属于非电解质的有___________ (填序号)。
(2)⑥漂白原理的化学方程式为___________ 。
(3)⑧在水中的电离方程式为___________ 。
(4)少量①和⑧的溶液混合,反应的离子方程式为___________ 。
(5)Ⅱ.已知离子还原性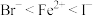 ,则氧化性
,则氧化性
___________  (填“>”“=”或“<”),有一混合溶液,其中只含有
(填“>”“=”或“<”),有一混合溶液,其中只含有 、
、 、
、 ,其中
,其中 、
、 的物质的量之比为3:4,向该溶液中通入少量氯气,一定会发生的反应的离子方程式是
的物质的量之比为3:4,向该溶液中通入少量氯气,一定会发生的反应的离子方程式是___________ 。如果要使溶液 、
、 的物质的量之比为3:1,通入氯气与溶液中剩余
的物质的量之比为3:1,通入氯气与溶液中剩余 的物质的量之比为
的物质的量之比为___________ 。
Ⅰ.有下10物质:①钠,②纯醋酸,③
 ,④
,④ ,⑤NaOH,⑥漂白粉,⑦HCl,⑧
,⑤NaOH,⑥漂白粉,⑦HCl,⑧ ,⑨碳酸氢钠,⑩乙醇。
,⑨碳酸氢钠,⑩乙醇。(1)上述物质中属于非电解质的有
(2)⑥漂白原理的化学方程式为
(3)⑧在水中的电离方程式为
(4)少量①和⑧的溶液混合,反应的离子方程式为
(5)Ⅱ.已知离子还原性
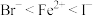 ,则氧化性
,则氧化性
 (填“>”“=”或“<”),有一混合溶液,其中只含有
(填“>”“=”或“<”),有一混合溶液,其中只含有 、
、 、
、 ,其中
,其中 、
、 的物质的量之比为3:4,向该溶液中通入少量氯气,一定会发生的反应的离子方程式是
的物质的量之比为3:4,向该溶液中通入少量氯气,一定会发生的反应的离子方程式是 、
、 的物质的量之比为3:1,通入氯气与溶液中剩余
的物质的量之比为3:1,通入氯气与溶液中剩余 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
【推荐3】已知反应:
①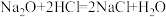
②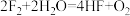
③
④
⑤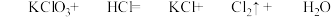
(1)上述反应中,属于置换反应的是_______ (填序号,下同);同一元素之间发生氧化还原的是_______ 。
(2)反应②中氧化剂是_______ (填化学式,下同);反应③中氧化产物是_______ 。
(3)在反应④中,每生成1个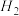 分子时,转移的电子数为
分子时,转移的电子数为_______ 。
(4)配平反应⑤并用双线桥法标出反应⑤中电子转移的方向和数目_______ 。
(5)反应⑤中氧化剂与还原剂的质量之比为_______ (填最简整数比)。
(6)已知有下列两个反应:①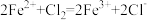 ;②
;② ,
, 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_______ 。
(7)下列物质中能使酸性 溶液褪色(转化为
溶液褪色(转化为 而褪色)的是
而褪色)的是_______ (填字母)。
a.臭碱(Na2S) b.小苏打(NaHCO3) c.水玻璃( 溶液)
溶液)
①
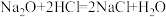
②
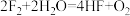
③

④

⑤
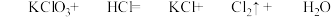
(1)上述反应中,属于置换反应的是
(2)反应②中氧化剂是
(3)在反应④中,每生成1个
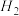 分子时,转移的电子数为
分子时,转移的电子数为(4)配平反应⑤并用双线桥法标出反应⑤中电子转移的方向和数目
(5)反应⑤中氧化剂与还原剂的质量之比为
(6)已知有下列两个反应:①
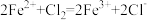 ;②
;② ,
, 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(7)下列物质中能使酸性
 溶液褪色(转化为
溶液褪色(转化为 而褪色)的是
而褪色)的是a.臭碱(Na2S) b.小苏打(NaHCO3) c.水玻璃(
 溶液)
溶液)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)写出漂白粉有效成分的化学式___________ ;
(2)写出铝与氢氧化钠反应的化学方程式___________ ;
(3)比较碳元素与硅元素的非金属性强弱:C___________ Si (填“>”“<”或“=”),用有关的离子反应方程式证明以上结论___________ 。
(2)写出铝与氢氧化钠反应的化学方程式
(3)比较碳元素与硅元素的非金属性强弱:C
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求回答下列问题:
(1)漂粉精主要成分的化学式_____ ,乙醛的结构简式是_____ 。
(2)在加热条件下,铜与浓硫酸反应的化学方程式:_____ 。
(3)NO不能用空气法收集,请用化学方程式解释其原因:_____ 。
(1)漂粉精主要成分的化学式
(2)在加热条件下,铜与浓硫酸反应的化学方程式:
(3)NO不能用空气法收集,请用化学方程式解释其原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学是实用性很强的学科。请根据题意填空。
(1) 胶体具有良好的净水效果,其分散质粒子直径大小范围为
胶体具有良好的净水效果,其分散质粒子直径大小范围为_______ ,其净水原理是胶体粒子具有_______ 性。
(2)漂粉精可作漂白棉、麻、纸张的漂白剂,也可用作游泳池等场所的消毒剂,其有效成分是_______ (填化学式)。
(3)现有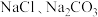 和
和 三种无色溶液,选用一种试剂把它们鉴别出来,请写出该试剂与
三种无色溶液,选用一种试剂把它们鉴别出来,请写出该试剂与 反应的离子方程式:
反应的离子方程式:_______ 。
(4)由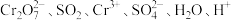 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生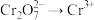 的反应。该反应中,被氧化的元素是
的反应。该反应中,被氧化的元素是_______ (填元素符号),写出该反应的离子方程式:_______ 。
(5) 的摩尔质量为
的摩尔质量为_______  ,将溶质质量分数为
,将溶质质量分数为 的
的 溶液蒸发掉
溶液蒸发掉 水后,得到
水后,得到 溶质质量分数为
溶质质量分数为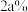 的
的 不饱和溶液,所得溶液的物质的量浓度为
不饱和溶液,所得溶液的物质的量浓度为_______ (用含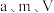 的代数式表示)
的代数式表示) 。
。
(1)
 胶体具有良好的净水效果,其分散质粒子直径大小范围为
胶体具有良好的净水效果,其分散质粒子直径大小范围为(2)漂粉精可作漂白棉、麻、纸张的漂白剂,也可用作游泳池等场所的消毒剂,其有效成分是
(3)现有
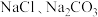 和
和 三种无色溶液,选用一种试剂把它们鉴别出来,请写出该试剂与
三种无色溶液,选用一种试剂把它们鉴别出来,请写出该试剂与 反应的离子方程式:
反应的离子方程式:(4)由
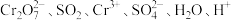 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生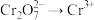 的反应。该反应中,被氧化的元素是
的反应。该反应中,被氧化的元素是(5)
 的摩尔质量为
的摩尔质量为 ,将溶质质量分数为
,将溶质质量分数为 的
的 溶液蒸发掉
溶液蒸发掉 水后,得到
水后,得到 溶质质量分数为
溶质质量分数为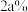 的
的 不饱和溶液,所得溶液的物质的量浓度为
不饱和溶液,所得溶液的物质的量浓度为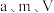 的代数式表示)
的代数式表示) 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
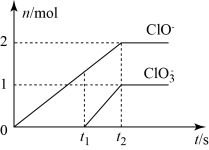
【推荐1】Ⅰ.在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应)。生成物中含有Cl-、ClO-、ClO 三种含氯元素的离子,其中ClO-、ClO
三种含氯元素的离子,其中ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
(1)t1时刻之前发生的反应是:___________
(2)t2时,Ca(OH)2与Cl2发生反应的总化学方程式为10Ca(OH)2+10Cl2=2Ca(ClO)2+Ca(ClO3)2+7CaCl2+10H2O,则该石灰乳中含有Ca(OH)2的物质的量是___________ mol。
(3)据分析,生成Ca(ClO3)2的反应是由温度升高引起的,通入Cl2的速度不同,ClO-和ClO 的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
___________ 2(填“>”、“<”或“=”);氯酸钙(Ca(ClO3)2)为有毒化学品,其粉尘对呼吸道、眼及皮肤有刺激性,吸入氯酸钙粉尘,会因积累在体内而引起中毒。为了防止使用漂白粉时出现意外,制备漂白粉时可以采取的措施___________ (写一条即可)。
(4)请配平化学方程式:KClO3+HCl--KCl+Cl2↑+H2O___________ 。若反应过程中转移2mol e-,则生成标准状况下Cl2的体积为___________ L。
Ⅱ.有下列三个在溶液中发生的氧化还原反应:
①3FeCl3+2KI=2FeCl2+2KCl+I2;
②2FeCl2+Cl2=2FeCl3;
③K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑
请根据上述反应分析推断后回答下列问题:
(5)FeCl3、I2、Cl2、K2Cr2O7的氧化性由强到弱依次是___________ 。
(6)在酸性溶液中存在大量的I-,则Cr2O 、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是
、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是___________ 。
 三种含氯元素的离子,其中ClO-、ClO
三种含氯元素的离子,其中ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
(1)t1时刻之前发生的反应是:
(2)t2时,Ca(OH)2与Cl2发生反应的总化学方程式为10Ca(OH)2+10Cl2=2Ca(ClO)2+Ca(ClO3)2+7CaCl2+10H2O,则该石灰乳中含有Ca(OH)2的物质的量是
(3)据分析,生成Ca(ClO3)2的反应是由温度升高引起的,通入Cl2的速度不同,ClO-和ClO
 的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
的比例也不同。若在原石灰乳中通入氯气的速度加快,则反应后
(4)请配平化学方程式:KClO3+HCl--KCl+Cl2↑+H2O
Ⅱ.有下列三个在溶液中发生的氧化还原反应:
①3FeCl3+2KI=2FeCl2+2KCl+I2;
②2FeCl2+Cl2=2FeCl3;
③K2Cr2O7+14HCl=2KCl+2CrCl3+7H2O+3Cl2↑
请根据上述反应分析推断后回答下列问题:
(5)FeCl3、I2、Cl2、K2Cr2O7的氧化性由强到弱依次是
(6)在酸性溶液中存在大量的I-,则Cr2O
 、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是
、Fe3+、Fe2+、Cl-中能与I-大量共存的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据题目信息,按要求完成下列填空:
(1)过氧化钠粉末与水反应的化学方程式:_____ 。
(2)实验室制取氨气(两种固体加热)的化学方程式:_____ 。
(3)二氧化硫通入溴水,可使溴水褪色,写出反应的化学方程式:_____ 。
(4)铜与浓硫酸加热条件下反应的化学方程式:_____ 。
(5)实验室制取氯气,多余的氯气可用氢氧化钠溶液吸收,写出反应的离子方程式:_____ 。
(6)三氟化氮(NF3)是一种无色无味的气体,27.0mLNF3和水充分反应,生成18.0mLNO(同温、同压下),写出反应的化学方程式:_____ 。
(1)过氧化钠粉末与水反应的化学方程式:
(2)实验室制取氨气(两种固体加热)的化学方程式:
(3)二氧化硫通入溴水,可使溴水褪色,写出反应的化学方程式:
(4)铜与浓硫酸加热条件下反应的化学方程式:
(5)实验室制取氯气,多余的氯气可用氢氧化钠溶液吸收,写出反应的离子方程式:
(6)三氟化氮(NF3)是一种无色无味的气体,27.0mLNF3和水充分反应,生成18.0mLNO(同温、同压下),写出反应的化学方程式:
您最近一年使用:0次



