氯气是一种重要的化工原料,能与有机物和无机物发生反应生成多种氯化物。现用如图装置制取氯气并进行一系列的实验探究。回答下列问题:

I.装置1用来制备纯净、干燥的氯气。
①装置A中圆底烧瓶内发生反应的离子方程式是___ ,反应中被氧化的HCl与消耗的HCl的分子数之比为____ 。
②装置B内试剂为____ ,装置C的作用是____ 。
II.若将装置1与装置2连接制备少量氯化铁固体(氯化铁易吸水,在300℃时升华),则:
①D中发生反应的化学方程式为_____ 。
②D、E间导管短且粗的原因是____ 。
③若在D装置的硬质玻璃管内装入硅藻土和碳粉,则发生如下反应:SiO2+2C+2Cl2 SiCl4+2CO,F装置之后还应添加一个装置用来
SiCl4+2CO,F装置之后还应添加一个装置用来____ 。
III.将装置1与装置3连接起来探究氯气是否具有漂白性。
①将氯气依次通过盛有干燥红色布条的广口瓶和盛有湿润红色布条的广口瓶,可观察到的现象是__ 。
②为防止氯气污染空气,根据氯水显酸性的性质,可用氢氧化钠溶液吸收多余的氯气,原理是___ 。(用离子方程式表示)。根据这一原理,工业上常用廉价的石灰乳吸收氯气制得漂白粉,漂白粉的有效成分是___ (填化学式),长期露置于空气中的失效漂白粉,加稀盐酸后产生的气体是__ (填字母代号)。
A.O2 B. H2 C.CO2 D.HClO

I.装置1用来制备纯净、干燥的氯气。
①装置A中圆底烧瓶内发生反应的离子方程式是
②装置B内试剂为
II.若将装置1与装置2连接制备少量氯化铁固体(氯化铁易吸水,在300℃时升华),则:
①D中发生反应的化学方程式为
②D、E间导管短且粗的原因是
③若在D装置的硬质玻璃管内装入硅藻土和碳粉,则发生如下反应:SiO2+2C+2Cl2
 SiCl4+2CO,F装置之后还应添加一个装置用来
SiCl4+2CO,F装置之后还应添加一个装置用来III.将装置1与装置3连接起来探究氯气是否具有漂白性。
①将氯气依次通过盛有干燥红色布条的广口瓶和盛有湿润红色布条的广口瓶,可观察到的现象是
②为防止氯气污染空气,根据氯水显酸性的性质,可用氢氧化钠溶液吸收多余的氯气,原理是
A.O2 B. H2 C.CO2 D.HClO
更新时间:2021-02-24 20:58:29
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验小组利用如下图所示的装置制备氯气及探究氯气的性质。
资料:单质碘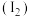 遇淀粉溶液变蓝,利用此现象可检验溶液中的
遇淀粉溶液变蓝,利用此现象可检验溶液中的 。
。
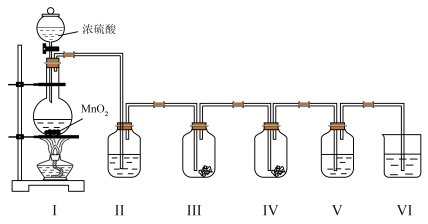
(1)Ⅰ中制备氯气时,发生反应的化学方程式是_______
(2)Ⅱ的目的是除去氯气中的水蒸气,则瓶中盛放的试剂是_______ 。
(3)利用Ⅲ、Ⅳ装置探究氯气与水反应的产物。
①实验前,向Ⅲ、Ⅳ中均放入干燥蓝色石蕊纸花,并向_______ 中滴少量水将纸花润湿。
②实验时,根据Ⅲ中的纸花不变色及_______ 现象,甲同学得出初步结论:氯气与水反应生成具有酸性及漂白性的物质。
③同学们分析后,认为用该实验装置不能得出“氯气与水反应有酸性物质生成”的结论,理由是_______ 。
(4)Ⅴ中盛有 淀粉溶液,随
淀粉溶液,随 通入,可获得
通入,可获得 具有氧化性的实验证据是
具有氧化性的实验证据是_______ 。
(5)Ⅵ中盛放的试剂是 溶液,其作用是
溶液,其作用是_______ ,发生反应的离子方程式是_______ 。
(6)利用如下装置也可以制取氯气,并利用氯气的氧化性制取 。
。
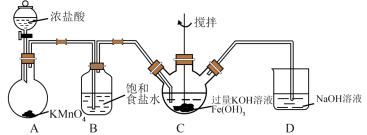
①装置A中, 被还原为
被还原为 ,写出反应的离子方程式:
,写出反应的离子方程式:_______ 。
②装置C中发生如下反应,将方程式配平:_______ 。
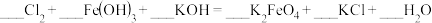
资料:单质碘
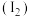 遇淀粉溶液变蓝,利用此现象可检验溶液中的
遇淀粉溶液变蓝,利用此现象可检验溶液中的 。
。
(1)Ⅰ中制备氯气时,发生反应的化学方程式是
(2)Ⅱ的目的是除去氯气中的水蒸气,则瓶中盛放的试剂是
(3)利用Ⅲ、Ⅳ装置探究氯气与水反应的产物。
①实验前,向Ⅲ、Ⅳ中均放入干燥蓝色石蕊纸花,并向
②实验时,根据Ⅲ中的纸花不变色及
③同学们分析后,认为用该实验装置不能得出“氯气与水反应有酸性物质生成”的结论,理由是
(4)Ⅴ中盛有
 淀粉溶液,随
淀粉溶液,随 通入,可获得
通入,可获得 具有氧化性的实验证据是
具有氧化性的实验证据是(5)Ⅵ中盛放的试剂是
 溶液,其作用是
溶液,其作用是(6)利用如下装置也可以制取氯气,并利用氯气的氧化性制取
 。
。
①装置A中,
 被还原为
被还原为 ,写出反应的离子方程式:
,写出反应的离子方程式:②装置C中发生如下反应,将方程式配平:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
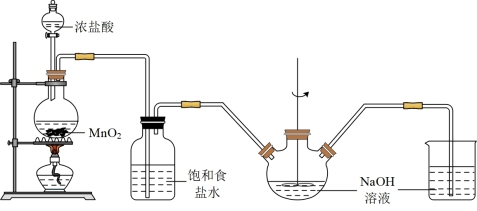
【推荐2】下表为“84”消毒液说明书,实验室制备消毒液的装置如下所示。
请回答下列问题。
(1)制得的Cl2通过盛有饱和食盐水的装置,目的是_______ 。
(2)水溶液中Cl2和SO2不能同时作为漂白剂使用,写出在水溶液中Cl2和SO2反应的离子方程式_______ 。
(3)实验室为制取消毒液,需配制500mL0.2mol/LNaOH溶液。
①配制过程中需要的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、_______ 。
②下列主要操作步骤的正确顺序是_______ (填序号)。
a称取一定质量的NaOH,放入烧杯中,用适量蒸馏水溶解;
b加水至液面离刻度线1~2cm,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相切;
c待冷却至室温后,将溶液转移到容量瓶中;
d盖好瓶塞,反复上下颠倒,摇匀;
e用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
③如果步骤b操作时俯视刻度线,会使NaOH溶液浓度_______ (填“偏高、偏低”或“不变”)。
(4)三颈烧瓶中生成各物质的物质的量和溶液的温度随时间的变化如下图所示。t1分钟后所发生主要反应的化学方程式为_______ 。
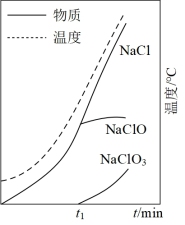
(5)家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是_______ 。

说明书 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00g/L~60.00g/L | |
| 注意事项 | 不可与其他洗涤剂或消毒液混合使用 |
(1)制得的Cl2通过盛有饱和食盐水的装置,目的是
(2)水溶液中Cl2和SO2不能同时作为漂白剂使用,写出在水溶液中Cl2和SO2反应的离子方程式
(3)实验室为制取消毒液,需配制500mL0.2mol/LNaOH溶液。
①配制过程中需要的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒、
②下列主要操作步骤的正确顺序是
a称取一定质量的NaOH,放入烧杯中,用适量蒸馏水溶解;
b加水至液面离刻度线1~2cm,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相切;
c待冷却至室温后,将溶液转移到容量瓶中;
d盖好瓶塞,反复上下颠倒,摇匀;
e用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
③如果步骤b操作时俯视刻度线,会使NaOH溶液浓度
(4)三颈烧瓶中生成各物质的物质的量和溶液的温度随时间的变化如下图所示。t1分钟后所发生主要反应的化学方程式为

(5)家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室制取气体装置一般由发生装置、净化装置、收集装置以及尾气吸收装置组成。以Cl2的实验室制法为例(见下图):
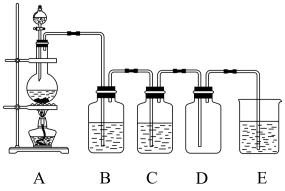
(1)反应原理: A中反应的离子方程式:___________ 。
(2)净化方法:B中盛放___________ 除去___________ ,C中盛放___________ 除去___________ 。
(3)收集方法:___________ 。
(4)验满方法:___________ 。
(5)尾气吸收:E中盛放___________ 。
(6)甲同学在实验室进行氯气性质的研究。按如图进行试验:

请描述现象:___________ ,结合化学方程式解释原因___________ 。
(7)工业上将氧气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为___________ ;漂白粉在空气中很容易变质,请写出漂白粉在空气中变质的反应方程式___________ 。

(1)反应原理: A中反应的离子方程式:
(2)净化方法:B中盛放
(3)收集方法:
(4)验满方法:
(5)尾气吸收:E中盛放
(6)甲同学在实验室进行氯气性质的研究。按如图进行试验:

请描述现象:
(7)工业上将氧气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某研究性学习小组制备高铁酸钾(K2FeO4)并探究其性质。查阅文献,得到以下资料: K2FeO4为紫色固体,微溶于 KOH 溶液;具有强氧化性,在酸性或中性溶液中快速产生 O2,在碱性溶液中较稳定。
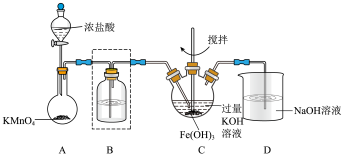
Ⅰ.制备 K2FeO4(夹持装置略)。
(1)A 为氯气的实验室发生装置。A 中反应方程式是______ (锰被还原为 Mn2+)。若反应中有 0.5molCl2产生,则电子转移的数目为______ 。工业制氯气的反应方程式为______ 。
(2)装置 B 中盛放的试剂是______ ,简述该装置在制备高铁酸钾中的作用______ 。
(3)C 中得到紫色固体和溶液。C 中 Cl2发生的反应有:3Cl2+2Fe(OH)3+10KOH→2K2FeO4+6KCl+8H2O,根据该反应方程式得出:碱性条件下,氧化性 Cl2______ FeO42-(填“>”或“<”)。另外C中还可能发生其他反应,请用离子方程式表示______ 。
Ⅱ.探究 K2FeO4 的性质
(4)甲同学取少量 K2FeO4 加入浑浊的泥浆水中,发现产生气体,搅拌,浑浊的泥浆水很快澄清。请简述 K2FeO4的净水原理。______ 。

Ⅰ.制备 K2FeO4(夹持装置略)。
(1)A 为氯气的实验室发生装置。A 中反应方程式是
(2)装置 B 中盛放的试剂是
(3)C 中得到紫色固体和溶液。C 中 Cl2发生的反应有:3Cl2+2Fe(OH)3+10KOH→2K2FeO4+6KCl+8H2O,根据该反应方程式得出:碱性条件下,氧化性 Cl2
Ⅱ.探究 K2FeO4 的性质
(4)甲同学取少量 K2FeO4 加入浑浊的泥浆水中,发现产生气体,搅拌,浑浊的泥浆水很快澄清。请简述 K2FeO4的净水原理。
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】在实验室中用二氧化锰与浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如图:
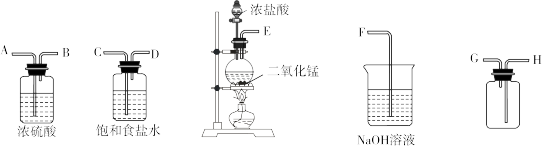
(1)上述仪器的正确连接顺序为(填各接口处的字母):___________ 。
(2)气体发生装置中进行的化学方程式为___________ 。
(3)装置中,饱和食盐水的作用是___________ ;NaOH溶液的作用是___________ 。
(4)84消毒液能有效杀灭新冠病毒,常用于环境场所消毒。可用 与氢氧化钠溶液反应制取,该反应的离子方程式为
与氢氧化钠溶液反应制取,该反应的离子方程式为___________ 。
(5)曾有报道,在清洗卫生间时,因混合使用洁厕灵(主要成分是稀盐酸)与84清毒液(主要成分是NaClO)而发生氯气中毒事件。请用离子方程式解释原因___________ 。

(1)上述仪器的正确连接顺序为(填各接口处的字母):
(2)气体发生装置中进行的化学方程式为
(3)装置中,饱和食盐水的作用是
(4)84消毒液能有效杀灭新冠病毒,常用于环境场所消毒。可用
 与氢氧化钠溶液反应制取,该反应的离子方程式为
与氢氧化钠溶液反应制取,该反应的离子方程式为(5)曾有报道,在清洗卫生间时,因混合使用洁厕灵(主要成分是稀盐酸)与84清毒液(主要成分是NaClO)而发生氯气中毒事件。请用离子方程式解释原因
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某学校兴趣小组采用如图装置制取 及无水
及无水 固体(容易潮解,在100℃左右升华)。
固体(容易潮解,在100℃左右升华)。
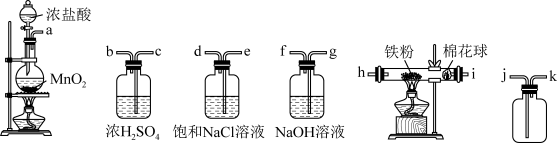
回答下列问题:
(1)上述装置从左至右的连接顺序为___________ →cbgf(填字母,必要的装置可重复使用)。
(2)饱和NaCl溶液的作用为___________ ;棉花球的作用为___________ ; 与Fe粉反应的化学方程式为
与Fe粉反应的化学方程式为___________ 。
(3)NaOH溶液的作用是___________ 。
(4)将干燥的 依次通过干燥的有色布条、湿润的有色布条,可观察到的现象是
依次通过干燥的有色布条、湿润的有色布条,可观察到的现象是___________ ,得出的结论是___________ 。
(5)实验结束后,从盛有NaOH溶液的广口瓶中取少量溶液于烧杯中,加入足量浓盐酸后,会产生一种黄绿色气体,写出生成该气体的离子方程式___________ 。
 及无水
及无水 固体(容易潮解,在100℃左右升华)。
固体(容易潮解,在100℃左右升华)。
回答下列问题:
(1)上述装置从左至右的连接顺序为
(2)饱和NaCl溶液的作用为
 与Fe粉反应的化学方程式为
与Fe粉反应的化学方程式为(3)NaOH溶液的作用是
(4)将干燥的
 依次通过干燥的有色布条、湿润的有色布条,可观察到的现象是
依次通过干燥的有色布条、湿润的有色布条,可观察到的现象是(5)实验结束后,从盛有NaOH溶液的广口瓶中取少量溶液于烧杯中,加入足量浓盐酸后,会产生一种黄绿色气体,写出生成该气体的离子方程式
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
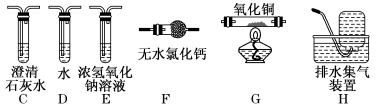
【推荐1】草酸(H2C2O4)广泛存在于自然界植物中草酸的钠盐易溶于水,而其钙盐难溶于水。草酸晶体(H2C2O4·2H2O)易溶于水,(熔点为101℃,受热脱水、升华,170℃以上分解。回答下列问题:
(1)已知25℃时,H2C2O4的 Ka1=5×10-2,Ka2=2×10-4。
①写出H2C2O4的电离方程式___________ 。
②计算反应 + H2O
+ H2O H2C2O4+OH-的水解常数Kh=
H2C2O4+OH-的水解常数Kh=___________ ,据此判断NaHC2O4溶液中c(H2C2O4)___________ c( )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。
(2)甲组同学按照下图所示的装置,通过实验检验草酸晶体的分解产物。

当观察到装置C中澄清石灰水变浑浊时,可知草酸晶体分解的产物中含有___________ (填化学式)。装置B的主要作用是___________ 。
(3)乙组同学认为草酸晶体分解的产物中还含有CO。为进行验证,选用甲组实验中的装置A、B和下图所示装置进行实验。
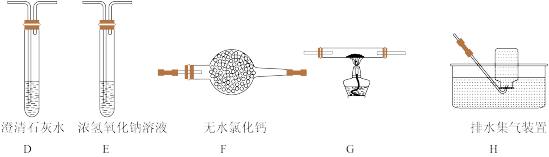
①乙组同学的实验装置中,依次连接的合理顺序为A、B、___________ (填字母序号),装置G反应管中盛有的物质是___________ (填化学式)。
②能证明草酸晶体分解产物中含有CO的现象是___________ 。
(1)已知25℃时,H2C2O4的 Ka1=5×10-2,Ka2=2×10-4。
①写出H2C2O4的电离方程式
②计算反应
 + H2O
+ H2O H2C2O4+OH-的水解常数Kh=
H2C2O4+OH-的水解常数Kh= )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。(2)甲组同学按照下图所示的装置,通过实验检验草酸晶体的分解产物。

当观察到装置C中澄清石灰水变浑浊时,可知草酸晶体分解的产物中含有
(3)乙组同学认为草酸晶体分解的产物中还含有CO。为进行验证,选用甲组实验中的装置A、B和下图所示装置进行实验。

①乙组同学的实验装置中,依次连接的合理顺序为A、B、
②能证明草酸晶体分解产物中含有CO的现象是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】探究有关物质氧化性的强弱。已知:①铋(Bi)位于元素周期表中第VA族,铋元素+3价较稳定,NaBiO3溶液为无色,Bi3+无色;②Mn2+无色,MnO 呈紫红色;③Pb元素常见的价态是+2价和+4价,+2价较稳定,PbSO4是一种白色沉淀。④H2O2+SO2=H2SO4。+3价较稳定,NaBiO3溶液为无色。取一定量的无色Mn(NO3)2溶液依次进行实验,现象记录如下:①滴加适量的NaBiO3溶液,溶液变为紫红色;②继续滴加适量H2O2,紫红色褪去,并有气泡产生;③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色;④最后通入足量的SO2气体。请回答下列问题:
呈紫红色;③Pb元素常见的价态是+2价和+4价,+2价较稳定,PbSO4是一种白色沉淀。④H2O2+SO2=H2SO4。+3价较稳定,NaBiO3溶液为无色。取一定量的无色Mn(NO3)2溶液依次进行实验,现象记录如下:①滴加适量的NaBiO3溶液,溶液变为紫红色;②继续滴加适量H2O2,紫红色褪去,并有气泡产生;③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色;④最后通入足量的SO2气体。请回答下列问题:
(1)推测实验④中现象为____ 。
(2)分析上述现象,KMnO4、H2O2、PbO2的氧化性由强到弱的顺序是____ 。
(3)写出②的离子方程式____ 。
(4)写出④的离子方程式____ 。
 呈紫红色;③Pb元素常见的价态是+2价和+4价,+2价较稳定,PbSO4是一种白色沉淀。④H2O2+SO2=H2SO4。+3价较稳定,NaBiO3溶液为无色。取一定量的无色Mn(NO3)2溶液依次进行实验,现象记录如下:①滴加适量的NaBiO3溶液,溶液变为紫红色;②继续滴加适量H2O2,紫红色褪去,并有气泡产生;③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色;④最后通入足量的SO2气体。请回答下列问题:
呈紫红色;③Pb元素常见的价态是+2价和+4价,+2价较稳定,PbSO4是一种白色沉淀。④H2O2+SO2=H2SO4。+3价较稳定,NaBiO3溶液为无色。取一定量的无色Mn(NO3)2溶液依次进行实验,现象记录如下:①滴加适量的NaBiO3溶液,溶液变为紫红色;②继续滴加适量H2O2,紫红色褪去,并有气泡产生;③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色;④最后通入足量的SO2气体。请回答下列问题:(1)推测实验④中现象为
(2)分析上述现象,KMnO4、H2O2、PbO2的氧化性由强到弱的顺序是
(3)写出②的离子方程式
(4)写出④的离子方程式
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】亚硝酰氯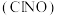 是有机物合成中的重要试剂,其沸点为
是有机物合成中的重要试剂,其沸点为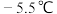 ,易水解。已知:
,易水解。已知: 微溶于水,能溶于硝酸,
微溶于水,能溶于硝酸, ,某学习小组在实验室用
,某学习小组在实验室用 和NO制备ClNO并测定其纯度,相关实验装置如图所示。
和NO制备ClNO并测定其纯度,相关实验装置如图所示。
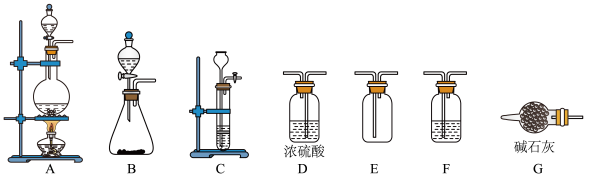
⑴制备 的发生装置可以选用
的发生装置可以选用_______ (填字母代号)装置,发生反应的离子方程式为___________ 。
⑵欲收集一瓶干燥的氯气,选择合适的装置,其连接顺序为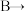
________________ (填字母代号)。
⑶实验室可用图示装置制备亚硝酰氯,检验装置气密性并装入药品,打开 ,然后再打开
,然后再打开 ,通入一段时间气体,其目的是
,通入一段时间气体,其目的是____________ ,然后进行其他操作,当Z中有一定量液体生成时,停止实验。
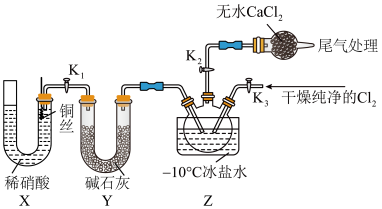
⑷已知:ClNO水解生成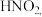 写出化学反应方程式
写出化学反应方程式__________________ 。
①欲设计实验证明 是弱酸,需选择如下
是弱酸,需选择如下_____________ 试剂开展实验 填选项
填选项 。
。
A.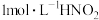 溶液 B.
溶液 B.  溶液 C. 红色石蕊试纸 D. 蓝色石蕊试纸
溶液 C. 红色石蕊试纸 D. 蓝色石蕊试纸
 已知下列物质在常温下的
已知下列物质在常温下的 如图:
如图:
通过以下实验测定ClNO样品的纯度。取Z中所得液体 溶于水,配制成
溶于水,配制成 溶液;取出
溶液;取出 样品溶于锥形瓶中,用
样品溶于锥形瓶中,用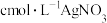 标准溶液滴定至终点,应加入的指示剂是
标准溶液滴定至终点,应加入的指示剂是_______________ 。
A. B.
B.  C.
C.  D.
D. 
消耗标准溶液的体积为 ,滴定终点的现象是
,滴定终点的现象是 ________________ ,亚硝酰氯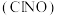 的质量分数为
的质量分数为________ 。
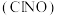 是有机物合成中的重要试剂,其沸点为
是有机物合成中的重要试剂,其沸点为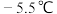 ,易水解。已知:
,易水解。已知: 微溶于水,能溶于硝酸,
微溶于水,能溶于硝酸, ,某学习小组在实验室用
,某学习小组在实验室用 和NO制备ClNO并测定其纯度,相关实验装置如图所示。
和NO制备ClNO并测定其纯度,相关实验装置如图所示。 
⑴制备
 的发生装置可以选用
的发生装置可以选用⑵欲收集一瓶干燥的氯气,选择合适的装置,其连接顺序为
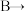
⑶实验室可用图示装置制备亚硝酰氯,检验装置气密性并装入药品,打开
 ,然后再打开
,然后再打开 ,通入一段时间气体,其目的是
,通入一段时间气体,其目的是
⑷已知:ClNO水解生成
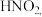 写出化学反应方程式
写出化学反应方程式①欲设计实验证明
 是弱酸,需选择如下
是弱酸,需选择如下 填选项
填选项 。
。 A.
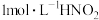 溶液 B.
溶液 B.  溶液 C. 红色石蕊试纸 D. 蓝色石蕊试纸
溶液 C. 红色石蕊试纸 D. 蓝色石蕊试纸  已知下列物质在常温下的
已知下列物质在常温下的 如图:
如图:| 化学式 | AgCl | AgBr | Ag2S | Ag2CrO4 |
颜色 | 白色 | 浅黄色 | 黑色 | 砖红色 |
Ksp | 1.56×10-10 | 5.4×10-13 | 2.0×10-48 | 1×10-12 |
 溶于水,配制成
溶于水,配制成 溶液;取出
溶液;取出 样品溶于锥形瓶中,用
样品溶于锥形瓶中,用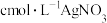 标准溶液滴定至终点,应加入的指示剂是
标准溶液滴定至终点,应加入的指示剂是A.
 B.
B.  C.
C.  D.
D. 
消耗标准溶液的体积为
 ,滴定终点的现象是
,滴定终点的现象是 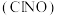 的质量分数为
的质量分数为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】“索尔维制碱法”工艺流程如图所示,请回答下列问题:
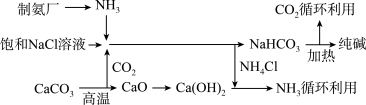
(1)向饱和氯化钠溶液中先通入___ ,效果更好。反应制得NaHCO3沉淀和NH4Cl溶液的化学方程式为____ 。
(2)索尔维制碱法除了得到纯碱外,还会产生一种废渣___ 。侯氏制碱法在此工艺上改进,不再使用碳酸钙制备CO2,而是在制备NH3的过程中制得CO2,则侯氏制碱法在得到纯碱的同时还制得了___ ,此物质在农业上的用途是___ 。

(1)向饱和氯化钠溶液中先通入
(2)索尔维制碱法除了得到纯碱外,还会产生一种废渣
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】硫代硫酸钠(Na2S2O3)可用于治疗砷、汞、铋、铅等重金属中毒,水溶液显弱碱性。由某文献知,35℃时,SO2、Na2S和Na2CO3溶液反应可生成Na2S2O3与一种气体产物。某兴趣小组欲利用下图装置(夹持装置和搅拌装置略去)制备Na2S2O3。
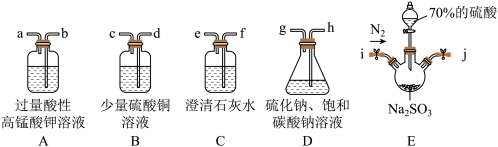
回答下列问题:
(1)盛放70%硫酸的仪器名称是___________ ,装置D采用的加热方式为___________ 。
(2)某同学猜测气体产物的成分可能为H2S或CO2.该同学利用上图装置设计实验制备硫代硫酸钠,并检验气体产物。正确的仪器连接顺序为(i)j→___________ (填小写字母)。
(3)按上述顺序连接仪器并进行实验过程中观察到A中紫色变浅,B中无明显现象,C中溶液变浑浊,则制备硫代硫酸钠的离子方程式为___________ 。
(4)反应过程中装置D中若出现大量淡黄色固体,可能的原因是___________ ;实验结束后,拆卸装置前,应打开i处弹簧夹,通入N2,此操作的目的为___________ 。
(5)从装置D中制得粗品。称取0.8g粗产品,配成溶液25.00mL置于锥形瓶中,再用0.0500mol·L-1的碘标准溶液进行滴定(2 +I2=
+I2= +2I-),消耗碘标准溶液的体积为30.00mL,则所得产品的纯度为
+2I-),消耗碘标准溶液的体积为30.00mL,则所得产品的纯度为___________ 。

回答下列问题:
(1)盛放70%硫酸的仪器名称是
(2)某同学猜测气体产物的成分可能为H2S或CO2.该同学利用上图装置设计实验制备硫代硫酸钠,并检验气体产物。正确的仪器连接顺序为(i)j→
(3)按上述顺序连接仪器并进行实验过程中观察到A中紫色变浅,B中无明显现象,C中溶液变浑浊,则制备硫代硫酸钠的离子方程式为
(4)反应过程中装置D中若出现大量淡黄色固体,可能的原因是
(5)从装置D中制得粗品。称取0.8g粗产品,配成溶液25.00mL置于锥形瓶中,再用0.0500mol·L-1的碘标准溶液进行滴定(2
 +I2=
+I2= +2I-),消耗碘标准溶液的体积为30.00mL,则所得产品的纯度为
+2I-),消耗碘标准溶液的体积为30.00mL,则所得产品的纯度为
您最近半年使用:0次