(1)酸雨形成的原理之一可表示为:
含硫化合物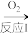 A
A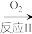 B
B 硫酸
硫酸
请回答下列问题。
①A的化学式为_______ 。
②三个反应中,不属于氧化还原反应的是_______ (填序号)。
③SO2中硫元素显+4价,它可以降低到0价,利用这一性质可在工厂的烟道气中通入合适的_______ (填“氧化剂”或“还原剂”)除去SO2,达到减少污染的目的。
(2)将4 molA气体和2molB气体在2L的密闭容器中混合并在一定条件下发生如下反应:2A(g)+B( g)⇌2C(g)。若经2 min时测得C的浓度为0.6 mol.L-I,填写下列空白:
①用物质A表示反应的平均速率为_______ 。
②其他条件不变时,再通入4 molA气体,该反应的速率将_______ (填“增大”或“减小”)。
含硫化合物
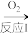 A
A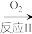 B
B 硫酸
硫酸请回答下列问题。
①A的化学式为
②三个反应中,不属于氧化还原反应的是
③SO2中硫元素显+4价,它可以降低到0价,利用这一性质可在工厂的烟道气中通入合适的
(2)将4 molA气体和2molB气体在2L的密闭容器中混合并在一定条件下发生如下反应:2A(g)+B( g)⇌2C(g)。若经2 min时测得C的浓度为0.6 mol.L-I,填写下列空白:
①用物质A表示反应的平均速率为
②其他条件不变时,再通入4 molA气体,该反应的速率将
更新时间:2021-03-24 07:51:10
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】某同学通过实验“证明鸡蛋壳的主要成分是碳酸钙”,装置示意图如图。
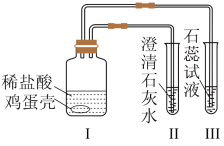
(1)按要求填写碳酸钙的类别属性(如按正离子分类,碳酸钙属于钙盐):按负离子分类,属于___________ ;按聚集状态分类,属于___________ ;按溶解性分类,属于___________ 。
(2)根据碳酸钙的物质类别推知,下列说法或现象不合理的是___________。
(3)写出Ⅰ中发生主要反应的离子方程式___________ ;此反应是否属于氧化还原反应___________ (填“是”或“否”)。
(4)下列能在澄清石灰水中大量共存的离子组是___________。
(5)试用简要的文字说明Ⅲ中现象产生的原因___________ 。

(1)按要求填写碳酸钙的类别属性(如按正离子分类,碳酸钙属于钙盐):按负离子分类,属于
(2)根据碳酸钙的物质类别推知,下列说法或现象不合理的是___________。
| A.Ⅰ中的鸡蛋壳发生了分解反应 | B.Ⅰ中的鸡蛋壳表面产生气泡 |
| C.Ⅱ中的澄清石灰水变浑浊 | D.Ⅲ中紫色石蕊试液变浅红 |
(4)下列能在澄清石灰水中大量共存的离子组是___________。
A. 、 、 | B. 、 、 | C. 、 、 | D. 、 、 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】走进“化学村”。“化学村”的布局如下:
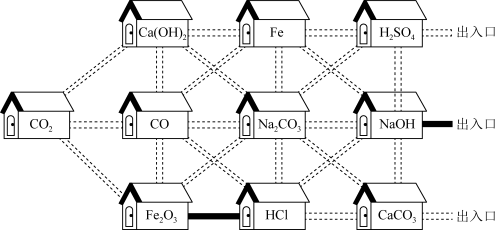
(1)10户“居民”中,俗称熟石灰的是___________ ,属于氧化物的有___________ 。
(2)“居民”CO与Fe2O3反应的化学方程式为___________ ,该反应是为___________ 。(填氧化还原反应或非氧化还原反应)

(1)10户“居民”中,俗称熟石灰的是
(2)“居民”CO与Fe2O3反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】汽车尾气(含有烃类、 、
、 、
、 等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂),它的特点是使
等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂),它的特点是使 和
和 反应,产生可参与大气循环的无毒气体,并促使烃类充分燃烧及
反应,产生可参与大气循环的无毒气体,并促使烃类充分燃烧及 的转化。
的转化。
(1)写出一氧化碳和一氧化氮反应的化学方程式:______________________________________ 。
(2)“催化转换器”的缺点是在一定程度上提高了空气的酸度,其原因是__________________ 。
 、
、 、
、 等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂),它的特点是使
等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂),它的特点是使 和
和 反应,产生可参与大气循环的无毒气体,并促使烃类充分燃烧及
反应,产生可参与大气循环的无毒气体,并促使烃类充分燃烧及 的转化。
的转化。(1)写出一氧化碳和一氧化氮反应的化学方程式:
(2)“催化转换器”的缺点是在一定程度上提高了空气的酸度,其原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】酸雨的形成
NO2形成酸雨的过程为___________ (用化学方程式表示)。
NO2形成酸雨的过程为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】下表是元素周期表的一部分,根据所给的10种元素,完成以下各小题。
(1)金属性最强的元素是___________ (填元素符号)。最不活泼元素的原子结构示意图为___________ 。
(2)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是___________ (填元素名称)。
(3)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式___________ 。
(4)工业上可以用Cl2和H2来制取盐酸,该反应的化学方程式为___________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | |||||||
| 2 | C | N | F | Ne | ||||
| 3 | Na | Mg | Al | S | Cl |
(1)金属性最强的元素是
(2)第3周期元素中,其最高价氧化物对应的水化物具有两性的元素是
(3)第3周期元素中,其元素的一种氧化物是形成酸雨的主要物质,该氧化物的化学式
(4)工业上可以用Cl2和H2来制取盐酸,该反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】回答下列问题:
(1)对于反应3X(g)+Y(g) Z(g),在其他条件不变时,改变其中一个条件,则生成Z的速率(填“增大”“减小”或“不变”):
Z(g),在其他条件不变时,改变其中一个条件,则生成Z的速率(填“增大”“减小”或“不变”):
①升高温度_____ ;
②加入催化剂_____ ;
③保持容器的体积不变,增加气体Ar____ ;
④保持压强不变,充入惰性气体____ 。
(2)某温度时,在一个2L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

①该反应的化学方程式为_____ 。
②反应开始至2min,以气体Z表示的平均反应速率为____ 。
(3)反应3A(g)+B(g) 2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为①vA=1mol/(L•min)、②vC=0.5mol/(L•min)、③vB=0.5mol/(L•min),三种情况下该反应速率由大到小的关系是
2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为①vA=1mol/(L•min)、②vC=0.5mol/(L•min)、③vB=0.5mol/(L•min),三种情况下该反应速率由大到小的关系是____ 。(用序号表示)
(1)对于反应3X(g)+Y(g)
 Z(g),在其他条件不变时,改变其中一个条件,则生成Z的速率(填“增大”“减小”或“不变”):
Z(g),在其他条件不变时,改变其中一个条件,则生成Z的速率(填“增大”“减小”或“不变”):①升高温度
②加入催化剂
③保持容器的体积不变,增加气体Ar
④保持压强不变,充入惰性气体
(2)某温度时,在一个2L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

①该反应的化学方程式为
②反应开始至2min,以气体Z表示的平均反应速率为
(3)反应3A(g)+B(g)
 2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为①vA=1mol/(L•min)、②vC=0.5mol/(L•min)、③vB=0.5mol/(L•min),三种情况下该反应速率由大到小的关系是
2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为①vA=1mol/(L•min)、②vC=0.5mol/(L•min)、③vB=0.5mol/(L•min),三种情况下该反应速率由大到小的关系是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】CH3OH也可由CO2和H2合成。在体积为1L的密闭容器中,充入lmolCO2和3molH2,一定条件下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2和CH3OH(g)浓度随时间变化如图所示:
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)浓度随时间变化如图所示:___________ mol/(L·min)。
(2)10min时,CH3OH的物质的量为___________ mol,10min内,以H2表示的化学反应速率是___________ mol/(L·min)。
(3)到达平衡时,CO2的转化率为___________ 。
(4)3min时,v(正)___________ v(逆)(填“大于”、“等于”、“小于”),此时化学反应朝___________ 进行(填“正方向”或“逆方向”)。
 CH3OH(g)+H2O(g),测得CO2和CH3OH(g)浓度随时间变化如图所示:
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)浓度随时间变化如图所示:
(2)10min时,CH3OH的物质的量为
(3)到达平衡时,CO2的转化率为
(4)3min时,v(正)
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】(1)某温度时,在2 L容器中三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式_______ 和反应开始至2 min末Z的平均反应速率分别为_______

(2)在1 L密闭容器中,把1 mol A和1 mol B混合发生如下反应:3A(g)+B(g) xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则
xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则
①x的值为___________ ;
②B的平衡浓度为___________ ;
③A的转化率为___________ ;
④D的体积分数为___________ ;

(2)在1 L密闭容器中,把1 mol A和1 mol B混合发生如下反应:3A(g)+B(g)
 xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则
xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol/L,则 ①x的值为
②B的平衡浓度为
③A的转化率为
④D的体积分数为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】用纯净的锌粒与100mL2mol/L稀盐酸反应制取氢气,请回答:
(1)实验过程如下图所示,图中

(2)为了加快上述反应的速率,欲向溶液中加入少量下列物质,你认为可行的是
A蒸馏水 B氯化铜固体 C氯化钠溶液 D浓盐酸
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某酸性工业废水中含有K2Cr2O7.光照下,草酸(H2C2O4)能将其中的Cr2O 转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)在25 ℃下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,做对比实验,完成以下实验设计表(表中不要留空格)。
测得实验①和②溶液中的Cr2O 浓度随时间变化关系如图所示。
浓度随时间变化关系如图所示。

(2)上述反应后草酸被氧化为___________ (填化学式)。
(3)实验①和②的结果表明___________ ;实验①中0~t1时间段反应速率v(Cr3+)=___________ mol·L-1·min-1(用代数式表示)。
 转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:(1)在25 ℃下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,做对比实验,完成以下实验设计表(表中不要留空格)。
| 实验编号 | 初始pH | 废水样品体积/mL | 草酸溶液体积/mL | 蒸馏水体积/mL |
| ① | 4 | 60 | 10 | 30 |
| ② | 5 | 60 | 10 | 30 |
| ③ | 5 | 60 |
 浓度随时间变化关系如图所示。
浓度随时间变化关系如图所示。
(2)上述反应后草酸被氧化为
(3)实验①和②的结果表明
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】硫酸的消费量是衡量一个国家化工生产水平的重要标志。而在硫酸的生产中,最关键的一步反应为:2SO2(g)+O2(g) 2SO3(g)。
2SO3(g)。
(1)一定条件下,SO2与O2反应10min后,若SO2和SO3物质的量浓度分别为1mol/L和3mol/L,则SO2起始物质的量浓度为___________________ ;10min生成SO3的化学反应速率为___________________ 。
(2)下列关于该反应的说法正确的是___________________ 。
A.增加O2的浓度能加快反应速率
B.降低体系温度能加快反应速率
C.使用催化剂能加快反应速率
D.一定条件下达到反应限度时SO2全部转化为SO3
(3)工业制硫酸,用过量的氨水对SO2尾气处理,请写出相关的离子方程式:____________ 。
 2SO3(g)。
2SO3(g)。(1)一定条件下,SO2与O2反应10min后,若SO2和SO3物质的量浓度分别为1mol/L和3mol/L,则SO2起始物质的量浓度为
(2)下列关于该反应的说法正确的是
A.增加O2的浓度能加快反应速率
B.降低体系温度能加快反应速率
C.使用催化剂能加快反应速率
D.一定条件下达到反应限度时SO2全部转化为SO3
(3)工业制硫酸,用过量的氨水对SO2尾气处理,请写出相关的离子方程式:
您最近一年使用:0次

 2Fe+3CO2的化学反应中,
2Fe+3CO2的化学反应中,

