下图是氮气及几种氮的化合物间的转换关系。请回答下列问题:

(1)请写出工业合成氨的化学方程式_______ 。
(2)工业上常用NH3制取NO,请写出反应的化学方程式_______ 。
(3)实验室里常用Cu与稀硝酸反应制取NO,当生成标准状况下3.36LNO时,转移的电子数为_______ 。
(4)生产硝酸时排放的NO会污染环境,一种治理方案是用氨气在催化剂作用下将NO还原成N2,请写出化学方程式:_______ 。
(5)有一瓶稀硫酸和稀硝酸的混合溶液,其中c(H2SO4)=2.0mol·L-1,c(HNO3)=1.0mol·L-1。取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为_______ L。

(1)请写出工业合成氨的化学方程式
(2)工业上常用NH3制取NO,请写出反应的化学方程式
(3)实验室里常用Cu与稀硝酸反应制取NO,当生成标准状况下3.36LNO时,转移的电子数为
(4)生产硝酸时排放的NO会污染环境,一种治理方案是用氨气在催化剂作用下将NO还原成N2,请写出化学方程式:
(5)有一瓶稀硫酸和稀硝酸的混合溶液,其中c(H2SO4)=2.0mol·L-1,c(HNO3)=1.0mol·L-1。取100mL该混合溶液与12.8g铜粉反应,标准状况下生成NO的体积为
更新时间:2021-04-12 18:58:50
|
相似题推荐
【推荐1】近来,《饮用天然矿泉水》新标准引起热议,其中备受争议的溴酸盐是一种致癌物,新标准中溴酸盐极值为0.01mg/L。已知在酸性条件下有以下反应:
①2 +I2===2
+I2===2 +Br2
+Br2
②2 +10Br-+12H+===I2+5Br2+6H2O
+10Br-+12H+===I2+5Br2+6H2O
③5Br-+ +6H+===3Br2+3H2O
+6H+===3Br2+3H2O
请回答下列问题:
(1)有同学根据反应①得出氧化性:I2>Br2的结论,请说明该结论错误的理由是:_________ 。
(2)反应②中: →l2发生的是
→l2发生的是__________ 反应(氧化、还原)。
现向含6mol的KI的硫酸溶液中逐滴滴加KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量有如图的关系:
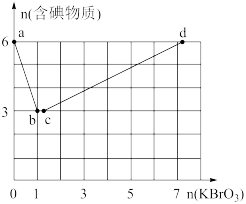
(3)完成a→b阶段的反应方程式,并标出电子转移的方向和数目:I-+BrO3-+H+→ ,________ 。
(4)b→c阶段只有一种元素化合价发生了改变,反应中氧化产物和还原产物的物质的量之比为______ 。
(5)a→b、b→c、c→d阶段的还原剂分别是______ 、_______ 、______ ,依次发生的这些反应,说明有关物质(l2、Br2、I-、Br-)还原性由强到弱的顺序是________ 。
①2
 +I2===2
+I2===2 +Br2
+Br2②2
 +10Br-+12H+===I2+5Br2+6H2O
+10Br-+12H+===I2+5Br2+6H2O③5Br-+
 +6H+===3Br2+3H2O
+6H+===3Br2+3H2O请回答下列问题:
(1)有同学根据反应①得出氧化性:I2>Br2的结论,请说明该结论错误的理由是:
(2)反应②中:
 →l2发生的是
→l2发生的是现向含6mol的KI的硫酸溶液中逐滴滴加KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量有如图的关系:

(3)完成a→b阶段的反应方程式,并标出电子转移的方向和数目:I-+BrO3-+H+→ ,
(4)b→c阶段只有一种元素化合价发生了改变,反应中氧化产物和还原产物的物质的量之比为
(5)a→b、b→c、c→d阶段的还原剂分别是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】氯化铁和摩尔盐是铁的两种重要盐类,在净水和定量分析等方面具有重要作用。
(1) 用FeCl3溶液腐蚀印刷电路板上的铜,向所得溶液中加入铁粉,对加入铁粉充分反应后的溶液分析合理的是____________ 。
a. 若无固体剩余,则溶液中一定有Fe3+ b. 若有固体存在,则溶液中一定有Fe2+
c. 若溶液中有Cu2+,则一定没有固体析出 d. 若溶液中有Fe2+,则一定有Cu析出
(2)工业上通过氧化酸性FeCl2废液得到含FeCl3的溶液。若酸性FeCl2废液中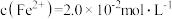 ,
,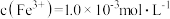 ,
,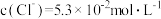 ,则该溶液的
,则该溶液的 约为
约为______ (不考虑水的电离和离子的水解)。
(3)摩尔盐 [(NH4)2Fe(SO4)2•6H2O]在定量分析中常作为基准物质,用来标定重铬酸钾、高锰酸钾等溶液的浓度,在 的该盐的溶液中,离子浓度由大到小的顺序是
的该盐的溶液中,离子浓度由大到小的顺序是____________ 。
(4)摩尔盐与酸性高锰酸钾发生反应: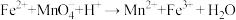
a.配平上述离子方程式:( ) Fe2++( ) MnO4-+( ) H+→( ) Mn2++( ) Fe3++( ) H2O
b.已知摩尔盐相对分子质量为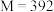 ,取摩尔盐产品
,取摩尔盐产品 (杂质不与高锰酸钾反应),配成
(杂质不与高锰酸钾反应),配成 溶液,取出
溶液,取出 用
用 溶液滴定,消耗
溶液滴定,消耗 溶液
溶液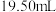 ,则产品中摩尔盐的质量分数为
,则产品中摩尔盐的质量分数为____________ (用小数表示,保留四位小数)。
(1) 用FeCl3溶液腐蚀印刷电路板上的铜,向所得溶液中加入铁粉,对加入铁粉充分反应后的溶液分析合理的是
a. 若无固体剩余,则溶液中一定有Fe3+ b. 若有固体存在,则溶液中一定有Fe2+
c. 若溶液中有Cu2+,则一定没有固体析出 d. 若溶液中有Fe2+,则一定有Cu析出
(2)工业上通过氧化酸性FeCl2废液得到含FeCl3的溶液。若酸性FeCl2废液中
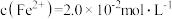 ,
,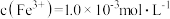 ,
,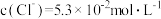 ,则该溶液的
,则该溶液的 约为
约为(3)摩尔盐 [(NH4)2Fe(SO4)2•6H2O]在定量分析中常作为基准物质,用来标定重铬酸钾、高锰酸钾等溶液的浓度,在
 的该盐的溶液中,离子浓度由大到小的顺序是
的该盐的溶液中,离子浓度由大到小的顺序是(4)摩尔盐与酸性高锰酸钾发生反应:
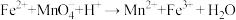
a.配平上述离子方程式:
b.已知摩尔盐相对分子质量为
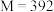 ,取摩尔盐产品
,取摩尔盐产品 (杂质不与高锰酸钾反应),配成
(杂质不与高锰酸钾反应),配成 溶液,取出
溶液,取出 用
用 溶液滴定,消耗
溶液滴定,消耗 溶液
溶液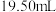 ,则产品中摩尔盐的质量分数为
,则产品中摩尔盐的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】Ⅰ.目前合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用氧化气化法提纯,其反应式为:
___C+ K2Cr2O7+___H2SO4===___CO2↑+___Cr2(SO4)3+___K2SO4+___H2O
(1)配平上述化学反应方程式(请将配平的计量数依次填入上式)_____________ 。
(2)该反应的氧化剂是______________ ,氧化产物的电子式为__________________ 。
(3)H2SO4在上述反应中表现出来的性质是________ (填选项编号)。
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应中若产生0.2 mol CO2 ,则转移电子的物质的量是_________ mol。
Ⅱ.三氟化氮(NF3)是一种无色无味的气体,可由氟与氨在一定条件下反应制得。
(1)写出该反应化学方程式并标明电子转移的方向和数目____________________________ 。
(2)27.0 mL NF3和水充分反应,生成 18.0 mL NO(同温、同压下),写出反应的化学方程式:______________________________________________________________________ 。
(3)NF3是一种无色无味的气体,但一旦NF3在空气中泄漏,还是易于发现的。该气体泄漏时的现象是_________________________________________________________________ 。
___C+ K2Cr2O7+___H2SO4===___CO2↑+___Cr2(SO4)3+___K2SO4+___H2O
(1)配平上述化学反应方程式(请将配平的计量数依次填入上式)
(2)该反应的氧化剂是
(3)H2SO4在上述反应中表现出来的性质是
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应中若产生0.2 mol CO2 ,则转移电子的物质的量是
Ⅱ.三氟化氮(NF3)是一种无色无味的气体,可由氟与氨在一定条件下反应制得。
(1)写出该反应化学方程式并标明电子转移的方向和数目
(2)27.0 mL NF3和水充分反应,生成 18.0 mL NO(同温、同压下),写出反应的化学方程式:
(3)NF3是一种无色无味的气体,但一旦NF3在空气中泄漏,还是易于发现的。该气体泄漏时的现象是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】氮及氮的化合物有着重要的用途。
(1)将空气中游离态的氮转化为含氮化合物的过程叫氮的固定,请举例说明一种自然界中氮的固定的途径_________________ (用化学方程式表示)。
(2)选择性催化还原技术(SCR)可使NOx与NH3直接反应,实现无害转化。当NO与NO2的物质的量之比为2:1时,写出发生反应的化学 方程式:___________________ 。
(3)利用ClO2氧化氮氧化物反应过程如下:NO NO2
NO2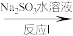 N2。反应Ⅰ的化学方程式是2NO+ClO2+H2O=NO2+HNO3+HCl,请写出反应Ⅱ转化关系的
N2。反应Ⅰ的化学方程式是2NO+ClO2+H2O=NO2+HNO3+HCl,请写出反应Ⅱ转化关系的离子 方程式___________________________ 。
(4)加入过量次氯酸钠可使废水中 完全转化为N2,而本身被还原为NaCl。
完全转化为N2,而本身被还原为NaCl。
①写出次氯酸的电子式__________________________________ 。
②上述反应中氧化剂和还原剂的物质的量之比为____________ ;若处理废水产生了0.448 L N2(标准状况),则至少需消耗浓度为2 mol·L-1的次氯酸钠的体积为______________ mL。
(5)“化学,让生活更美好”,下列叙述不能直接体现这一主旨的是( )
A.风力发电,让能源更清洁 B.合成光纤,让通讯更快捷
C.合成药物,让人类更健康 D.环保涂料,让环境更宜居
(1)将空气中游离态的氮转化为含氮化合物的过程叫氮的固定,请举例说明一种自然界中氮的固定的途径
(2)选择性催化还原技术(SCR)可使NOx与NH3直接反应,实现无害转化。当NO与NO2的物质的量之比为2:1时,写出发生反应的
(3)利用ClO2氧化氮氧化物反应过程如下:NO
 NO2
NO2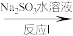 N2。反应Ⅰ的化学方程式是2NO+ClO2+H2O=NO2+HNO3+HCl,请写出反应Ⅱ转化关系的
N2。反应Ⅰ的化学方程式是2NO+ClO2+H2O=NO2+HNO3+HCl,请写出反应Ⅱ转化关系的(4)加入过量次氯酸钠可使废水中
 完全转化为N2,而本身被还原为NaCl。
完全转化为N2,而本身被还原为NaCl。①写出次氯酸的电子式
②上述反应中氧化剂和还原剂的物质的量之比为
(5)“化学,让生活更美好”,下列叙述不能直接体现这一主旨的是
A.风力发电,让能源更清洁 B.合成光纤,让通讯更快捷
C.合成药物,让人类更健康 D.环保涂料,让环境更宜居
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】工业上利用氨催化氧化法可制取硝酸,加入脱水剂后制得较高浓度的硝酸。现以17吨氨作为原料,假设NH3全部转化为HNO3。
(1)写出NH3完全转化为HNO3的总化学反应方程式___________________ ;
(2)生产过程中需加水吸收,如果加入脱水剂后脱去水的量相等,则所得硝酸溶液的质量分数为__________ ?
(3)如果生产中同时制得50%的硝酸m1吨和90%的硝酸m2吨(脱去的水可循环使用,制得较低浓度的稀硝酸),若共加入27吨水,则m1与m2的质量比为__________ ?
(1)写出NH3完全转化为HNO3的总化学反应方程式
(2)生产过程中需加水吸收,如果加入脱水剂后脱去水的量相等,则所得硝酸溶液的质量分数为
(3)如果生产中同时制得50%的硝酸m1吨和90%的硝酸m2吨(脱去的水可循环使用,制得较低浓度的稀硝酸),若共加入27吨水,则m1与m2的质量比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和 混合气体在标准状况下的体积为11.2L。请回答:
混合气体在标准状况下的体积为11.2L。请回答:
(1)求NO和 混合气体的平均摩尔质量
混合气体的平均摩尔质量_______ 。
(2)待产生的气体全部释放后,向溶液加入V mL浓度为a mol/L的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为___________ mol/L。
(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为 ,至少需要30%的过氧化氢
,至少需要30%的过氧化氢___________ g。
 混合气体在标准状况下的体积为11.2L。请回答:
混合气体在标准状况下的体积为11.2L。请回答:(1)求NO和
 混合气体的平均摩尔质量
混合气体的平均摩尔质量(2)待产生的气体全部释放后,向溶液加入V mL浓度为a mol/L的NaOH溶液,恰好使溶液中的
 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为
 ,至少需要30%的过氧化氢
,至少需要30%的过氧化氢
您最近一年使用:0次
【推荐2】将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。请回答:
(1)NO的体积为_____ L,NO2的体积为______ L。
(2)参加反应的硝酸的物质的量是_______ mol。
(3)待产生的气体全部释放后,向溶液加入VmL a mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为___________ mol/L。(结果不需化简)
(4)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水________ g。
(1)NO的体积为
(2)参加反应的硝酸的物质的量是
(3)待产生的气体全部释放后,向溶液加入VmL a mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为
(4)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】取m克铁粉与1 L 1.2 mol/L的稀HNO3恰好完全反应,反应后的溶液中只含Fe2+且硝酸的还原产物只有NO。则:
(1)m=______________ g。
(2)若将反应后的溶液低温蒸干,析出晶体135 g,则析出晶体的组成可能是_________ 。
a.Fe(NO3)2∙7H2O和Fe(NO3)2∙4H2O
b.Fe(NO3)2∙7H2O和Fe(NO3)2∙H2O
c.Fe(NO3)2∙4H2O和Fe(NO3)2∙H2O
(3)若向反应后的溶液中加入100 mL 1.5 mol/L的稀H2SO4,则标准状态下还能产生NO的体积为______ L。
(1)m=
(2)若将反应后的溶液低温蒸干,析出晶体135 g,则析出晶体的组成可能是
a.Fe(NO3)2∙7H2O和Fe(NO3)2∙4H2O
b.Fe(NO3)2∙7H2O和Fe(NO3)2∙H2O
c.Fe(NO3)2∙4H2O和Fe(NO3)2∙H2O
(3)若向反应后的溶液中加入100 mL 1.5 mol/L的稀H2SO4,则标准状态下还能产生NO的体积为
您最近一年使用:0次

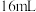 由
由 与
与 组成的混合气体在催化剂作用下于
组成的混合气体在催化剂作用下于 左右可发生反应:
左右可发生反应: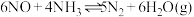 ,达到平衡时在相同条件下气体体积变为
,达到平衡时在相同条件下气体体积变为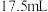 ,计算原混合气体中
,计算原混合气体中

