下列说法不正确的是
①N2H4分子中既含极性键又含非极性键
②若R2-和M+的电子层结构相同,则原子序数:R>M
③F2、Cl2、Br2、I2熔点逐渐增大
④NCl3、PCl3、CO2、CS2分子中各原子均达到8e-稳定结构
⑤固体熔化成液体的过程是物理变化,所以不会破坏化学键
⑥HF分子很稳定是由于HF分子之间能形成氢键
⑦由于非金属性:Cl>Br>I,所以酸性:HCl>HBr>HI
①N2H4分子中既含极性键又含非极性键
②若R2-和M+的电子层结构相同,则原子序数:R>M
③F2、Cl2、Br2、I2熔点逐渐增大
④NCl3、PCl3、CO2、CS2分子中各原子均达到8e-稳定结构
⑤固体熔化成液体的过程是物理变化,所以不会破坏化学键
⑥HF分子很稳定是由于HF分子之间能形成氢键
⑦由于非金属性:Cl>Br>I,所以酸性:HCl>HBr>HI
| A.③⑤⑦ | B.①③⑤ | C.②④⑤ | D.②⑤⑥⑦ |
更新时间:2021-04-20 09:37:53
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期主族元素 A、B、C、D的原子序数依次增大,p区元素 A 的基态原子的电子总数是其最高能级电子数的2倍,C 的周期数是族序数的3倍,B 和 D 价电子数相同。下列叙述正确的是
A.简单离子半径大小顺序为  |
| B.A 和 B 两元素不能形成化合物 |
| C.A 和 D形成的一种化合物可用于饮用水的消毒 |
| D.C 与其他三种元素分别形成的化合物中只含有离子键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知W、X、Y、Z均为短周期元素,常温下,它们的最高价氧化物对应的水化物溶液(浓度均为 )的pH和原子半径、原子序数的关系如图所示。下列说法正确的是
)的pH和原子半径、原子序数的关系如图所示。下列说法正确的是
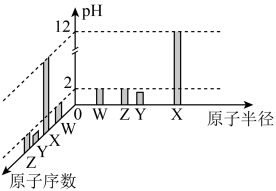
 )的pH和原子半径、原子序数的关系如图所示。下列说法正确的是
)的pH和原子半径、原子序数的关系如图所示。下列说法正确的是
| A.电负性:Z<Y |
| B.简单离子半径:Z>Y>W>X |
C.元素W形成的某阳离子 空间构型为正四面体 空间构型为正四面体 |
D.化合物 中含有极性共价键和非极性共价键 中含有极性共价键和非极性共价键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】主族元素 、
、 、
、 、
、 的原子序数依次增加,且均不大于20。
的原子序数依次增加,且均不大于20。 、
、 、
、 族序数之和为10;
族序数之和为10; 的原子半径在同周期主族元素中最小;
的原子半径在同周期主族元素中最小; 与
与 形成的化合物常温下可与饱和
形成的化合物常温下可与饱和 溶液反应,产生的气体常用于切割和焊接金属。下列说法错误的是
溶液反应,产生的气体常用于切割和焊接金属。下列说法错误的是
 、
、 、
、 、
、 的原子序数依次增加,且均不大于20。
的原子序数依次增加,且均不大于20。 、
、 、
、 族序数之和为10;
族序数之和为10; 的原子半径在同周期主族元素中最小;
的原子半径在同周期主族元素中最小; 与
与 形成的化合物常温下可与饱和
形成的化合物常温下可与饱和 溶液反应,产生的气体常用于切割和焊接金属。下列说法错误的是
溶液反应,产生的气体常用于切割和焊接金属。下列说法错误的是A.简单离子半径: |
B. 的单质是人类将太阳能转化为电能的常用材料 的单质是人类将太阳能转化为电能的常用材料 |
C. 与 与 形成的化合物均满足8电子稳定结构 形成的化合物均满足8电子稳定结构 |
D. 与 与 形成的化合物与饱和 形成的化合物与饱和 溶液的反应可选用启普发生器 溶液的反应可选用启普发生器 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】与 晶体中所含化学键类型相同的物质是
晶体中所含化学键类型相同的物质是
 晶体中所含化学键类型相同的物质是
晶体中所含化学键类型相同的物质是A. | B. | C. | D. |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列分子中,所有原子均满足8电子稳定结构的是( )
| A.C2H4 | B.H2S | C.Cl2 | D.NH3 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
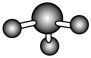
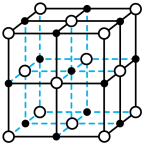
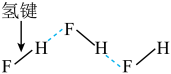
【推荐1】下列示意图正确的是
。
|
|
|
|
A. 的VSEPR模型 的VSEPR模型 | B.氯化铯的晶胞结构图 | C. 分子间的氢键 分子间的氢键 | D.丙氨酸的手性异构体 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列物质的变化过程中,只需克服分子间作用力的是( )
| A.食盐溶解 | B.氯化氢溶于水 | C.干冰升华 | D.氯化铵分解 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.只含有一种元素的物质一定是纯净物 |
| B.H2O汽化成水蒸气、分解为H2和O2,都需要破坏共价键 |
| C.CCl4分子中,每个原子的最外电子层都具有8电子稳定结构 |
| D.HF很稳定是因为HF分子间存在氢键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列叙述中正确的是
| A.SiO2是酸性氧化物可以和水反应生成硅酸 |
| B.HF很稳定,是因为HF分子间存在着氢键 |
| C.Na 和Cs 属于第IA 族元素,Cs 失电子能力比Na的强 |
| D.P 和As属于第VA 族元素,H3PO4酸性比H3AsO4的弱 |
您最近半年使用:0次

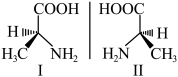
 )再生的绿色甲醇(
)再生的绿色甲醇( )作为主火炬塔燃料,实现循环内的零排放。下列说法错误的是
)作为主火炬塔燃料,实现循环内的零排放。下列说法错误的是 杂化,O为
杂化,O为 杂化
杂化

