(1)有以下四种物质 ①22gCO2;②5gH2;③1.204×1024个N2;④4℃时18gH2O,它们所含分子数最多的是_______ ;质量最大的是_______ ;常温时体积最大的是_______ (填序号)。
(2)在标准状况下,448mL某气体的质量为0.64g,则这种气体的相对分子质量为_______
(3)某FeCl3和NaCl的混合液,已知c(Fe3+)= 0.2 mol·L-1,c(Cl-)= 1 mol·L-1,则c(Na+)=_______ (忽略H+和OH-浓度)
(4)VL Fe2(SO4)3溶液中含Fe3+ m g,则溶液中 的物质的量浓度为
的物质的量浓度为_______
(5)在无土栽培中,配制1L含5mol NH4Cl、1.6mol KCl、2.4mol K2SO4的营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为_______ 、_______
(6)已知2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑,氧化剂与还原剂的物质的量之比是_______ ,HCl在反应中表现的性质有_______
(2)在标准状况下,448mL某气体的质量为0.64g,则这种气体的相对分子质量为
(3)某FeCl3和NaCl的混合液,已知c(Fe3+)= 0.2 mol·L-1,c(Cl-)= 1 mol·L-1,则c(Na+)=
(4)VL Fe2(SO4)3溶液中含Fe3+ m g,则溶液中
 的物质的量浓度为
的物质的量浓度为(5)在无土栽培中,配制1L含5mol NH4Cl、1.6mol KCl、2.4mol K2SO4的营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为
(6)已知2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑,氧化剂与还原剂的物质的量之比是
更新时间:2021-04-26 08:36:38
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】某铝土矿的主要成分为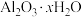 ,还含有
,还含有 和
和 杂质。称取
杂质。称取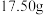 铝土矿样品,加入
铝土矿样品,加入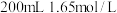 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。
(1)该试样中 的物质的量为
的物质的量为___________ mol。
(2)样品中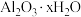 的x=
的x=___________ 。
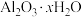 ,还含有
,还含有 和
和 杂质。称取
杂质。称取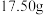 铝土矿样品,加入
铝土矿样品,加入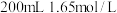 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。(1)该试样中
 的物质的量为
的物质的量为(2)样品中
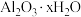 的x=
的x=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】将甲烷和乙烯的混合气体共0.2mol通入溴水中,发生反应的化学方程式是_______ ,反应的类型为__________ ,若充分反应后溴水增重2.8克,则原混合气体中甲烷和乙烯的物质的量之比为______ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】回答下列问题
(1)1.5molH2SO4的质量是_______ ,其中含有_______ molH,含有_______ g氧。
(2)4.4gCO2的物质的量是_______ ,其中含有二氧化碳分子_______ 个,电子_______ 个,它在标况下占有的体积为_______ 。
(3)等质量的HCl、NH3、CO2、O2四种气体,在相同温度和相同压强条件下,体积最大的是_______ 。
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为_______ ,R的相对原子质量为_______ 。
(5)实验室需要0.1mol/L的氢氧化钠溶液100mL,其中需要2mol/L的氢氧化钠溶液_______ mL,将71 g Na2SO4溶于水配成1 L溶液,该溶液中Na2 SO4的物质的量浓度为_______ ,溶液中Na+的物质的量浓度为_______
(1)1.5molH2SO4的质量是
(2)4.4gCO2的物质的量是
(3)等质量的HCl、NH3、CO2、O2四种气体,在相同温度和相同压强条件下,体积最大的是
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为
(5)实验室需要0.1mol/L的氢氧化钠溶液100mL,其中需要2mol/L的氢氧化钠溶液
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】以“物质的量”为中心的计算是化学计算的基础,请根据所学知识回答下列问题。
(1) 个
个 的物质的量是
的物质的量是______ ,与______ g  含有的氧原子数相等。
含有的氧原子数相等。
(2)相同质量的 和
和 所含硫原子的个数之比为
所含硫原子的个数之比为______ 。
(3)某无土栽培用的营养液中, ,若用
,若用 、KCl、
、KCl、 来配制该营养液,则这三种盐的物质的量之比为
来配制该营养液,则这三种盐的物质的量之比为______ 。
(4)将0.1 的
的 溶液由a mL稀释至b mL,稀释后溶液中
溶液由a mL稀释至b mL,稀释后溶液中 的物质的量浓度是
的物质的量浓度是______ (用含a、b的代数式表示)
(5)把一定量的铁粉放入过量的盐酸中,得到5.6L (标准状况),参加反应的铁粉物质的量是
(标准状况),参加反应的铁粉物质的量是___ (写出详细的计算步骤)
(1)
 个
个 的物质的量是
的物质的量是 含有的氧原子数相等。
含有的氧原子数相等。(2)相同质量的
 和
和 所含硫原子的个数之比为
所含硫原子的个数之比为(3)某无土栽培用的营养液中,
 ,若用
,若用 、KCl、
、KCl、 来配制该营养液,则这三种盐的物质的量之比为
来配制该营养液,则这三种盐的物质的量之比为(4)将0.1
 的
的 溶液由a mL稀释至b mL,稀释后溶液中
溶液由a mL稀释至b mL,稀释后溶液中 的物质的量浓度是
的物质的量浓度是(5)把一定量的铁粉放入过量的盐酸中,得到5.6L
 (标准状况),参加反应的铁粉物质的量是
(标准状况),参加反应的铁粉物质的量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】铜、铁、锌等质量合成的合金W g,加入FeCl3和盐酸的混合液中,充分反应后:
(1)若无固体剩余,则溶液中的阳离子一定有_______ ,还可能有_______ 。
(2)若剩余固体为 g,则溶液中的阳离子一定有
g,则溶液中的阳离子一定有_______ ,可能还有_______ 。一定没有_______ 。
(3)若剩余固体为 g,则溶液中的阳离子一定有
g,则溶液中的阳离子一定有_______ ,一定没有_______ 。
(1)若无固体剩余,则溶液中的阳离子一定有
(2)若剩余固体为
 g,则溶液中的阳离子一定有
g,则溶液中的阳离子一定有(3)若剩余固体为
 g,则溶液中的阳离子一定有
g,则溶液中的阳离子一定有
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)在反应2KMnO4+16HBr=5Br2+2MnBr2+2KBr+8H2O中,还原剂是 。
(2)浓盐酸在反应___KClO3+___HCl→___KCl+___ClO2+___Cl2+___ ____ (补充完整此项化学式及化学计量数)中显示出来的性质是 。
(3)在一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为 。
(2)浓盐酸在反应___KClO3+___HCl→___KCl+___ClO2+___Cl2+___ ____ (补充完整此项化学式及化学计量数)中显示出来的性质是 。
(3)在一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】亚硝酰硫酸(HOSO3NO)是一种浅黄色或蓝紫色液体,能溶于浓硫酸,与水反应,主要用于印染、医药领域的重氮化反应中替代亚硝酸钠。实验室用下图所示装置(部分夹持装置略)制备少量HOSO3NO,并测定产品纯度。

测定HOSO3NO的纯度:准确称取1.350g产品放入250mL碘量瓶中,加入60.00mL0.1000mol•L-1KMnO4标准溶液和10mL25%硫酸溶液,摇匀(过程中无气体产生);用0.2500mol•L-1草酸钠标准溶液滴定,平均消耗草酸钠标准溶液的体积为20.00mL。已知:2KMnO4+5HOSO3NO+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4。
①上述反应中,HOSO3NO体现了_______ (填“氧化”或“还原”)性。
②亚硝酰硫酸的纯度为_______ (计算结果保留4位有效数字)。

测定HOSO3NO的纯度:准确称取1.350g产品放入250mL碘量瓶中,加入60.00mL0.1000mol•L-1KMnO4标准溶液和10mL25%硫酸溶液,摇匀(过程中无气体产生);用0.2500mol•L-1草酸钠标准溶液滴定,平均消耗草酸钠标准溶液的体积为20.00mL。已知:2KMnO4+5HOSO3NO+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4。
①上述反应中,HOSO3NO体现了
②亚硝酰硫酸的纯度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室还可以利用高锰酸钾制氯气,其原理为:2KMnO4 + 16HCl = 2KCl + 2MnCl 2+ 5Cl 2↑ + 8H2O,若有15.8g KMnO4做氧化剂,试计算参加反应盐酸的物质的量和被氧化的盐酸的质量____________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】磷及部分重要化合物的相互转化如图所示.

①步骤Ⅰ为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,其中SiO2的作用是用于造渣(CaSiO3),焦炭的作用是________ ;
②不慎将白磷沾到皮肤上,可用0.2mol/LCuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol/LCuSO4溶液所能氧化的白磷的物质的量为________ .

①步骤Ⅰ为白磷的工业生产方法之一,反应在1300℃的高温炉中进行,其中SiO2的作用是用于造渣(CaSiO3),焦炭的作用是
②不慎将白磷沾到皮肤上,可用0.2mol/LCuSO4溶液冲洗,根据步骤Ⅱ可判断,1mol/LCuSO4溶液所能氧化的白磷的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】实验室用50 mL浓盐酸跟足量的氯酸钾固体共热制取氯气,该反应的化学方程式为KClO3+6HCl(浓) ===3Cl2↑+KCl+3H2O。
(1)浓盐酸在此反应中所具有的性质是__________ (填写编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)若产生0.3 mol Cl2,求反应中转移的电子数__________ 。
(3)若反应中HCl的利用率为50%,当反应结束时,生成氯气0.15 mol,则浓盐酸的物质的量浓度为_________ 。
(1)浓盐酸在此反应中所具有的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)若产生0.3 mol Cl2,求反应中转移的电子数
(3)若反应中HCl的利用率为50%,当反应结束时,生成氯气0.15 mol,则浓盐酸的物质的量浓度为
您最近一年使用:0次


 和
和 中,氢原子的个数比是
中,氢原子的个数比是 与
与 的体积比为
的体积比为 、
、 、
、 、
、

