缺电子化合物是指分子中的原子通过共享电子,其价层电子数未达到8(H原子除外)的一类化合物。下列说法错误的是
| A.B2H6是缺电子化合物 |
| B.BeCl2的二聚体是平面分子 |
| C.AlCl3的二聚体中有配位键,中心原子的杂化方式为sp2 |
| D.化合物BF3与NH3形成的配位化合物为H3N→BF3 |
2021·山东潍坊·三模 查看更多[2]
更新时间:2021-05-28 12:01:30
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列元素最易形成共价键的是( )
| A.Na | B.Mg | C.Al | D.Si |
您最近一年使用:0次
【推荐2】中国航天科技发展举世瞩目。2020年“嫦娥五号”成功携带月球样品返回地球,2021年“天问一号”着陆火星,它们都是由以液氢为燃料的“长征五号”火箭搭载升空的。下列有关说法错误的是
| A.氢气燃烧时有非极性键的断裂和形成 |
| B.氢气燃烧的产物不污染环境,有利于实现“碳中和” |
| C.低温液态储氢可以大大提高氢气的密度,降低储运成本 |
| D.氢气的来源较多,包括水的电解、煤的气化、乙烷裂解和氯碱工业等 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列分子中,各原子未处于同一平面上的是
| A.NH3 | B.C2H4 | C.H2O | D.CH2O |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】对下列事实的解释不正确 的是
| 选项 | 事实 | 解释 |
| A | 稳定性: | H-F键键能大于H-I键键能。 |
| B | 键角: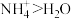 | 中心原子均采取 杂化,孤电子对有较大的斥力 杂化,孤电子对有较大的斥力 |
| C | 熔点:石英>干冰 | 石英是共价晶体,干冰是分子晶体;共价键比分子间作用力强 |
| D | 金属活动性: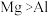 | 第一电离能: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列说法错误的是
A.沸点:邻羟基苯甲酸(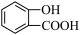 )<对羟基苯甲酸( )<对羟基苯甲酸(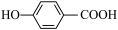 ) ) |
| B.根据对角线规则,锂与镁性质相似,锂燃烧生成氧化锂而不是过氧化锂 |
| C.钠的焰色试验呈黄色是原子核外电子跃迁释放能量的结果 |
D.甲烷分子失去一个 ,形成甲基阳离子 ,形成甲基阳离子 ,变化过程中微粒的键角发生了改变,但碳原子的杂化类型没有改变 ,变化过程中微粒的键角发生了改变,但碳原子的杂化类型没有改变 |
您最近一年使用:0次
【推荐2】阴离子 和二脲基分子能通过一种弱相互作用形成超分子阴离子配合物,如下图所示(图中省略阴离子配合物中部分原子)。下列关于该阴离子配合物的说法正确的是
和二脲基分子能通过一种弱相互作用形成超分子阴离子配合物,如下图所示(图中省略阴离子配合物中部分原子)。下列关于该阴离子配合物的说法正确的是
 和二脲基分子能通过一种弱相互作用形成超分子阴离子配合物,如下图所示(图中省略阴离子配合物中部分原子)。下列关于该阴离子配合物的说法正确的是
和二脲基分子能通过一种弱相互作用形成超分子阴离子配合物,如下图所示(图中省略阴离子配合物中部分原子)。下列关于该阴离子配合物的说法正确的是
A.二脲基分子中N-H的H和 离子的O形成氢键 离子的O形成氢键 |
| B.所含元素电负性、第一电离能最大的均是N |
| C.二脲基分子中C、N均只有一种杂化方式 |
| D.所含元素的基态原子未成对电子数为2的只有1种 |
您最近一年使用:0次
【推荐1】下列说法错误的是
A.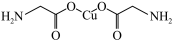 σ键和π键比例为7:1 σ键和π键比例为7:1 |
B.在NH 和[Cu(NH3)4]2+中都存在配位键 和[Cu(NH3)4]2+中都存在配位键 |
C.C 与O 与O 互为等电子体,O 互为等电子体,O 的电子式为 的电子式为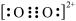 |
| D.已知反应N2O4(l)+2N2H4(l)=3N2(g)+4H2O(l),若该反应中有4molN−H键断裂,则形成的π键数目为3NA |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列对有关事实的解释正确的是( )
| 选项 | 事实 | 解释 |
| A | 乙烯比氮气更易发生加成反应 | 氮元素比碳元素的电负性强 |
| B | HF的酸性比HCl弱 | H-F比H-Cl的键能小 |
| C | 向硫酸铜溶液加入过量氨水最终无沉淀生成 | NH3·H2O为弱碱,溶液中OH-浓度太小 |
| D | 某些金属盐灼烧时呈现不同焰色 | 激发态原子的电子从高能级轨道跃迁至低能级轨道,释放出不同波长的光 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次


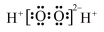
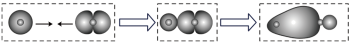
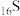 的价层电子排布图:
的价层电子排布图: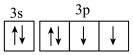
 键的形成:
键的形成: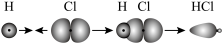
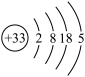
 的VSEPR模型:
的VSEPR模型:

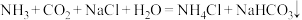 ,下列关于该原理涉及到的物质说法正确的是
,下列关于该原理涉及到的物质说法正确的是 晶体中只存在离子键
晶体中只存在离子键 分子中存在非极性共价键
分子中存在非极性共价键 分子中碳原子采取
分子中碳原子采取 杂化
杂化 分子的空间结构是三角锥形
分子的空间结构是三角锥形 可与某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。
可与某有机多齿配体形成具有较强荧光性能的配合物,其结构如图所示。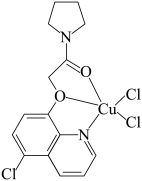
 键
键 的键角比
的键角比 小
小 形成的配位键有3mol
形成的配位键有3mol

