我国秦俑彩绘和汉代器物上用的颜料被称为中国蓝”、“中国紫”,近年来,人们对这些颜料的成分进行了研究,发现其成分主要为BaCuSi4O10、BaCuSi2O6
(1)基态Cu原子核外有_______ 个运动状态不同的电子,其在周期表中的位置_______ 。Si、O、Ba元素电负性由大到小的顺序为_______ 。
(2)“中国蓝”的发色中心是以Cu2+为中心离子的配合物,其中提供孤电子对的是_______ 元素。
(3)比较Si、SiC、 CO2 三种物质晶体状态时熔点由高到低的顺序为_______ ,原因为_______ 。
(4)C、N元素与颜料中的氧元素同周期。
①写出CO的一种常见等电子体分子的电子式_______ ;NO 的VSEPR模型为
的VSEPR模型为_______ ,酸性:HNO2_______ HNO3(填“强于”或“弱于”)。
②C、N元素能形成一种类石墨的聚合物半导体g-C3N4其单层平面结构如图1,晶胞结构如图2。
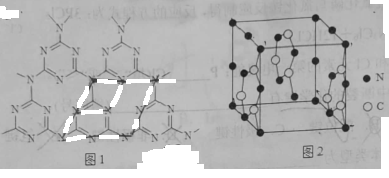
i.g-C3N4中氮原子的杂化类型是_______ 。
ii.已知该晶胞的体积为Vcm3,中间层原子均在晶胞内部。设阿伏加德罗常数的值为NA,则g-C3N4的密度为_______ 。
iii.根据图2,在图1中用平行四边形画出个最小重复单元_____ 。
(1)基态Cu原子核外有
(2)“中国蓝”的发色中心是以Cu2+为中心离子的配合物,其中提供孤电子对的是
(3)比较Si、SiC、 CO2 三种物质晶体状态时熔点由高到低的顺序为
(4)C、N元素与颜料中的氧元素同周期。
①写出CO的一种常见等电子体分子的电子式
 的VSEPR模型为
的VSEPR模型为②C、N元素能形成一种类石墨的聚合物半导体g-C3N4其单层平面结构如图1,晶胞结构如图2。

i.g-C3N4中氮原子的杂化类型是
ii.已知该晶胞的体积为Vcm3,中间层原子均在晶胞内部。设阿伏加德罗常数的值为NA,则g-C3N4的密度为
iii.根据图2,在图1中用平行四边形画出个最小重复单元
更新时间:2021-05-28 14:52:27
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】有A、B、C、D、E、F六种前四周期元素,它们的原子序数依次增大。A、D同主族,A元素的原子最外层p能级的电子数等于次外层的电子总数,C原子最外层中有两个未成对的电子且与A同周期;C元素可分别与A、B、D、E生成RC2型化合物,并知EC2中E与C的质量比为1/1;F能形成红色(或砖红色)和黑色的两种氧化物。根据以上条件,回答下列问题:
(1)请写出F元素的名称___________ F元素电子排布式___________________________
(2)在EC2分子中,E原子的杂化轨道类型为_________ ,分子的空间构型为 _______ ;
(3)H2E和H2C2的主要物理性质比较如下:
H2E和H2C2的相对分子质量基本相同,造成上述几种物理性质差异的主要原因_____________ 。
(4)元素A的一种氢化物是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是( )
A.分子中含有分子间氢键 C.只含有4个sp-s的σ键和1个p-p的π键
B.属于含有极性键的非极性分子 D.该氢化物分子中A原子采用sp2杂化
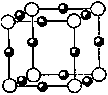
(5)B和F形成某种化合物的晶胞结构如右图所示(每个球均表示1个原子,其中B显-3价),则其化学式为__________ 。F的常见离子和B的最简单氢化物形成的配离子的名称为___________ ,其水溶液颜色为________________ 。
(1)请写出F元素的名称
(2)在EC2分子中,E原子的杂化轨道类型为
(3)H2E和H2C2的主要物理性质比较如下:
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2E | 187 | 202 | 2.6 |
| H2C2 | 272 | 423 | 以任意比互溶 |
H2E和H2C2的相对分子质量基本相同,造成上述几种物理性质差异的主要原因
(4)元素A的一种氢化物是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是
A.分子中含有分子间氢键 C.只含有4个sp-s的σ键和1个p-p的π键
B.属于含有极性键的非极性分子 D.该氢化物分子中A原子采用sp2杂化
(5)B和F形成某种化合物的晶胞结构如右图所示(每个球均表示1个原子,其中B显-3价),则其化学式为

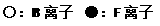
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)酸性强弱比较:苯酚_______ 碳酸(填“>”、“=”或“<”),原因(用相应的离子方程式表示):_______ 。
(2)(CN)2是一种无色气体,有苦杏仁臭味,极毒,请写出该物质的电子式_______ 。
(3)H3BO3具有一元弱酸的性质,在水中可产生正四面体结构的离子,写出电离方程式:_______ 。
(2)(CN)2是一种无色气体,有苦杏仁臭味,极毒,请写出该物质的电子式
(3)H3BO3具有一元弱酸的性质,在水中可产生正四面体结构的离子,写出电离方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硼(B)及其化合物在化学中有重要的地位。请回答下列问题:
(1)Ga与B同主族,Ga的基态原子核外电子排布式为_______ ,第一电离能由大到小的顺序是_______ 。
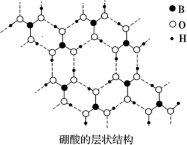
(2)硼酸(H3BO3)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
①硼酸中B原子的杂化轨道类型为_______ 。
②硼酸晶体中存在的作用力有范德华力和_______ 。
③加热时,硼酸的溶解度增大,主要原因是_______ 。
④硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的OH-而呈酸性。写出硼酸的电离方程式:_______ 。
(3)硼氢化钠(NaBH4)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:_______ 。[BH4]-的空间构型是_______ 。
(4)B3N3H6可用来制造具有耐油、耐高温性能的特殊材料。写出它的一种等电子体物质的分子式:_______ 。
(5)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为_______ 。

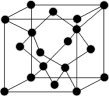
(6)金刚石的晶胞如图。立方氮化硼的结构与金刚石相似,已知晶胞边长为361.5 pm,则立方氮化硼的密度是_______ g· cm-3。(只要求列算式,不必计算出数值,阿伏加德罗常数用NA表示)。
(1)Ga与B同主族,Ga的基态原子核外电子排布式为
(2)硼酸(H3BO3)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。

①硼酸中B原子的杂化轨道类型为
②硼酸晶体中存在的作用力有范德华力和
③加热时,硼酸的溶解度增大,主要原因是
④硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的OH-而呈酸性。写出硼酸的电离方程式:
(3)硼氢化钠(NaBH4)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:
(4)B3N3H6可用来制造具有耐油、耐高温性能的特殊材料。写出它的一种等电子体物质的分子式:
(5)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为

(6)金刚石的晶胞如图。立方氮化硼的结构与金刚石相似,已知晶胞边长为361.5 pm,则立方氮化硼的密度是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】硼是一种重要的非金属元素,在化学中有很重要的地位。
(1)氨硼烷(NH3BH3)是一种具有潜力的固体储氢材料。NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),三种元素电负性由大到小顺序是_______ 。与NH3BH3原子总数相等的等电子体是_______ (写分子式),其熔点比NH3BH3_______ (填“高”或“低”)。
(2)硼酸是一元弱酸,其呈酸性的机理是∶硼酸与水作用时,硼原子与水电离产生的OH-以配位键结合形成Y-,导致溶液中c(H+)>c(OH-)。Y-的结构简式_______ (配位键用“→”表示)。硼酸与水作用时,每生成一个Y-,断裂_______ 个 键。
键。
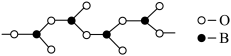
(3)在硼酸盐中,阴离子有链状、环状等多种结构形式。图是一种链状结构的多硼酸根,则多硼酸根离子符号为_______ 。
(1)氨硼烷(NH3BH3)是一种具有潜力的固体储氢材料。NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),三种元素电负性由大到小顺序是
(2)硼酸是一元弱酸,其呈酸性的机理是∶硼酸与水作用时,硼原子与水电离产生的OH-以配位键结合形成Y-,导致溶液中c(H+)>c(OH-)。Y-的结构简式
 键。
键。(3)在硼酸盐中,阴离子有链状、环状等多种结构形式。图是一种链状结构的多硼酸根,则多硼酸根离子符号为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】最近,科学家发现对LiTFSI(一种亲水有机盐,结构如下图所示)进行掺杂和改进,能显著提高锂离子电池传输电荷的能力。
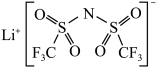
请回答下列问题:
(1)若同学将基态氮原子的电子排布图画为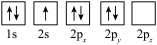 ,该排布图违背的规则有
,该排布图违背的规则有___________ 。
(2)LiTFSI中所含元素中,电负性最大的三种元素电负性由小到大的顺序为___________ (填元素符号,下同);LiTFSI中的第二周期非金属元素第一电离能由小到大的顺序为___________ 。
(3)LiTFSI中存在的化学键有___________ 。
a.离子键 b.极性键 c.金属键 d.氢键
(4)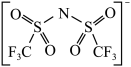 中氮原子的杂化类型为
中氮原子的杂化类型为___________ 。
(5)常见的含硫微粒有: 、
、 、
、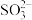 、
、 、
、 等,其中
等,其中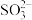 的空间构型为
的空间构型为___________ ; 、
、 中键角较大的是
中键角较大的是___________ 。

请回答下列问题:
(1)若同学将基态氮原子的电子排布图画为
 ,该排布图违背的规则有
,该排布图违背的规则有(2)LiTFSI中所含元素中,电负性最大的三种元素电负性由小到大的顺序为
(3)LiTFSI中存在的化学键有
a.离子键 b.极性键 c.金属键 d.氢键
(4)
 中氮原子的杂化类型为
中氮原子的杂化类型为(5)常见的含硫微粒有:
 、
、 、
、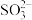 、
、 、
、 等,其中
等,其中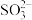 的空间构型为
的空间构型为 、
、 中键角较大的是
中键角较大的是
您最近一年使用:0次
【推荐3】明朝《天工开物》中有世界上最早的“火法”炼锌技术的记载,锌是生命体必需的微量元素,被称为“生命之花”。(已知阿伏加德罗常数的值为NA)
(1)基态Zn原子核外的最高能层符号是_______ ,Zn原子处于_______ 区,基态Zn2+最外层电子排布式为_______ 。
(2)1mol乳酸锌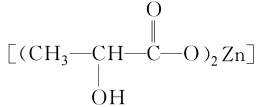 中含有
中含有_______ 个σ键,其中C原子的杂化轨道类型为_______ 杂化。
(3)一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图所示:
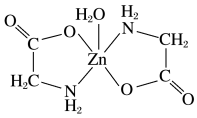
其中所涉及的非金属元素的电负性由大到小的顺序是_______ ,Zn2+的配位数为_______ 。
(4)SO2+与短周期中某元素形成的物质互为等电子体,其中的σ键和π键数目之比为_______ ,SO 离子的立体构型是
离子的立体构型是_______ 。
(1)基态Zn原子核外的最高能层符号是
(2)1mol乳酸锌
 中含有
中含有(3)一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图所示:

其中所涉及的非金属元素的电负性由大到小的顺序是
(4)SO2+与短周期中某元素形成的物质互为等电子体,其中的σ键和π键数目之比为
 离子的立体构型是
离子的立体构型是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
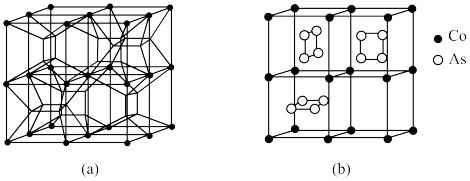
【推荐1】雄黄(As4S4)、雌黄(As2S3)均可入药,具有解毒、杀菌、去燥湿的功效,也是中国画主要的黄色矿物质颜料。回答下列问题:
(1)基态硫原子核外电子的运动轨道数有___________ 种;其核外电子运动最高能级的电子云轮廓图的形状为___________ 。
(2)基态砷原子的价层电子的轨道表示式为___________ 。
(3)S和As比较,电负性较大的是___________ ,其判断理由是___________ 。
(4)元素Mg的第一电离能大于Al的第一电离能的原因是___________ 。
(5)已知高温下CuO→Cu2O+O2,从铜原子价层电子结构(3d和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是___________ 。
(6)CS2分子中,共价键的类型有___________ ,C原子的杂化轨道类型是___________ ,写出两个与CS2具有相同空间构型和键合形式的分子或离子___________ 。
(1)基态硫原子核外电子的运动轨道数有
(2)基态砷原子的价层电子的轨道表示式为
(3)S和As比较,电负性较大的是
(4)元素Mg的第一电离能大于Al的第一电离能的原因是
(5)已知高温下CuO→Cu2O+O2,从铜原子价层电子结构(3d和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是
(6)CS2分子中,共价键的类型有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
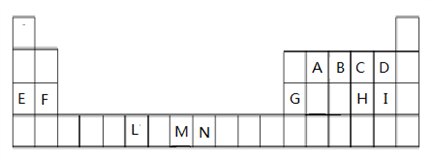
试回答下列问题:
(1)请写出元素M的基态原子的价电子排布式:________________________ 。
(2)标准状况下,11.2L AC2含有π键的数目为______ 。写出AC2的电子式:_________________ 。
(3)E、F、G的第一电离能由大到小的顺序为:____________ 。(填元素符号)
(4)LC2I2常温下为深红色液体,能与 CCl4、CS2 等互溶,据此可判断 LC2I2是________ (填“极性”或“非极性”)分子。
(5)在①苯、②CH3OH、③CS2、④C2H4、⑤CCl4五种物质中,碳原子采取sp2杂化的分子有________ (填序号)。
(6)元素N可以形成分子式为Co(NH3)5BrSO4,配位数均为6的两种配合物,若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为_______________ 。

试回答下列问题:
(1)请写出元素M的基态原子的价电子排布式:
(2)标准状况下,11.2L AC2含有π键的数目为
(3)E、F、G的第一电离能由大到小的顺序为:
(4)LC2I2常温下为深红色液体,能与 CCl4、CS2 等互溶,据此可判断 LC2I2是
(5)在①苯、②CH3OH、③CS2、④C2H4、⑤CCl4五种物质中,碳原子采取sp2杂化的分子有
(6)元素N可以形成分子式为Co(NH3)5BrSO4,配位数均为6的两种配合物,若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】盐酸氯丙嗪是一种多巴胺受体的阻断剂,临床有多种用途。化合物Ⅲ是盐酸氯丙嗪制备的原料,可由化合物I和Ⅱ在铜作催化剂条件下反应制得。

(1) Cu基态核外电子排布式为________________ 。
(2) 1 mol化合物Ⅰ分子中含有σ键数目为________ 。
(3) 化合物Ⅲ分子中sp3方式杂化的原子数目是____________ 。
(4) 向[Cu(NH3)4]SO4溶液中通入SO2至微酸性,有白色沉淀生成。分析表明该白色沉淀中Cu、S、N的物质的量之比为1∶1∶1,沉淀中有一种三角锥形的阴离子和一种正四面体形的阳离子。
①[Cu(NH3)4]SO4中存在的化学键类型有________ (填字母)。
A.共价键 B.氢键 C.离子键 D.配位键 E. 分子间作用力
② 铜的氢化物的晶体结构如图所示,写出该晶体的化学式:____________ 。


(1) Cu基态核外电子排布式为
(2) 1 mol化合物Ⅰ分子中含有σ键数目为
(3) 化合物Ⅲ分子中sp3方式杂化的原子数目是
(4) 向[Cu(NH3)4]SO4溶液中通入SO2至微酸性,有白色沉淀生成。分析表明该白色沉淀中Cu、S、N的物质的量之比为1∶1∶1,沉淀中有一种三角锥形的阴离子和一种正四面体形的阳离子。
①[Cu(NH3)4]SO4中存在的化学键类型有
A.共价键 B.氢键 C.离子键 D.配位键 E. 分子间作用力
② 铜的氢化物的晶体结构如图所示,写出该晶体的化学式:

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】铁原子与氮原子形成的一种晶胞如图所示(白球代表铁原子,黑球代表氮原子),该晶体的化学式为_______ ,已知该晶体的密度为d g· cm-3,正六棱柱底边边长为x cm,NA为阿伏加德罗常数的值,则该正六棱柱的高为_______ cm(用含x、d、NA的代数式表示,列出计算式即可)。


您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】钒(23V)是我国的丰产元素,广泛用于催化及钢铁工业。回答下列问题:
(1)钒在元素周期表中的位置为_____ ,其价层电子排布图为_______ 。
(2)V2O5常用作SO2转化为SO3的催化剂。SO2分子中S原子价层电子对数是_______ 对,分子的立体构型为_______ ;SO3气态为单分子,该分子中S原子的杂化轨道类型为_______ ;SO3的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为_______ ;该结构中S—O键长有两类,一类键长约140pm,另一类键长约160pm,较短的键为_______ (填图中字母),该分子中含有_______ 个σ键。
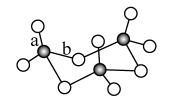
(3)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为_______ ;也可以得到偏钒酸钠,其阴离子呈如图所示的无限链状结构,则偏钒酸钠的化学式为_______ 。
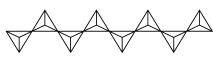
(1)钒在元素周期表中的位置为
(2)V2O5常用作SO2转化为SO3的催化剂。SO2分子中S原子价层电子对数是

(3)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为

您最近一年使用:0次