已知化学反应①:Fe(s)+CO2(g) FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g) FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1 173 K情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1 173 K情况下,K1、K2的值分别如下:
请填空:
(1)通过表格中的数值可以推断:反应①是___________ (填“吸热”或“放热”)反应。
(2)现有反应③:CO2(g)+H2(g) CO(g)+H2O(g),写出该反应的平衡常数K3的表达式:K3=
CO(g)+H2O(g),写出该反应的平衡常数K3的表达式:K3=___________ 。
(3)根据反应①与②可推导出K1、K2与K3之间的关系式___________ ,据此关系式及上表数据,也能推断出反应③是___________ (填“吸热”或“放热”)反应。
(4)图甲、图乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:

①图甲t2时刻改变的条件是___________ 。
②图乙t2时刻改变的条件是___________ 。
 FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g) FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1 173 K情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1 173 K情况下,K1、K2的值分别如下:| 温度 | K1 | K2 |
| 973 K | 1.47 | 2.38 |
| 1 173 K | 2.15 | 1.67 |
(1)通过表格中的数值可以推断:反应①是
(2)现有反应③:CO2(g)+H2(g)
 CO(g)+H2O(g),写出该反应的平衡常数K3的表达式:K3=
CO(g)+H2O(g),写出该反应的平衡常数K3的表达式:K3=(3)根据反应①与②可推导出K1、K2与K3之间的关系式
(4)图甲、图乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:

①图甲t2时刻改变的条件是
②图乙t2时刻改变的条件是
20-21高二下·山东淄博·期中 查看更多[2]
更新时间:2021-05-13 13:27:27
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO 2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1) 已知该反应ΔS<0,在上述条件下反应能够自发进行,则反应的ΔH________ 0(填写“>”“<”或“=”)。
(2)前2 s内的平均反应速率v(N2)=________ 。
(3)在该温度下,反应的平衡常数表达式K=________ 。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是________ 。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
 2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(10-4mol·L-1) | 10 | 4.5 | 2.5 | 1.5 | 1.0 | 1.0 |
| c(CO)/(10-3mol·L-1) | 36.0 | 30.5 | 28.5 | 27.5 | 27.0 | 27.0 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1) 已知该反应ΔS<0,在上述条件下反应能够自发进行,则反应的ΔH
(2)前2 s内的平均反应速率v(N2)=
(3)在该温度下,反应的平衡常数表达式K=
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】一定条件下,体积为1L的密闭容器中存在如下反应:
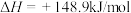 。
。
(1)下列各项中能说明该反应已达化学平衡状态的是_______ (填序号)。
a.v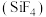 消耗=v
消耗=v 生成 b.容器内气体压强不再变化
生成 b.容器内气体压强不再变化
c.容器内气体的总质量不再变化 d.容器内HF体积分数不再变化
(2)反应过程中测定的部分数据如下表(表中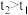 ):
):
通过计算a或b的值判断t1时刻反应是否达到化学平衡状态:_______ 。
(3)若只改变一个条件使上述反应的化学平衡常数变大,该反应_______ (填序号)。
a.一定向正反应方向移动 b.一定是增大压强造成的
c.一定是升高温度造成的 d.SiF4的平衡转化率一定增大
(4)反应进行到2min时,容器内气体的密度减小了0.03g/L,则这2min内: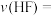
_______ 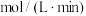 。
。

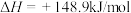 。
。(1)下列各项中能说明该反应已达化学平衡状态的是
a.v
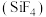 消耗=v
消耗=v 生成 b.容器内气体压强不再变化
生成 b.容器内气体压强不再变化c.容器内气体的总质量不再变化 d.容器内HF体积分数不再变化
(2)反应过程中测定的部分数据如下表(表中
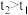 ):
):| 反应时间/min | n(SiF4)/mol | n(H2O)/mol |
| 0 | 1.20 | 2.40 |
| t1 | 0.80 | a |
| t2 | b | 1.60 |
(3)若只改变一个条件使上述反应的化学平衡常数变大,该反应
a.一定向正反应方向移动 b.一定是增大压强造成的
c.一定是升高温度造成的 d.SiF4的平衡转化率一定增大
(4)反应进行到2min时,容器内气体的密度减小了0.03g/L,则这2min内:
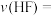
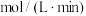 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】已知:H2S(g) H2(g)+
H2(g)+ S2(g),在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为cmol/L,测定H2S的转化率,H2S的平衡转化率与温度关系如图所示。据图可知:温度升高平衡常数K
S2(g),在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为cmol/L,测定H2S的转化率,H2S的平衡转化率与温度关系如图所示。据图可知:温度升高平衡常数K_______ (填“增大”、“减小”或“不变”)。若985℃时平衡常数K=0.04,则起始浓度c=______ 。

 H2(g)+
H2(g)+ S2(g),在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为cmol/L,测定H2S的转化率,H2S的平衡转化率与温度关系如图所示。据图可知:温度升高平衡常数K
S2(g),在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为cmol/L,测定H2S的转化率,H2S的平衡转化率与温度关系如图所示。据图可知:温度升高平衡常数K
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在某2L的密闭容器中加入0.1mol碘单质和足量钨(W),在943K时,发生反应W(s)+I2(g)⇌WI2(g),当I2的转化率为20%时,达化学平衡状态;
(1)反应从开始至平衡状态过程中用时20s,其平均反应速率v(WI2)为_________________ ;
(2)943K时,该反应的平衡常数K=_______________ ;
(3)若起始时,加入的碘为0.2mol(其他条件不变)达平衡时容器中气体的体积比V(I2):V(WI2)=____________ ;
(4)在上述(1)平衡状态下,同时增加I2(g)和WI2(g)各0.02mol(其他条件不变),化学平衡向____________ (填“正反应”或“逆反应”)方向移动,判断的依据是____________ 。
(1)反应从开始至平衡状态过程中用时20s,其平均反应速率v(WI2)为
(2)943K时,该反应的平衡常数K=
(3)若起始时,加入的碘为0.2mol(其他条件不变)达平衡时容器中气体的体积比V(I2):V(WI2)=
(4)在上述(1)平衡状态下,同时增加I2(g)和WI2(g)各0.02mol(其他条件不变),化学平衡向
您最近一年使用:0次
填空题
|
较易
(0.85)
真题
名校
【推荐3】反应A(g) B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:

(1)上述反应的温度T1___ T2,平衡常数K(T1)___ K(T2)。(填“大于”、“小于” 或“等于”)
(2)若温度T2时,5min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为_______ 。
②反应的平衡常数K=______ 。
③反应在0~5min区间的平均反应速率v(A)=_______ 。
 B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
(1)上述反应的温度T1
(2)若温度T2时,5min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为
②反应的平衡常数K=
③反应在0~5min区间的平均反应速率v(A)=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】一定条件下2L的密闭容器中,反应aA(g)+bB(g) cC(g)+dD(g)达到平衡。
cC(g)+dD(g)达到平衡。
(1)若起始时A为lmol,反应2min达到平衡,A剩余0.4mol,则在0~2min内A的平均反应速率为________ mol/(L·min)
(2)在其他条件不变的情况下,扩大容器体积,若平衡向逆反应方向移动,则a+b_____ c+d(选填“>”、“<”或“=”),v逆_____ (选填“增大”、“减小”或“不变”)
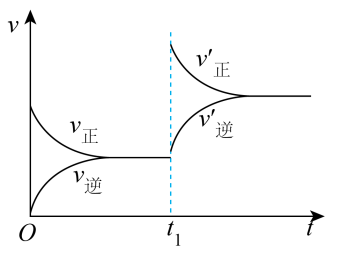
(3)若反应速率(v)与时间(t)的关系如图所示,则导致t1时刻速率发生变化的原因可能是______ 。(选填编号)
a.增大A的浓度
b.缩小容器体积
c.加入催化剂
d.升高温度
 cC(g)+dD(g)达到平衡。
cC(g)+dD(g)达到平衡。(1)若起始时A为lmol,反应2min达到平衡,A剩余0.4mol,则在0~2min内A的平均反应速率为
(2)在其他条件不变的情况下,扩大容器体积,若平衡向逆反应方向移动,则a+b
(3)若反应速率(v)与时间(t)的关系如图所示,则导致t1时刻速率发生变化的原因可能是

a.增大A的浓度
b.缩小容器体积
c.加入催化剂
d.升高温度
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】在一密闭容器中发生反应N2+3H2=2NH3 ΔH<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示。
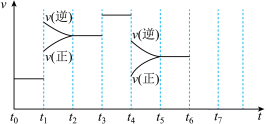
回答下列问题:
(1)处于平衡状态的时间段是___________ (填字母,下同)。
A.t0~t1 B.t1~t2 C.t2~t3
D.t3~t4 E.t4~t5 F.t5~t6
(2)判断t1、t3、t4时刻分别改变的一个条件。
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
t1时刻___________ ;t3时刻___________ ;t4时刻___________ 。
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是___________ 。
A.t0~t1 B.t2~t3
C.t3~t4 D.t5~t6
(4)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图中画出反应速率的变化曲线______ 。

回答下列问题:
(1)处于平衡状态的时间段是
A.t0~t1 B.t1~t2 C.t2~t3
D.t3~t4 E.t4~t5 F.t5~t6
(2)判断t1、t3、t4时刻分别改变的一个条件。
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
t1时刻
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是
A.t0~t1 B.t2~t3
C.t3~t4 D.t5~t6
(4)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图中画出反应速率的变化曲线
您最近一年使用:0次

 3C(气),下图中甲、乙、丙分别表示在不同的条件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:
3C(气),下图中甲、乙、丙分别表示在不同的条件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:


