高炉炼铁中发生的反应有:FeO(s) + CO(g)=Fe(s) + CO2(g) △H < 0
(1)该反应的平衡常数表达式K=_______ 。
(2)已知1100℃时,K=0.263温度升高,平衡常数K_______ (增大,减少或不变)。
(3)1100℃时,测得高炉中c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下该反应是否处于平衡状态_______ (填是或否),此时反应速率是v正_______ v逆(填>,<,=)。
(1)该反应的平衡常数表达式K=
(2)已知1100℃时,K=0.263温度升高,平衡常数K
(3)1100℃时,测得高炉中c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下该反应是否处于平衡状态
更新时间:2022-01-08 07:32:28
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】钒是重要的战略资源,以硫酸工业产生的废钒催化剂为原料(含 、
、 、
、 、
、 以及少量的
以及少量的 等),综合回收利用钒、硅、钾实现变废为宝、保护环境的目的,回收工艺流程如下:
等),综合回收利用钒、硅、钾实现变废为宝、保护环境的目的,回收工艺流程如下: 、
、 存在,
存在, 增大时
增大时 可转化为
可转化为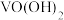 沉淀。
沉淀。
“萃取”时选择有机萃取剂,原理是: (有机层)
(有机层)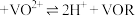 (有机层),“反萃取”应选择在
(有机层),“反萃取”应选择在___________ 环境中进行(选填“酸性”、“中性”或“碱性”)。
 、
、 、
、 、
、 以及少量的
以及少量的 等),综合回收利用钒、硅、钾实现变废为宝、保护环境的目的,回收工艺流程如下:
等),综合回收利用钒、硅、钾实现变废为宝、保护环境的目的,回收工艺流程如下: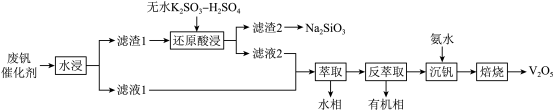
 、
、 存在,
存在, 增大时
增大时 可转化为
可转化为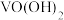 沉淀。
沉淀。“萃取”时选择有机萃取剂,原理是:
 (有机层)
(有机层)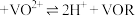 (有机层),“反萃取”应选择在
(有机层),“反萃取”应选择在
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】 和
和 在水溶液中的反应为
在水溶液中的反应为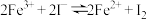 。
。
(1)该反应的平衡常数K的表达式为_______ 。当上述反应达到平衡后,保持其他条件不变,加入 萃取溶液中的
萃取溶液中的 ,上述平衡如何移动?
,上述平衡如何移动?______
(2)请设计一种能使平衡向逆反应方向移动的方案。______
 和
和 在水溶液中的反应为
在水溶液中的反应为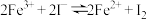 。
。(1)该反应的平衡常数K的表达式为
 萃取溶液中的
萃取溶液中的 ,上述平衡如何移动?
,上述平衡如何移动?(2)请设计一种能使平衡向逆反应方向移动的方案。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】工业上合成氨的化学反应,在容积为10L的密闭容器中,通入40molN2和120mol H2在一定条件下进行反应,4s后达到平衡状态,此时N2的浓度为2mol/L。通过计算回答下列问题:
(1)用N2 表示的4s内化学反应的平均速率是________ 。
(2)若生成17g氨气,放出46.2kJ热量,写出合成生成2摩尔氨反应的热化学方程式________ 。
(3)以上化学反应平衡常数的表达式为____ ,若外界条件改变为升高温度,平衡常数将____ (填“增大、减小、不变”)
(4)上述反应达到平衡后,在其它条件不变的情况下,通过减小容器体积增大压强,则化学平衡向_____ 移动的是(填“正向”或“逆向”)。
(1)用N2 表示的4s内化学反应的平均速率是
(2)若生成17g氨气,放出46.2kJ热量,写出合成生成2摩尔氨反应的热化学方程式
(3)以上化学反应平衡常数的表达式为
(4)上述反应达到平衡后,在其它条件不变的情况下,通过减小容器体积增大压强,则化学平衡向
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题
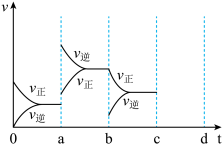
(1)如图表示在密闭容器中反应:2SO2+O2 2SO3 ∆H<0达到平衡时,如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为
2SO3 ∆H<0达到平衡时,如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为_______ ,由于条件改变而引起反应速度和化学平衡的变化情况,a-b过程中改变的条件可能是_______ ;b-c过程中改变的条件可能是_______ ;若增大压强时,反应速度变化情况画在c-d处_____ 。
(2)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
回答下列问题:
①该反应的化学平衡常数表达式为K=_______ ;
②该反应为_______ 反应(选填吸热、放热)
③能判断该反应是否达到化学平衡状态的依据是_______ (多选扣分)
a.容器中压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
④某温度下平衡浓度符合下式:c(CO2)·c(H2)=(CO)·c(H2O),试判断此时的温度为_______ ℃。
(1)如图表示在密闭容器中反应:2SO2+O2
 2SO3 ∆H<0达到平衡时,如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为
2SO3 ∆H<0达到平衡时,如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为
(2)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:| t°C | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
①该反应的化学平衡常数表达式为K=
②该反应为
③能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
④某温度下平衡浓度符合下式:c(CO2)·c(H2)=(CO)·c(H2O),试判断此时的温度为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】正误判断
1.在FeCl3+3KSCN⇌Fe(SCN)3+3KCl平衡体系中,加入KCl固体,颜色变浅。________
2.由温度或压强改变引起的平衡正向移动,反应物的转化率一定增大。________
3.对于反应N2(g)+3H2(g)⇌2NH3(g) △H<0,其他条件不变时,升高温度,v(H2)和α(H2)均增大。________
4.对于反应C(s)+H2O(g)⇌CO(g)+H2(g),其平衡常数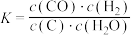 。
。________
5.H2(g)+I2(g)⇌2HI(g)的平衡常数为K1,1/2H2(g)+1/2I2(g)⇌HI(g)的平衡常数为K2,则K1×K2=1。________
1.在FeCl3+3KSCN⇌Fe(SCN)3+3KCl平衡体系中,加入KCl固体,颜色变浅。
2.由温度或压强改变引起的平衡正向移动,反应物的转化率一定增大。
3.对于反应N2(g)+3H2(g)⇌2NH3(g) △H<0,其他条件不变时,升高温度,v(H2)和α(H2)均增大。
4.对于反应C(s)+H2O(g)⇌CO(g)+H2(g),其平衡常数
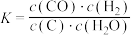 。
。5.H2(g)+I2(g)⇌2HI(g)的平衡常数为K1,1/2H2(g)+1/2I2(g)⇌HI(g)的平衡常数为K2,则K1×K2=1。
您最近一年使用:0次
【推荐1】甲醇是一种重要的化工原料又是一种可再生能源,具有开发和应用的广阔前景。
(1)在一容积为2 L的密闭容器内,充入0.2 mol CO与0.4 mol H2发生反应,CO(g)+2H2(g) CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
①A、B两点对应的压强大小关系是PA_______ PB(填“>、<、=”)。
②在压强为P2时B、C两点的正反应速率大小关系是______________
③下列叙述能说明上述反应已达到化学平衡状态的是__________
A.H2的消耗速率是CH3OH生成速率的2倍 B.CH3OH的体积分数不再改变
C.混合气体的密度不再改变 D.CO和CH3OH的物质的量之比保持不变
(2)在压强为P1、温度为T1℃时,H2的平衡转化率为__________ (计算出结果),再加入1.0 mol CO后重新到达平衡,则CO的转化率___________ (填“增大”、“不变”或“减小”)。
(3) 在压强为P1、温度为T1℃时,1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.05 mol、H2:0.1mol、CH3OH:0.05mol。此时v(正)________ v(逆)(填“>”、“<”或“=”)。
(1)在一容积为2 L的密闭容器内,充入0.2 mol CO与0.4 mol H2发生反应,CO(g)+2H2(g)
 CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。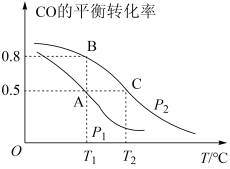
①A、B两点对应的压强大小关系是PA
②在压强为P2时B、C两点的正反应速率大小关系是
③下列叙述能说明上述反应已达到化学平衡状态的是
A.H2的消耗速率是CH3OH生成速率的2倍 B.CH3OH的体积分数不再改变
C.混合气体的密度不再改变 D.CO和CH3OH的物质的量之比保持不变
(2)在压强为P1、温度为T1℃时,H2的平衡转化率为
(3) 在压强为P1、温度为T1℃时,1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.05 mol、H2:0.1mol、CH3OH:0.05mol。此时v(正)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】I.CH4、CO2都是碳的重要化合物,实现碳及其化合物的相互转化,对开发新能源和降低碳排放意义重大。
(1)在一定条件下,可通过CH4与NOx反应除去NOx,已知有下列热化学方程式:
①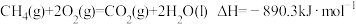
②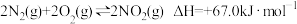
③
则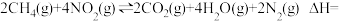
___________  ;
;
(2)(在一恒容装置中,通入一定量CH4和NO2,测得在相同时间内,在不同温度下,NO2的转化率如图(横坐标为反应温度,纵坐标为NO2转化率/%):
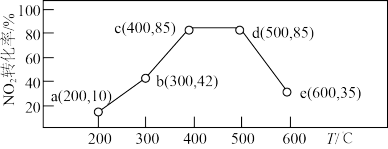
则下列叙述正确的是___________。
(3)在一定条件下,二氧化碳转化为甲烷的反应如下: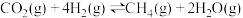 ;向一容积为2L的恒容密闭容器中充入2molCO2和8molH2,在300℃时发生上述反应,达到平衡时H2的浓度为
;向一容积为2L的恒容密闭容器中充入2molCO2和8molH2,在300℃时发生上述反应,达到平衡时H2的浓度为 。则300℃时上述反应的平衡常数K=
。则300℃时上述反应的平衡常数K=___________ 。200℃时该反应的平衡常数K=64.8,则该反应的
___________ (填“>”或“<”)0。
II.已知可逆反应 的正、逆反应均为一级反应,v正=k正•c(A),v逆=k逆•c(B)且存在如下数据:
的正、逆反应均为一级反应,v正=k正•c(A),v逆=k逆•c(B)且存在如下数据:
(4)600K时,在容积为1L的恒容密闭容器中充入2mol气体A,已知反应过程中物质的浓度、速率常数和反应时间之间满足如下关系: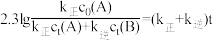 ,[c0(A)为反应物A的起始浓度,ct(A)、ct(B)分别为A,B任意时刻的浓度,k为反应速率常数,t为反应时间],则:
,[c0(A)为反应物A的起始浓度,ct(A)、ct(B)分别为A,B任意时刻的浓度,k为反应速率常数,t为反应时间],则:
①t=___________ min时反应达平衡。
②反应一段时间后A,B浓度相等,则这段时间内正反应的平均反应速率v=___________ mol(L∙min)(保留整数)。(已知lg2=0.3,lg5=0.7)
(1)在一定条件下,可通过CH4与NOx反应除去NOx,已知有下列热化学方程式:
①
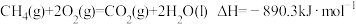
②
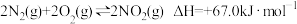
③

则
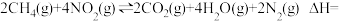
 ;
;(2)(在一恒容装置中,通入一定量CH4和NO2,测得在相同时间内,在不同温度下,NO2的转化率如图(横坐标为反应温度,纵坐标为NO2转化率/%):

则下列叙述正确的是___________。
| A.若温度维持在200℃更长时间,NO2的转化率将大于19% |
| B.反应速率:b点的v(逆)>e点的v(逆) |
| C.平衡常数:c点=d点 |
| D.提高c点时NO2的转化率和反应速率,可减小压强或增大c(CH4) |
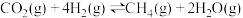 ;向一容积为2L的恒容密闭容器中充入2molCO2和8molH2,在300℃时发生上述反应,达到平衡时H2的浓度为
;向一容积为2L的恒容密闭容器中充入2molCO2和8molH2,在300℃时发生上述反应,达到平衡时H2的浓度为 。则300℃时上述反应的平衡常数K=
。则300℃时上述反应的平衡常数K=
II.已知可逆反应
 的正、逆反应均为一级反应,v正=k正•c(A),v逆=k逆•c(B)且存在如下数据:
的正、逆反应均为一级反应,v正=k正•c(A),v逆=k逆•c(B)且存在如下数据:| 温度(K) | 600 | 850 | |
| 速率 常数 | k正(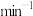 ) ) | 32 | 70 |
k逆(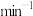 ) ) | 8 | 12 | |
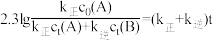 ,[c0(A)为反应物A的起始浓度,ct(A)、ct(B)分别为A,B任意时刻的浓度,k为反应速率常数,t为反应时间],则:
,[c0(A)为反应物A的起始浓度,ct(A)、ct(B)分别为A,B任意时刻的浓度,k为反应速率常数,t为反应时间],则:①t=
②反应一段时间后A,B浓度相等,则这段时间内正反应的平均反应速率v=
您最近一年使用:0次

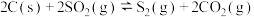 反应过程中,各物质浓度与时间的关系如图:
反应过程中,各物质浓度与时间的关系如图: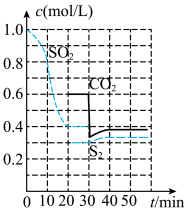

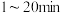 化学反应速率表示
化学反应速率表示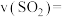
 时改变外界条件,使
时改变外界条件,使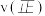
 (选填“大于”、“小于”或“等于”)。
(选填“大于”、“小于”或“等于”)。
 的平衡常数
的平衡常数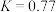 。当
。当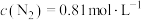 ,
,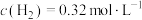 ,
, 时,试通过计算判断反应进行的方向。
时,试通过计算判断反应进行的方向。

