以镍废渣(主要成分为Ni,含少量Fe、Al、Fe3O4、Al2O3和不溶性杂质等)为原料获得碳酸镍流程如图:回答下列问题:[溶液中某离子浓度c(X)T≤10-5 mol·L-1时,即视为沉淀完全] 。
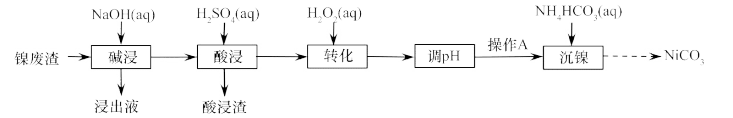
(1)“碱浸”时加入NaOH溶液的作用是___________ 。
(2)“酸浸”滤液中含有的阳离子主要为H+、___________ 。
(3)“转化”时加入H2O2的目的是___________ (用离子方程式表示),该过程温度不宜过高,原因可能是___________ 。
(4)请写出“沉镍”时的离子方程式___________ 。
(5)若选用Na2CO3溶液“沉镍”,当溶液中碳总浓度[ c(C)]为0.1 mol·L-1时,溶液中镍总浓度的对数[lgc(Ni)]与溶液pH关系如图。注:c(C)=c( )+c(
)+c( )+c(H2CO3)
)+c(H2CO3)

①a点(pH≈8.2)时溶液中析出的沉淀主要为___________ (填化学式)。
②b点溶液中Ni2+是否沉淀完全___________ (填“是”或“否”)
(6)取“操作A”所得的NiSO4溶液VmL,用c mol·L-1 EDTA(Na2H2Y)的标准溶液滴定至终点(发生反应Ni2++H2Y2-=NiY2-+2H+),消耗标准液20.00 mL,则“沉镍”过程中,当NiCO3开始沉淀时,溶液中 浓度为
浓度为___________ 。[已知常温下,Ksp(NiCO3)=1.42×10-7,只列计算式,不考虑杂质反应]。
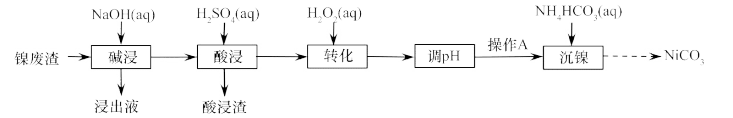
(1)“碱浸”时加入NaOH溶液的作用是
(2)“酸浸”滤液中含有的阳离子主要为H+、
(3)“转化”时加入H2O2的目的是
(4)请写出“沉镍”时的离子方程式
(5)若选用Na2CO3溶液“沉镍”,当溶液中碳总浓度[ c(C)]为0.1 mol·L-1时,溶液中镍总浓度的对数[lgc(Ni)]与溶液pH关系如图。注:c(C)=c(
 )+c(
)+c( )+c(H2CO3)
)+c(H2CO3)
①a点(pH≈8.2)时溶液中析出的沉淀主要为
②b点溶液中Ni2+是否沉淀完全
(6)取“操作A”所得的NiSO4溶液VmL,用c mol·L-1 EDTA(Na2H2Y)的标准溶液滴定至终点(发生反应Ni2++H2Y2-=NiY2-+2H+),消耗标准液20.00 mL,则“沉镍”过程中,当NiCO3开始沉淀时,溶液中
 浓度为
浓度为
更新时间:2021-05-14 08:58:23
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】在生活中亚硝酸钠( )应用十分广泛,它是一种白色固体,外观与NaCl极其相似。少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长;还可用于治疗氰化物中毒等。
)应用十分广泛,它是一种白色固体,外观与NaCl极其相似。少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长;还可用于治疗氰化物中毒等。
(1)人体正常的血红蛋白含有 ,若误食亚硝酸钠会把
,若误食亚硝酸钠会把 转换为
转换为 而中毒,应立即注射美蓝溶液进行治疗。上述过程中,亚硝酸钠作
而中毒,应立即注射美蓝溶液进行治疗。上述过程中,亚硝酸钠作_______ (填“氧化”或“还原”下同)剂,美蓝溶液被_______ 。
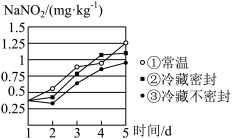
(2)某腌制品中亚硝酸钠含量随时间变化如图所示,若要保证在亚硝酸钠含量低于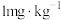 时食用,则三种条件下保存时间最长的是
时食用,则三种条件下保存时间最长的是_______ (填序号)。
(3)某化学兴趣小组查阅资料得知 ,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)
,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)
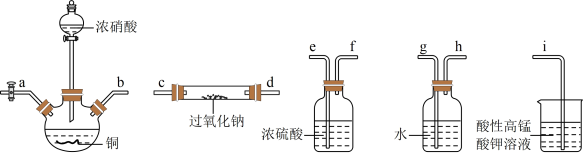
已知: 易被空气氧化,NO能被酸性高锰酸钾溶液氧化为
易被空气氧化,NO能被酸性高锰酸钾溶液氧化为 ,但不能被浓硫酸氧化;酸性高锰酸钾溶液可将
,但不能被浓硫酸氧化;酸性高锰酸钾溶液可将 氧化成
氧化成
①盛装浓硝酸的仪器名称为_______ ,仪器按气流方向连接顺序为b→g_______ (装置可重复使用)。
②反应开始前打开止水夹a,通入过量氮气的目的是排除装置中的空气,若不排除装置中的空气,可能产生的后果是_______ ;反应结束后打开止水夹a,通入过量氮气的目的是_______ 。
③盛水的洗气瓶的作用是_______ 。
④判断 已被NO反应完全的现象是
已被NO反应完全的现象是_______ 。
(4)某工厂以硝酸为原料生产亚硝酸钠,其工艺流程如下:
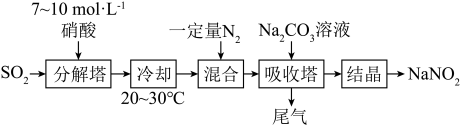
已知: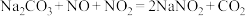 。按一定计量比在“分解塔”中通
。按一定计量比在“分解塔”中通 和喷入硝酸,若反应后生成的NO与
和喷入硝酸,若反应后生成的NO与 的物质的量之比恰好为1:1,则“分解塔”中发生反应的化学方程式:
的物质的量之比恰好为1:1,则“分解塔”中发生反应的化学方程式:_______ 。
 )应用十分广泛,它是一种白色固体,外观与NaCl极其相似。少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长;还可用于治疗氰化物中毒等。
)应用十分广泛,它是一种白色固体,外观与NaCl极其相似。少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长;还可用于治疗氰化物中毒等。(1)人体正常的血红蛋白含有
 ,若误食亚硝酸钠会把
,若误食亚硝酸钠会把 转换为
转换为 而中毒,应立即注射美蓝溶液进行治疗。上述过程中,亚硝酸钠作
而中毒,应立即注射美蓝溶液进行治疗。上述过程中,亚硝酸钠作(2)某腌制品中亚硝酸钠含量随时间变化如图所示,若要保证在亚硝酸钠含量低于
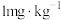 时食用,则三种条件下保存时间最长的是
时食用,则三种条件下保存时间最长的是
(3)某化学兴趣小组查阅资料得知
 ,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)
,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)
已知:
 易被空气氧化,NO能被酸性高锰酸钾溶液氧化为
易被空气氧化,NO能被酸性高锰酸钾溶液氧化为 ,但不能被浓硫酸氧化;酸性高锰酸钾溶液可将
,但不能被浓硫酸氧化;酸性高锰酸钾溶液可将 氧化成
氧化成
①盛装浓硝酸的仪器名称为
②反应开始前打开止水夹a,通入过量氮气的目的是排除装置中的空气,若不排除装置中的空气,可能产生的后果是
③盛水的洗气瓶的作用是
④判断
 已被NO反应完全的现象是
已被NO反应完全的现象是(4)某工厂以硝酸为原料生产亚硝酸钠,其工艺流程如下:

已知:
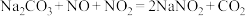 。按一定计量比在“分解塔”中通
。按一定计量比在“分解塔”中通 和喷入硝酸,若反应后生成的NO与
和喷入硝酸,若反应后生成的NO与 的物质的量之比恰好为1:1,则“分解塔”中发生反应的化学方程式:
的物质的量之比恰好为1:1,则“分解塔”中发生反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】高中化学课本必修一中出现的部分物质间的转化关系如图所示(部分物质已省略。已知 是实验室制取氯气的主要方法之一,H的焰色试验呈黄色),请完成下列填空。
是实验室制取氯气的主要方法之一,H的焰色试验呈黄色),请完成下列填空。
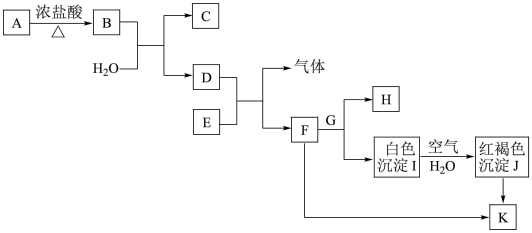
(1)H的化学式为:______________ 。
(2)若K中含有F的杂质,应加入_______ (填化学式)除杂。
(3)I转化为J的化学方程式为___________________________ 。
(4)K的饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是_____(填字母序号)。
(5)将B通入G溶液中可得到一种漂白液,能杀菌、消毒,该漂白液的有效成分是_______ (填化学式)。
(6) 为公认的高效安全灭菌消毒剂之一,常温下亚氯酸钠
为公认的高效安全灭菌消毒剂之一,常温下亚氯酸钠 固体与B反应可得到
固体与B反应可得到 和NaCl,该反应中的离子方程式为
和NaCl,该反应中的离子方程式为______________
(7)能将KI氧化为 的氧化剂有
的氧化剂有 、
、 、
、 、
、 、
、 、
、 等。
等。
已知下列四种氧化剂氧化KI后对应的还原产物如下:
判断等物质的量的四种氧化剂分别与足量KI作用,得到 最多的是
最多的是______________
 是实验室制取氯气的主要方法之一,H的焰色试验呈黄色),请完成下列填空。
是实验室制取氯气的主要方法之一,H的焰色试验呈黄色),请完成下列填空。
(1)H的化学式为:
(2)若K中含有F的杂质,应加入
(3)I转化为J的化学方程式为
(4)K的饱和溶液滴入沸水中,可得到胶体L。胶体L区别于K的饱和溶液最本质的特征是_____(填字母序号)。
A.胶体L的分散质粒子直径为 | B.胶体L具有丁达尔效应 |
| C.胶体L是均一的分散系 | D.胶体L比K的饱和溶液颜色深 |
(6)
 为公认的高效安全灭菌消毒剂之一,常温下亚氯酸钠
为公认的高效安全灭菌消毒剂之一,常温下亚氯酸钠 固体与B反应可得到
固体与B反应可得到 和NaCl,该反应中的离子方程式为
和NaCl,该反应中的离子方程式为(7)能将KI氧化为
 的氧化剂有
的氧化剂有 、
、 、
、 、
、 、
、 、
、 等。
等。已知下列四种氧化剂氧化KI后对应的还原产物如下:
氧化剂 |
|
|
|
|
还原产物 |
|
|
| NO |
 最多的是
最多的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】依据图中氮元素及其化合物的转化关系,回答问题:
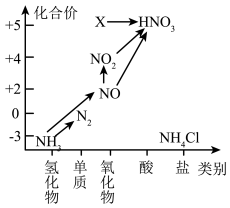
(1)图中X的化学式为_______ 。
(2)实验室常用NH4C1与Ca(OH)2制取氨气,该反应的化学方程式为_______ 。
(3)实验室收集NH3方法_______ 。
A.向上排空法 B.向下排空法 C.排水法
(4)如何检验NH4Cl溶液中阳离子_______ 。
(5)写出NH3 → NO的化学方程式:_______ 。
(6)久置浓硝酸呈黄色的原因是_______ ,(用化学方程式解释)。
(7)预测N2O可能有_______ 性质。
A.仅有还原性
B.仅有氧化性
C.既有氧化性又有还原性

(1)图中X的化学式为
(2)实验室常用NH4C1与Ca(OH)2制取氨气,该反应的化学方程式为
(3)实验室收集NH3方法
A.向上排空法 B.向下排空法 C.排水法
(4)如何检验NH4Cl溶液中阳离子
(5)写出NH3 → NO的化学方程式:
(6)久置浓硝酸呈黄色的原因是
(7)预测N2O可能有
A.仅有还原性
B.仅有氧化性
C.既有氧化性又有还原性
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】KMnO4是一种常用的氧化剂。某实验小组利用氯气氧化K2MnO4制备KMnO4并对其性质进行探究。
资料:①锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3 +2H2O=2
+2H2O=2 +MnO2↓+4OH-
+MnO2↓+4OH-
②酸性条件下的氧化性:KMnO4>KIO3>I2
I.KMnO4的制备
(1)从A—D中选择合适的装置制备KMnO4,正确的连接顺序是a→___________ (按气流方向,用小写字母表示)。
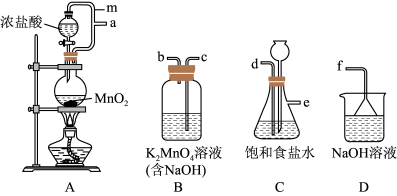
(2)若没有使用装置C,造成的影响是___________ 。
Ⅱ.KMnO4性质探究
取适量制取的KMnO4溶液稀释至约0.01mol·L-1(用硫酸酸化至pH=1),取配制好的KMnO4溶液2mL于试管中,逐滴滴加0.1mol·L-1KI溶液,KMnO4紫色溶液迅速变为棕褐色悬浊液,然后沉淀逐渐消失,最终溶液变为棕黄色。
(3)最终溶液呈现棕黄色推测生成了___________ (写化学式)。
(4)实验小组对初始阶段的产物成分进行探究:

①黑色固体是MnO2,试剂X是___________ (写化学式)。
②在“紫色清液”中存在 ,写出生成
,写出生成 的离子方程式:
的离子方程式:___________ 。
③下列实验方案中,可用于检验“紫色清液”中是否存在 的是
的是___________ (填字母)。
A.用洁净的玻璃棒蘸取紫色清液滴在淀粉-KI试纸上,观察试纸是否变蓝色。
B.取少量紫色清液于试管中,向其中加入几滴淀粉溶液,溶液不变蓝,再加入过量NaHSO3溶液,观察溶液是否变色。
C.取少量紫色清液于试管中,向其中加入稀硝酸酸化,再加入几滴硝酸银溶液,观察是否生成黄色沉淀。
Ⅲ.KMnO4的应用
(5)采用KMnO4滴定法测定某FeC2O4·2H2O样品(杂质不参与反应)的纯度,实验步骤:取mg样品于锥形瓶中,加入稀H2SO4溶解。用cmol﹒L-1的KMnO4溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗KMnO4溶液VmL。样品中所含的FeC2O4·2H2O(M=180g·mol-1)质量分数表达式为_______ 。
资料:①锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3
 +2H2O=2
+2H2O=2 +MnO2↓+4OH-
+MnO2↓+4OH-②酸性条件下的氧化性:KMnO4>KIO3>I2
I.KMnO4的制备
(1)从A—D中选择合适的装置制备KMnO4,正确的连接顺序是a→

(2)若没有使用装置C,造成的影响是
Ⅱ.KMnO4性质探究
取适量制取的KMnO4溶液稀释至约0.01mol·L-1(用硫酸酸化至pH=1),取配制好的KMnO4溶液2mL于试管中,逐滴滴加0.1mol·L-1KI溶液,KMnO4紫色溶液迅速变为棕褐色悬浊液,然后沉淀逐渐消失,最终溶液变为棕黄色。
(3)最终溶液呈现棕黄色推测生成了
(4)实验小组对初始阶段的产物成分进行探究:

①黑色固体是MnO2,试剂X是
②在“紫色清液”中存在
 ,写出生成
,写出生成 的离子方程式:
的离子方程式:③下列实验方案中,可用于检验“紫色清液”中是否存在
 的是
的是A.用洁净的玻璃棒蘸取紫色清液滴在淀粉-KI试纸上,观察试纸是否变蓝色。
B.取少量紫色清液于试管中,向其中加入几滴淀粉溶液,溶液不变蓝,再加入过量NaHSO3溶液,观察溶液是否变色。
C.取少量紫色清液于试管中,向其中加入稀硝酸酸化,再加入几滴硝酸银溶液,观察是否生成黄色沉淀。
Ⅲ.KMnO4的应用
(5)采用KMnO4滴定法测定某FeC2O4·2H2O样品(杂质不参与反应)的纯度,实验步骤:取mg样品于锥形瓶中,加入稀H2SO4溶解。用cmol﹒L-1的KMnO4溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗KMnO4溶液VmL。样品中所含的FeC2O4·2H2O(M=180g·mol-1)质量分数表达式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某小组在实验室用NaClO溶液和NH3反应制备肼(N2H4),并进行相关性质探究实验。
Ⅰ.实验室制备N2H4
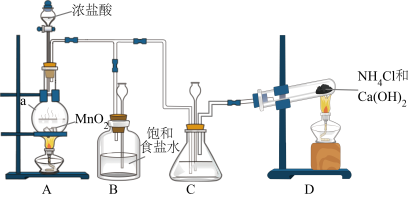
(1)装置D中反应的化学方程式是___________ 。
(2)装置C中盛放的试剂是___________ 。
(3)制备N2H4的离子方程式___________ 。
Ⅱ.测定产品中水合肼(N2H4·H2O)的含量
(4)称取产品6.0g,加入适量NaHCO3固体(调节溶液的pH保持在6.5左右),加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.3000mol/L的碘标准溶液滴定(已知:N2H4·H2O +2I2 = N2↑+ 4HI + H2O)。
①滴定到达终点的现象是___________ 。
②重复上述滴定实验2~3次,测得消耗碘标准溶液的平均值为20.00mL,产品中水合肼的质量分数为___________ 。
Ⅲ.探究肼的化学性质。将制得的肼分离提纯后,进行如下实验。
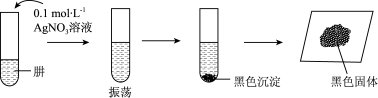
【查阅资料】AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】
(5)设计如下方案,进行实验。
③综合上述实验,肼具有的性质是___________
(6)N2H4是一种二元弱碱,在水中的电离与NH3相似,写出肼的第一步电离方程式___________
Ⅰ.实验室制备N2H4

(1)装置D中反应的化学方程式是
(2)装置C中盛放的试剂是
(3)制备N2H4的离子方程式
Ⅱ.测定产品中水合肼(N2H4·H2O)的含量
(4)称取产品6.0g,加入适量NaHCO3固体(调节溶液的pH保持在6.5左右),加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.3000mol/L的碘标准溶液滴定(已知:N2H4·H2O +2I2 = N2↑+ 4HI + H2O)。
①滴定到达终点的现象是
②重复上述滴定实验2~3次,测得消耗碘标准溶液的平均值为20.00mL,产品中水合肼的质量分数为
Ⅲ.探究肼的化学性质。将制得的肼分离提纯后,进行如下实验。

【查阅资料】AgOH在溶液中不稳定,易分解生成黑色的Ag2O,Ag2O可溶于氨水。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】
(5)设计如下方案,进行实验。
| 操作 | 现象 | 结论 |
| ⅰ.取少量黑色固体于试管中,加入足量① | 黑色固体部分溶解 | 黑色固体有Ag2O |
| ⅱ.取少量黑色固体于试管中,加入足量稀硝酸,振荡 | ② | 黑色固体是Ag和Ag2O |
(6)N2H4是一种二元弱碱,在水中的电离与NH3相似,写出肼的第一步电离方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】(NH4)2Cr2O7可用作有机合成催化剂、媒染剂、显影液等。某化学兴趣小组对(NH4)2Cr2O7的部分性质及组成进行探究。已知:Cr2O72-(橙色)+ H2O 2CrO42-(黄色)+ 2H+。请回答下列问题:
2CrO42-(黄色)+ 2H+。请回答下列问题:
(2)为探究(NH4)2Cr2O7(摩尔质量为252 g/mol)加热的分解产物,按下图连接好仪器,加热装置略去,在A中加入5.040 g样品进行实验。

②连接好装置,点燃酒精灯之前,先通入一段时间N2其目的为
③反应结束后,依然要通一段时间的氮气的原因是
④加热A至恒重,观察到D中溶液不变色,同时测得A中残留物为Cr2O3、B中质量的变化为1.44 g,写出重铬酸铵加热分解反应的化学方程式:
(3)实验室常用甲醛法测定含(NH4)2Cr2O7的样品中氮的质量分数(杂质不发生反应),其反应原理为2Ba2++Cr2O72-+ H2O = 2BaCrO4↓+2H+、4NH4++6HCHO =3H++6H2O+(CH2)6N4H+[滴定时,1 mol (CH2)6N4H+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。
实验步骤:称取样品5.600 g,配成500 mL溶液,移取25.00 mL样品溶液于250 mL锥形瓶中,用氯化钡溶液使Cr2O72-完全沉淀后,加入10 mL 20.00 mol·L-1的中性甲醛溶液,摇匀、静置5 min后,加入1〜2滴酚酞试液,用0.200 mol • L-1NaOH标准溶液滴定至终点。重复上述操作3次,最终滴定用去NaOH标准溶液体积的平均值为16.00 mL。
①若滴定终点时,俯视读数,则测定结果
②滴定计算得该样品中氮的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】醋酸镍[(CH3COO)2Ni]是一种重要的化工原料。一种以含镍废料(含NiS、Al2O3、FeO、CaO、SiO2)为原料,制取醋酸镍的工艺流程图如下:
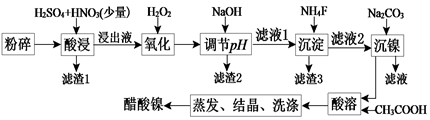
相关离子生成氢氧化物的pH和相关物质的溶解性如下表:
(1)将粉碎的含镍废料酸浸时要不断搅拌,粉碎和搅拌的目的是________________ 。
(2)调节pH步骤中,溶液pH的调节范围是__________________________________ 。
(3)滤渣1和滤渣3主要成分的化学式分别是________________ ,_____________ 。
(4)氧化步骤中加入H2O2发生反应的离子方程式为____________________________ 。
(5)酸浸过程中,lmol NiS失去6NA个电子,同时生成两种无色有毒气体。该反应的化学方程式为____________________ 。
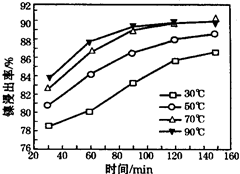
(6)保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如右图。酸浸的最佳温度与时间分别为:_______ ℃、_______ min。
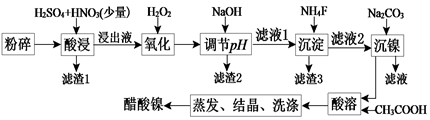
相关离子生成氢氧化物的pH和相关物质的溶解性如下表:
| 金属离子 | 开始沉淀pH | 沉淀完全pH | 物质 | 20℃溶解性(H2O) | |
| Fe3+ | 1.1 | 3.2 | CaSO4 | 微溶 | |
| Fe2+ | 5.8 | 8.8 | NiF2 | 可溶 | |
| Al3+ | 3.0 | 5.0 | CaF2 | 难溶 | |
| Ni2+ | 6.7 | 9.5 | NiCO3 | Ksp=9.6×10-6 |
(2)调节pH步骤中,溶液pH的调节范围是
(3)滤渣1和滤渣3主要成分的化学式分别是

(4)氧化步骤中加入H2O2发生反应的离子方程式为
(5)酸浸过程中,lmol NiS失去6NA个电子,同时生成两种无色有毒气体。该反应的化学方程式为
(6)保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如右图。酸浸的最佳温度与时间分别为:
您最近一年使用:0次
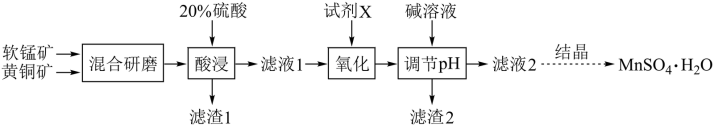
【推荐2】硫酸锰晶体(MnSO4·H2O)是一种重要的化工原料,利用软锰矿(主要成分为MnO2)和黄铜矿(主要成分为CuFeS2)可以制取(MnSO4·H2O),其化工生产流程如下:
已知:Ksp[Mn(OH)2]=4.0×10-14、Ksp[Cu(OH)2]=2.0×10-20、Ksp[Fe(OH)3]=2.6×10-39、Ksp[Fe(OH)2]=1×10-16.3;
(1)将矿石混合研磨成细粉的目的是_______ ,“酸浸”过程中得到滤渣1为单质硫,滤液中含有Cu2+、Mn2+、Fe3+,写出“酸浸”发生反应的离子方程式:_______ 。
(2)氧化的目的是将酸性滤液中可能含有的Fe2+转化为Fe3+,则试剂X可能为_______ (填化学式)。检验滤液1中Fe3+常用的试剂为_______ 。
(3)滤渣2的成分为_______ (填化学式),为了得到较为纯净的MnSO4·H2O,使用碱液调节pH的范围为_______ 。(lg2=0.3)(已知:①滤液2中Mn2+的浓度为0.02mol/L;②当离子浓度小于10-6mol/L时,即可认为该离子已除净)
(4)若工艺流程改为先“调节pH”后“氧化”,则“滤液2”中可能含有的杂质离子为_______ 。
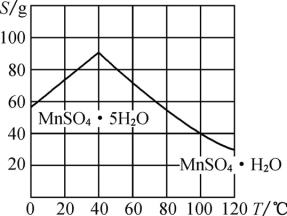
(5)结合图象,由滤液2获得(MnSO4·H2O)晶体的具体实验步骤是加1.0mol/L稀硫酸酸化,高于40℃蒸发结晶、_______ ,酒精洗涤,低温干燥 。

已知:Ksp[Mn(OH)2]=4.0×10-14、Ksp[Cu(OH)2]=2.0×10-20、Ksp[Fe(OH)3]=2.6×10-39、Ksp[Fe(OH)2]=1×10-16.3;
(1)将矿石混合研磨成细粉的目的是
(2)氧化的目的是将酸性滤液中可能含有的Fe2+转化为Fe3+,则试剂X可能为
(3)滤渣2的成分为
(4)若工艺流程改为先“调节pH”后“氧化”,则“滤液2”中可能含有的杂质离子为
(5)结合图象,由滤液2获得(MnSO4·H2O)晶体的具体实验步骤是加1.0mol/L稀硫酸酸化,高于40℃蒸发结晶、

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】某化工厂用水钴矿(主要成分为 ,含少量
,含少量 、
、 、MnO等)制取
、MnO等)制取 的工艺流程如下:
的工艺流程如下:
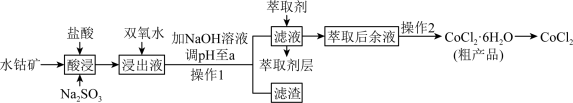
已知:i.氧化性: 。
。
ii.“酸浸”后溶液中含有的阳离子主要有 、
、 、
、 、
、 、
、 等。
等。
iii.室温下,部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(当离子浓度不大于 时,认为该离子沉淀完全)
时,认为该离子沉淀完全)
(1)为了提高“酸浸”效率,可以采取的措施有___________ (写一条即可)。
(2)写出 与
与 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
(3)“浸出液”中加入双氧水的目的是___________ 。
(4)加NaOH溶液调节pH至a除铁和铝,则a的最小值为___________ ;当 时,溶液中
时,溶液中
___________  。
。
(5)“滤液”中加入萃取剂的作用是___________ 。
 ,含少量
,含少量 、
、 、MnO等)制取
、MnO等)制取 的工艺流程如下:
的工艺流程如下:
已知:i.氧化性:
 。
。ii.“酸浸”后溶液中含有的阳离子主要有
 、
、 、
、 、
、 、
、 等。
等。iii.室温下,部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(当离子浓度不大于
 时,认为该离子沉淀完全)
时,认为该离子沉淀完全)| 沉淀物 |  |  |  |  |  |
| 沉淀完全时的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)写出
 与
与 溶液反应的离子方程式
溶液反应的离子方程式(3)“浸出液”中加入双氧水的目的是
(4)加NaOH溶液调节pH至a除铁和铝,则a的最小值为
 时,溶液中
时,溶液中
 。
。(5)“滤液”中加入萃取剂的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】乳酸亚铁晶体{[CH3CH(OH)COO]2Fe·3H2O,Mr=288}是常用的补铁剂。乳酸亚铁可由乳酸与FeCO3反应制得。
Ⅰ.制备碳酸亚铁(FeCO3)
(1)利用如图所示装置进行实验,进行以下两步操作:
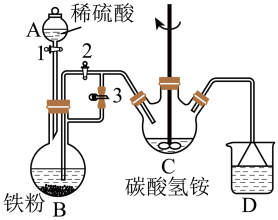
第一步:关闭活塞2,依次打开活塞3、1,反应一段时间;
第二步:①___________ ,发现C中有白色沉淀和气体生成。
②要先进行第一步操作,反应一段时间后才能开始第二步操作的原因是___________ 。
③C中反应生成白色沉淀的离子方程式是___________ 。
④仪器C中的混合物经过滤,洗涤后得到FeCO3沉淀,检验其是否洗净的方法是___________ (填操作,现象和结论)。
Ⅱ.制备乳酸亚铁晶体和定量测量
(2)制备乳酸亚铁晶体。将制得的FeCO3加入到乳酸溶液中,加入少量铁粉,在70℃下搅拌使反应充分进行,静置一段时间后过滤,再经操作a,得到乳酸亚铁晶体,洗涤,干燥后得到产品。操作a的步骤包括(填操作过程)___________ 。
(3)用铈(Ce)量法测定产品中Fe2+的含量。取1.440g产品配成100mL溶液,每次取该溶液20.00mL,进行必要处理,用0.0500mol·L-1Ce(SO4)2标准溶液滴定至终点,平均消耗Ce(SO4)2标准液19.00mL。滴定反应如下:Ce4++Fe2+=Ce3++Fe3+,则产品中乳酸亚铁的质量分数为___________ 。
(4)该兴趣小组发现若用KMnO4法测定样品中亚铁离子的含量进而计算产品中乳酸亚铁的质量分数,产品的质量分数总是大于100%,其原因可能是___________ 。
Ⅰ.制备碳酸亚铁(FeCO3)
(1)利用如图所示装置进行实验,进行以下两步操作:

第一步:关闭活塞2,依次打开活塞3、1,反应一段时间;
第二步:①
②要先进行第一步操作,反应一段时间后才能开始第二步操作的原因是
③C中反应生成白色沉淀的离子方程式是
④仪器C中的混合物经过滤,洗涤后得到FeCO3沉淀,检验其是否洗净的方法是
Ⅱ.制备乳酸亚铁晶体和定量测量
(2)制备乳酸亚铁晶体。将制得的FeCO3加入到乳酸溶液中,加入少量铁粉,在70℃下搅拌使反应充分进行,静置一段时间后过滤,再经操作a,得到乳酸亚铁晶体,洗涤,干燥后得到产品。操作a的步骤包括(填操作过程)
(3)用铈(Ce)量法测定产品中Fe2+的含量。取1.440g产品配成100mL溶液,每次取该溶液20.00mL,进行必要处理,用0.0500mol·L-1Ce(SO4)2标准溶液滴定至终点,平均消耗Ce(SO4)2标准液19.00mL。滴定反应如下:Ce4++Fe2+=Ce3++Fe3+,则产品中乳酸亚铁的质量分数为
(4)该兴趣小组发现若用KMnO4法测定样品中亚铁离子的含量进而计算产品中乳酸亚铁的质量分数,产品的质量分数总是大于100%,其原因可能是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
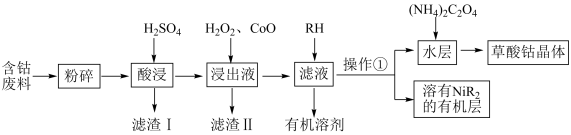
【推荐2】用含钴废料(主要成分为Co,含有一定量的NiO、Al2O3、Fe、SiO2等)制备草酸钴晶体(CoC2O4·2H2O)的工业流程如下图.已知:①草酸钴晶体难溶于水②RH为有机物(难电离)。请回答下列问题:
(1)滤渣I的主要成分是_____ (填化学式),写出一种能提高酸浸速率的措施_______ 。
(2)操作①用到的玻璃仪器有_______________ 。
(3)H2O2是一种绿色氧化剂,写出加入H2O2后发生反应的离子方程式:_______________ 。
(4)加入氧化钴的目的是调节溶液的pH.若要将浸出液中Fe3+和Al3+全部沉淀,则应将浸出液的PH控制在_______ 。(已知:溶液中离子浓度小于1×10-5mol/L,则认为离子完全沉淀;Ni(OH)2、Fe(OH)3、Al(OH)3的Ksp分别为1×10-15,1×10-38,1×10-32)
(5)加入(NH4)2C2O4反应的离子方程式为________ ,过滤得到的草酸钴晶体需要用蒸馏水洗涤,检验是否洗涤干净的方法是____________ 。
(6)加入有机萃取剂的目的是__________ 。实验室可以用酸性KMnO4标准液滴定草酸根离子(C2O42-)来测定溶液中C2O42-的浓度,KMnO4标准溶液常用硫酸酸化,若用盐酸酸化,会使测定结果______ (填“偏高”、“偏低”或“无影响”).
(1)滤渣I的主要成分是
(2)操作①用到的玻璃仪器有
(3)H2O2是一种绿色氧化剂,写出加入H2O2后发生反应的离子方程式:
(4)加入氧化钴的目的是调节溶液的pH.若要将浸出液中Fe3+和Al3+全部沉淀,则应将浸出液的PH控制在
(5)加入(NH4)2C2O4反应的离子方程式为
(6)加入有机萃取剂的目的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】铝元素在自然界中主要存在于铝土矿(主要成分为A ,还含有F
,还含有F 、FeO、Si
、FeO、Si )中.工业上用铝土矿制备铝的某种化合物的工艺流程如下。
)中.工业上用铝土矿制备铝的某种化合物的工艺流程如下。
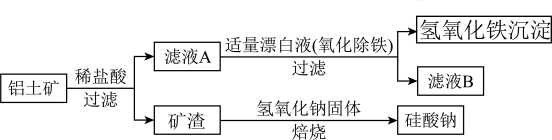
(1)在滤液A中加入漂白液,目的是氧化除铁,便于后期形成Fe(OH 沉淀,所得滤液B显酸性。
沉淀,所得滤液B显酸性。
①检验滤液A中含有F 的试剂为
的试剂为_____
②检验滤液B中不含有F 的实验操作方法为
的实验操作方法为_____ 。
③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为_____ (填选项编号)。
a.氢氧化钠溶液 b.硫酸溶液 c.二氧化碳 d.氨水
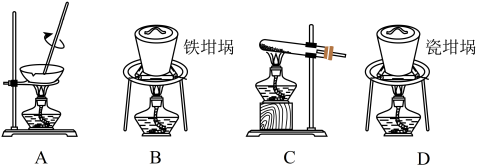
(2)矿渣中一定含有的物质是_____ (填化学式)。焙烧制备硅酸钠,可采用的装置为_____ (填选项编号)。
 ,还含有F
,还含有F 、FeO、Si
、FeO、Si )中.工业上用铝土矿制备铝的某种化合物的工艺流程如下。
)中.工业上用铝土矿制备铝的某种化合物的工艺流程如下。
(1)在滤液A中加入漂白液,目的是氧化除铁,便于后期形成Fe(OH
 沉淀,所得滤液B显酸性。
沉淀,所得滤液B显酸性。①检验滤液A中含有F
 的试剂为
的试剂为②检验滤液B中不含有F
 的实验操作方法为
的实验操作方法为③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为
a.氢氧化钠溶液 b.硫酸溶液 c.二氧化碳 d.氨水
(2)矿渣中一定含有的物质是

您最近一年使用:0次




