现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大。A元素的价电子构型为nsnnpn+1;C元素为最活泼的非金属元素;D元素核外有三个电子层,最外层电子数是核外电子总数的 ;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的未成对电子是第四周期最多的元素;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的未成对电子是第四周期最多的元素;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)A元素的第一电离能___ (填“<”“>”或“=”)B元素的第一电离能,A、B、C三种元素的电负性由小到大的顺序为___ (用元素符号表示)。
(2)D元素原子的价电子排布式是___ 。
(3)C元素的电子排布图为___ ;E3+的离子符号为___ 。
(4)F元素位于元素周期表的___ 区,其基态原子的电子排布式为___ 。
(5)G元素可能的性质___ 。
A.其单质可作为半导体材料 B.其电负性大于磷
C.其原子半径大于锗 D.其第一电离能小于硒
(6)活泼性:D___ Al(填“>”或“<”,下同),I1(Mg)___ I1(Al),其原因是___ 。
 ;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的未成对电子是第四周期最多的元素;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素基态原子的未成对电子是第四周期最多的元素;G元素与A元素位于同一主族,其某种氧化物有剧毒。(1)A元素的第一电离能
(2)D元素原子的价电子排布式是
(3)C元素的电子排布图为
(4)F元素位于元素周期表的
(5)G元素可能的性质
A.其单质可作为半导体材料 B.其电负性大于磷
C.其原子半径大于锗 D.其第一电离能小于硒
(6)活泼性:D
更新时间:2021-05-19 18:08:38
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有四种短周期元素,相关信息如下表。请根据表中信息回答:
(1)A在周期表中位于___________ 。
(2)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是__________ (填化学式)。
(3)已知硒(Se)与D同主族,且位于D的下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是__________ (填标号)。
a.其单质在常温下呈固态
b. 既有氧化性又有还原性
既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为
d.非金属性比C元素的强
| 元素 | 相关信息 |
| A | 气态氢化物极易溶于水,可用作制冷剂 |
| B | 单质的焰色为黄色 |
| C | 单质是黄绿色气体,可用于自来水消毒 |
| D | -2价阴离子的电子层结构与Ar原子相同 |
(2)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是
(3)已知硒(Se)与D同主族,且位于D的下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
a.其单质在常温下呈固态
b.
 既有氧化性又有还原性
既有氧化性又有还原性c.最高价氧化物对应的水化物的化学式为

d.非金属性比C元素的强
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4,请回答下列问题:
(1)用电子式表示Z2R的形成过程___________ 。
(2)W在周期表中的位置是___________ 。
(3)ZYX的电子式为___________ ,XQY的结构式为。___________ 。
(4)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是___________ (用元素的离子符号表示)。
(5)下列说法能证明非金属性Q强于R的是___________ (填字母)。
a.简单阴离子的还原性:Q>R
b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性:Q>R
d.Q与Fe反应生成Fe3+,R与Fe反应生成Fe2+
(6)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是___________ 。
(7)处于周期表中对角线位置(左上方和右下方)的元素,其性质具有相似性,称为“对角线规则”,写出Be(OH)2与氢氧化钠溶液反应的化学方程式___________ 。
(1)用电子式表示Z2R的形成过程
(2)W在周期表中的位置是
(3)ZYX的电子式为
(4)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(5)下列说法能证明非金属性Q强于R的是
a.简单阴离子的还原性:Q>R
b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性:Q>R
d.Q与Fe反应生成Fe3+,R与Fe反应生成Fe2+
(6)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是
(7)处于周期表中对角线位置(左上方和右下方)的元素,其性质具有相似性,称为“对角线规则”,写出Be(OH)2与氢氧化钠溶液反应的化学方程式
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】I、 X、Y、Z三种常见的短周期元素,可以形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物。已知Y的离子和Z的离子有相同的电子层结构,X离子比Y离子多1个电子层。试回答:
(1)X在周期表中的位置___________ ,Z2Y2的电子式_________ ,含有的化学键____________ 。
(2)Z2Y2溶在水中的反应方程式为__________________________ 。
(3)用电子式表示Z2X的形成过程_________________________ 。
II、以乙烯为原料可以合成很多的化工产品,已知有机物D是一种有水果香味的油状液体。试根据下图回答有关问题:
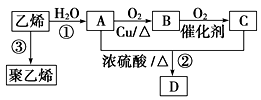
(4)反应①②的反应类型分别是__________ 、__________ 。
(5)决定有机物A、C的化学特性的原子团的名称分别是_____________ 。
(6)写出图示反应②、③的化学方程式:
②_________________________________________ ;
③__________________________________________ 。
(1)X在周期表中的位置
(2)Z2Y2溶在水中的反应方程式为
(3)用电子式表示Z2X的形成过程
II、以乙烯为原料可以合成很多的化工产品,已知有机物D是一种有水果香味的油状液体。试根据下图回答有关问题:

(4)反应①②的反应类型分别是
(5)决定有机物A、C的化学特性的原子团的名称分别是
(6)写出图示反应②、③的化学方程式:
②
③
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】磷、氮和硫的相关化合物在药物化学及农业化学领域应用广泛。回答下列问题:
(1) 分子空间结构为
分子空间结构为___________ , 与
与 反应生成
反应生成 ,
, 结构为
结构为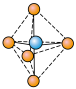 ,
, 是
是___________ (填“极性”或“非极性”)分子。
(2)氯吡苯脲是一种常用的膨大剂,其结构简式为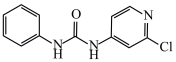 ,它是经国家批准使用的植物生长调节剂。
,它是经国家批准使用的植物生长调节剂。
①氯吡苯脲分子___________ (填“是”或“不是”)手性分子。
②氯吡苯脲分子中存在的作用力包括___________ (填字母)。
A.离子键 B.极性键 C.非极性键 D. 键 E.配位键
键 E.配位键
(3)胆矾 可写成
可写成 ,其结构示意图如下:
,其结构示意图如下:
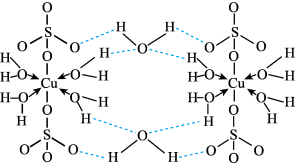
⑤该配合物的中心离子是___________ 。
②下列关于胆矾的说法正确的是___________ (填字母)。
A.基态 的价层电子排布式为
的价层电子排布式为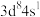
B.胆矾在不同温度下分步失去结晶水
C.根据结构图显示,胆矾在微观层次是平面结构
D.胆矾中的水分子间存在氢键
(1)
 分子空间结构为
分子空间结构为 与
与 反应生成
反应生成 ,
, 结构为
结构为 ,
, 是
是(2)氯吡苯脲是一种常用的膨大剂,其结构简式为
 ,它是经国家批准使用的植物生长调节剂。
,它是经国家批准使用的植物生长调节剂。①氯吡苯脲分子
②氯吡苯脲分子中存在的作用力包括
A.离子键 B.极性键 C.非极性键 D.
 键 E.配位键
键 E.配位键(3)胆矾
 可写成
可写成 ,其结构示意图如下:
,其结构示意图如下:
⑤该配合物的中心离子是
②下列关于胆矾的说法正确的是
A.基态
 的价层电子排布式为
的价层电子排布式为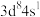
B.胆矾在不同温度下分步失去结晶水
C.根据结构图显示,胆矾在微观层次是平面结构
D.胆矾中的水分子间存在氢键
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】砷化镓(GaAs)是优良的半导体材料,其晶体结构与单晶硅相似。
(1)基态Ga原子的价电子排布式为___________ ,其同周期元素中未成对电子数最多的是___________ (填元素符号)。
(2)GaAs可用 (常温下为无色液体)和
(常温下为无色液体)和 高温反应制得,同时生成另一种产物,写出反应方程式
高温反应制得,同时生成另一种产物,写出反应方程式___________ ,另一种产物中心原子的杂化类型为___________ 。
(3)沸点
___________  (填“>”、“<”、“=”),原因是
(填“>”、“<”、“=”),原因是___________ 。
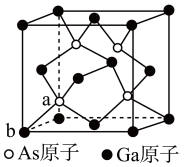
(4)GaAs的晶胞结构如图所示,键角___________ ,若晶胞中距离最近的两个Ga原子距离为a nm,阿伏加德罗常数的值为 ,则GaAs的密度为
,则GaAs的密度为___________  。
。
(1)基态Ga原子的价电子排布式为
(2)GaAs可用
 (常温下为无色液体)和
(常温下为无色液体)和 高温反应制得,同时生成另一种产物,写出反应方程式
高温反应制得,同时生成另一种产物,写出反应方程式(3)沸点

 (填“>”、“<”、“=”),原因是
(填“>”、“<”、“=”),原因是(4)GaAs的晶胞结构如图所示,键角
 ,则GaAs的密度为
,则GaAs的密度为 。
。
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】2014年7月和12月山西大学分子科学研究所翟华金教授、李思殿教授与清华大学李隽教授、美国布朗大学Lai-Sheng Wang教授及复旦大学刘智攀教授课题组合作,首次合成“中国红灯笼分子”——硼球烯B40。B40是继C60之后第二个从实验和理论上完全确认的无机非金属笼状团簇。
(1) 基态硼原子的外围电子排布式为___________ ,碳60中碳原子杂化方式为____________ 。
(2)构成碳60晶体的作用力是___________________ 。
⑶与硼同周期但第一电离能比硼大的元素有___________ 种。
(4)磷化硼(BP)是由硼元素与磷元素组成的无机化合物,属于一种半导体材料。磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成。BP晶胞中B采用面心立方堆积,P原子填入四面体空隙中。
①写出三溴化硼和三溴化磷的空间构型:
三溴化硼__________ ;三溴化磷____________ 。
②磷化硼晶体内微粒间的作用力有__________ 。
③计算磷化硼中硼原子和磷原子之间的最近距离(晶胞参数为478pm)____________ 。

(1) 基态硼原子的外围电子排布式为
(2)构成碳60晶体的作用力是
⑶与硼同周期但第一电离能比硼大的元素有
(4)磷化硼(BP)是由硼元素与磷元素组成的无机化合物,属于一种半导体材料。磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成。BP晶胞中B采用面心立方堆积,P原子填入四面体空隙中。
①写出三溴化硼和三溴化磷的空间构型:
三溴化硼
②磷化硼晶体内微粒间的作用力有
③计算磷化硼中硼原子和磷原子之间的最近距离(晶胞参数为478pm)
您最近半年使用:0次
【推荐1】在建国70周年阅兵仪式上,“歼20”“东风-41核导弹”等国之重器亮相,它们采用了大量合金材料。回答下列问题:
(1)早期战斗机主要采用铝合金,其中超硬铝属Al-Cu-Mg-Zn系。Cu在元素周期表中的位置是___ ,比较第一电离能Al___ Mg(填“>”“<”“=”)。
(2)查阅资料显示第二电离能Cu大于Zn,理由是___ 。
(3)中期战斗机主要采用钛合金,Ti的价电子排布图为___ 。钛晶体在882℃以上为体心立方的β钛,其中钛原子的配位数为___ 。
(4)钛镍合金可用于战斗机的油压系统,该合金溶于热的硫酸生成Ti(SO4)2、NiSO4,其中阴离子的中心原子杂化类型是___ 。
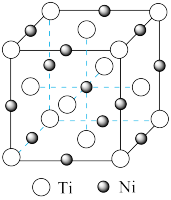
(5)一种钛镍合金的立方晶胞结构如图所示,若晶胞的边长为a pm,则晶胞的密度为___ g/cm3(用含a、NA的计算式表示)。
(6)隐形战机采用Fe(CO)5(羰基铁)作为吸波材料,羰基铁在常温下为红棕色液体,固体羰基铁属于___ 晶体,CO与Fe之间的化学键称为___ 。
(1)早期战斗机主要采用铝合金,其中超硬铝属Al-Cu-Mg-Zn系。Cu在元素周期表中的位置是
(2)查阅资料显示第二电离能Cu大于Zn,理由是
(3)中期战斗机主要采用钛合金,Ti的价电子排布图为
(4)钛镍合金可用于战斗机的油压系统,该合金溶于热的硫酸生成Ti(SO4)2、NiSO4,其中阴离子的中心原子杂化类型是
(5)一种钛镍合金的立方晶胞结构如图所示,若晶胞的边长为a pm,则晶胞的密度为

(6)隐形战机采用Fe(CO)5(羰基铁)作为吸波材料,羰基铁在常温下为红棕色液体,固体羰基铁属于
您最近半年使用:0次
【推荐2】氮族元素是一类重要元素,广泛应用于生产生活,特别是在医药、纳米材料制备中。
(1)氮化硼(BN)是由氮原子和硼原子所构成的晶体。工业上制备氮化硼的一种方法为 。形成BCl3时,基态B原子价电子层上的电子先激发再杂化,激发时B原子的价电子轨道表示式可能为___________(填标号)。
。形成BCl3时,基态B原子价电子层上的电子先激发再杂化,激发时B原子的价电子轨道表示式可能为___________(填标号)。
(2)肼(N2H4)和偏二甲肼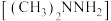 均为无色液体,属于同系物,是常用的火箭推进剂,其熔沸点如表,二者熔沸点差异较大的主要原因是
均为无色液体,属于同系物,是常用的火箭推进剂,其熔沸点如表,二者熔沸点差异较大的主要原因是______________________ 。
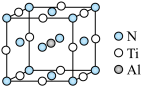
(3)Al掺杂的氮化钛晶胞结构如图所示。距离Ti最近的Al有___________ 个,已知阿伏加德罗常数的值为NA,若晶体的密度为ρg∙cm-3,该晶胞的边长为___________ pm(列出算式)。
(4)吡啶( )是类似于苯的芳香化合物,工业上用作合成药品、消毒剂、染料等的原料。
)是类似于苯的芳香化合物,工业上用作合成药品、消毒剂、染料等的原料。
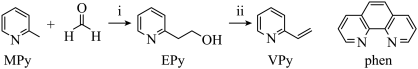
2-乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如图路线合成。
①MPy的分子式为___________ ,分子中的大π键可用 表示,则吡啶中大π键表示为
表示,则吡啶中大π键表示为___________ 。
②MPy→EPy的反应类型为___________ 。
③邻二氮菲(phen,结构如图)中的N与吡啶中N的杂化方式一致,邻二氮菲通过N原子与Fe2+形成稳定的配合物 ,该配合物的特征颜色可测定Fe2+的浓度。
,该配合物的特征颜色可测定Fe2+的浓度。 中Fe2+的配位数为
中Fe2+的配位数为___________ ;实验表明,邻二氮菲检验Fe2+的适宜pH范围是2~9,试分析原因是____________ 。
(1)氮化硼(BN)是由氮原子和硼原子所构成的晶体。工业上制备氮化硼的一种方法为
 。形成BCl3时,基态B原子价电子层上的电子先激发再杂化,激发时B原子的价电子轨道表示式可能为___________(填标号)。
。形成BCl3时,基态B原子价电子层上的电子先激发再杂化,激发时B原子的价电子轨道表示式可能为___________(填标号)。A.  | B. 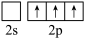 |
C.  | D. 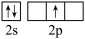 |
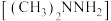 均为无色液体,属于同系物,是常用的火箭推进剂,其熔沸点如表,二者熔沸点差异较大的主要原因是
均为无色液体,属于同系物,是常用的火箭推进剂,其熔沸点如表,二者熔沸点差异较大的主要原因是| 物质 | 肼 | 偏二甲肼 |
| 熔点 | 1.4℃ |  |
| 沸点 | 113.5℃ | 63.9℃ |

(4)吡啶(
 )是类似于苯的芳香化合物,工业上用作合成药品、消毒剂、染料等的原料。
)是类似于苯的芳香化合物,工业上用作合成药品、消毒剂、染料等的原料。2-乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如图路线合成。

①MPy的分子式为
 表示,则吡啶中大π键表示为
表示,则吡啶中大π键表示为②MPy→EPy的反应类型为
③邻二氮菲(phen,结构如图)中的N与吡啶中N的杂化方式一致,邻二氮菲通过N原子与Fe2+形成稳定的配合物
 ,该配合物的特征颜色可测定Fe2+的浓度。
,该配合物的特征颜色可测定Fe2+的浓度。 中Fe2+的配位数为
中Fe2+的配位数为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】碳、氢、硫元素及其化合物在自然界广泛存在并具有许多用途。请回答下列有关问题:
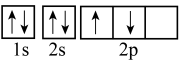
(1)某同学画出的基态碳原子的核外电子轨道表示式如下图,该电子排布图违背了_______ (填字母)。
A.泡利原理 B.洪特规则 C.能量最低原理
(2) 、
、 均是有机反应的重要中间体,
均是有机反应的重要中间体, 的空间构型为
的空间构型为_______ , 中心碳正离子的杂化方式是
中心碳正离子的杂化方式是_______ 。
(3)类卤素 对应的酸有硫氰酸
对应的酸有硫氰酸 和异硫氰酸
和异硫氰酸 两种,其中硫氰酸的沸点
两种,其中硫氰酸的沸点_______ 异硫氰酸的沸点(填“<”、“=”、“>”)。
(4)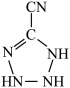 中
中 键与
键与 键的个数比为
键的个数比为_______ 。
(5)石墨相氮化碳是光催化剂研究的热点之一,类似石墨层状结构,其结构单元及晶胞如图所示。
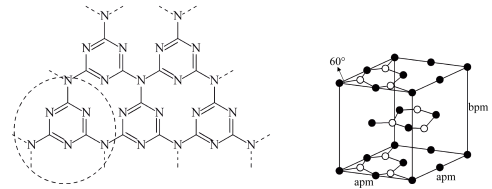
①石墨相氮化碳的化学式为_______ 。
②晶体中存在的微粒间作用力有_______ (填字母)。
a.极性键 b.氢键 c.金属键 d.范德华力
③该晶体的密度为_______  (只列出计算表达式,
(只列出计算表达式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)某同学画出的基态碳原子的核外电子轨道表示式如下图,该电子排布图违背了

A.泡利原理 B.洪特规则 C.能量最低原理
(2)
 、
、 均是有机反应的重要中间体,
均是有机反应的重要中间体, 的空间构型为
的空间构型为 中心碳正离子的杂化方式是
中心碳正离子的杂化方式是(3)类卤素
 对应的酸有硫氰酸
对应的酸有硫氰酸 和异硫氰酸
和异硫氰酸 两种,其中硫氰酸的沸点
两种,其中硫氰酸的沸点(4)
 中
中 键与
键与 键的个数比为
键的个数比为(5)石墨相氮化碳是光催化剂研究的热点之一,类似石墨层状结构,其结构单元及晶胞如图所示。

①石墨相氮化碳的化学式为
②晶体中存在的微粒间作用力有
a.极性键 b.氢键 c.金属键 d.范德华力
③该晶体的密度为
 (只列出计算表达式,
(只列出计算表达式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近半年使用:0次
【推荐1】氟及其化合物用途非常广泛。回答下列问题:
(1)聚四氟乙烯商品名称为“特氟龙”,可做不粘锅涂层。它是一种准晶体,该晶体是一种无平移周期序、但有严格准周期位置序的独特晶体。可通过____ 方法区分晶体、准晶体和非晶体。
(2)基态锑(Sb)原子价电子排布的轨道式为____ 。[H2F]+[SbF6]-(氟酸锑)是一种超强酸,存在[H2F]+,该离子的空间构型为______ ,依次写出一种与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是_______ 、_________ 。
(3)硼酸(H3BO3)和四氟硼酸铵(NH4BF4)都有着重要的化工用途。
①H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序_____ (填元素符号)。
②H3BO3本身不能电离出H+,在水中易结合一个OH﹣生成[B(OH)4]﹣,而体现弱酸性。[B(OH)4]﹣中B原子的杂化类型为_____ 。
③NH4BF4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在_______ (填序号):
A.离子键 B.σ键 C.π键 D.配位键 E.范德华力
(4)某砷镍合金的晶胞如图所示,设阿伏加 德罗常数的值为NA,该晶体的密度ρ=____ g/cm3。

(1)聚四氟乙烯商品名称为“特氟龙”,可做不粘锅涂层。它是一种准晶体,该晶体是一种无平移周期序、但有严格准周期位置序的独特晶体。可通过
(2)基态锑(Sb)原子价电子排布的轨道式为
(3)硼酸(H3BO3)和四氟硼酸铵(NH4BF4)都有着重要的化工用途。
①H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序
②H3BO3本身不能电离出H+,在水中易结合一个OH﹣生成[B(OH)4]﹣,而体现弱酸性。[B(OH)4]﹣中B原子的杂化类型为
③NH4BF4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在
A.离子键 B.σ键 C.π键 D.配位键 E.范德华力
(4)某砷镍合金的晶胞如图所示,设阿伏加 德罗常数的值为NA,该晶体的密度ρ=

您最近半年使用:0次
【推荐2】嫦娥五号带回的月球土壤中可能存在金、银、铜、铁、锌、铼等元素。
(1)鉴定月球土壤的元素组成,可采用的方法是_______ 。
A.光谱分析 B.质谱分析 C.X-射线衍射分析
(2)铼位于第六周期,与锰属于同一副族。类比锰,写出基态铼(Re)原子的价层电子排布式_______ 。
(3)第二电离能(I2):I2(Cu)_______ I2(Zn)(填“>”“<”或“=”),原因是_______ 。
(4)[Zn(IMI)4](ClO4)2是Zn2+的一种配合物,IMI的结构为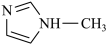 。
。
①IMI分子中碳原子的杂化方式有_______ 。
②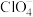 中,氯原子的价层电子对数为
中,氯原子的价层电子对数为_______ ,其立体构型为_______ 。
③常温下IMI的某种衍生物与甘氨酸形成的离子化合物(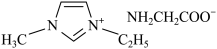 )为液态而非固态,其原因可能是
)为液态而非固态,其原因可能是_______ 。
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______ 。六棱柱底边边长为acm,高为ccm,阿伏加德罗常数的值为NA,Zn的密度为_______ g/cm3(列出计算式)。

(1)鉴定月球土壤的元素组成,可采用的方法是
A.光谱分析 B.质谱分析 C.X-射线衍射分析
(2)铼位于第六周期,与锰属于同一副族。类比锰,写出基态铼(Re)原子的价层电子排布式
(3)第二电离能(I2):I2(Cu)
(4)[Zn(IMI)4](ClO4)2是Zn2+的一种配合物,IMI的结构为
 。
。①IMI分子中碳原子的杂化方式有
②
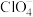 中,氯原子的价层电子对数为
中,氯原子的价层电子对数为③常温下IMI的某种衍生物与甘氨酸形成的离子化合物(
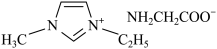 )为液态而非固态,其原因可能是
)为液态而非固态,其原因可能是(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E五种元素位于元素周期表中前四周期,原子序数依次增大。A元素的价电子排布为nsnnpn+1;B元素原子最外层电子数是次外层电子数的3倍;C位于B的下一周期,是本周期最活泼的金属元素;D基态原子的3d原子轨道上的电子数是4s原子轨道上的4倍;E元素原子的4p轨道上有3个未成对电子。
回答下列问题(用元素符号表示或按要求作答)。
(1)A、B、C的第一电离能由小到大的顺序为__________ ,三者电负性由大到小的顺序为__________ ;
(2)A和E的简单气态氢化物沸点高的是__________ ,其原因是__________ ;
(3)E基态原子的价电子轨道表示式为__________
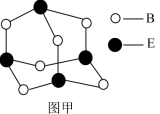
(4)B和E形成分子的结构如图甲所示,该分子的化学式为__________ ,E原子的杂化类型为__________ ;
(5)B和C能形成离子化合物R,其晶胞结构如图乙所示:
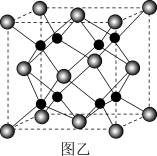
①一个晶胞中含__________ 个B离子。R的化学式为__________ ;
②晶胞参数为apm,则晶体R的密度__________ g•cm-3(只列计算式)。
回答下列问题(用元素符号表示或按要求作答)。
(1)A、B、C的第一电离能由小到大的顺序为
(2)A和E的简单气态氢化物沸点高的是
(3)E基态原子的价电子轨道表示式为
(4)B和E形成分子的结构如图甲所示,该分子的化学式为

(5)B和C能形成离子化合物R,其晶胞结构如图乙所示:

①一个晶胞中含
②晶胞参数为apm,则晶体R的密度
您最近半年使用:0次



