综合利用富钛废渣(含TiO2、ZnO、Fe2O3和少量有机物)制备锂离子电池正极材料中间体,并获得部分副产品的工艺流程如图:
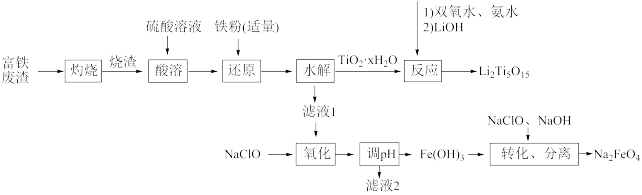
已知:Ksp[Zn(OH)2]=1.0×10-17、Ksp[Fe(OH)2]=1.0×10-16、Ksp[Fe(OH)3]=1.0×10-38,溶液中离子浓度≤10-5mol/L时认为该离子沉淀完全。回答下列问题:
(1)“灼烧”除去的物质为___ 。
(2)“还原”(避免水解产生其他杂质)中发生的主要离子反应为___ 。
(3)“酸溶”后钛以TiO2+形式存在,则“水解”反应的离子方程式为___ 。
(4)若“氧化”后所得溶液中金属离子的浓度均为0.1mol/L,则“调pH”的合理范围为___ 。
(5)“转化、分离”生成Na2FeO4,氧化剂与还原剂的物质的量之比为___ 。

已知:Ksp[Zn(OH)2]=1.0×10-17、Ksp[Fe(OH)2]=1.0×10-16、Ksp[Fe(OH)3]=1.0×10-38,溶液中离子浓度≤10-5mol/L时认为该离子沉淀完全。回答下列问题:
(1)“灼烧”除去的物质为
(2)“还原”(避免水解产生其他杂质)中发生的主要离子反应为
(3)“酸溶”后钛以TiO2+形式存在,则“水解”反应的离子方程式为
(4)若“氧化”后所得溶液中金属离子的浓度均为0.1mol/L,则“调pH”的合理范围为
(5)“转化、分离”生成Na2FeO4,氧化剂与还原剂的物质的量之比为
更新时间:2021-05-20 17:30:07
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】某同学欲在实验室中完成Fe与水蒸气反应的实验,装置如图甲、乙两种。
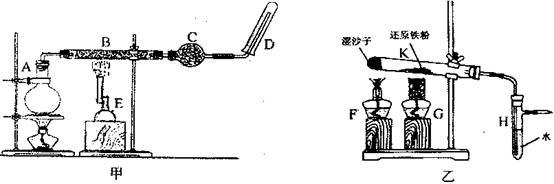
已知B中放入的是铁与石棉绒的混合物,C中放的是干燥剂,E为酒精喷灯,G为带有铁丝网罩的酒精灯。
Ⅰ.对比两装置,回答下列问题:
(1)如何检查乙装置的气密性?_____________________________________ 。
(2)乙装置中湿沙子的作用是________________________________________ 。
(3)B处发生反应的化学方程式:__________________________________________ 。
(4)该同学认为欲在乙装置的尖嘴导管处点燃反应产生的气体,装置H必不可少,H的作用是__________________ 。
(5)对比甲、乙两装置的B和K,B的优点是______________________________ 。
Ⅱ.某同学为了研究一定时间内铁粉的转化率,用上图中的甲装置设计了如下实验:准确称量一定质量的铁粉进行反应,收集并测量反应后生成的气体体积,计算铁粉的转化率。
①用排水法收集并测量气体体积可选下图中的_________________ 装置。
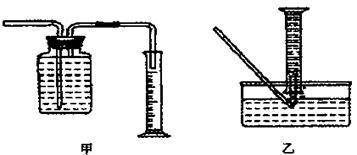
②称取mg铁粉与适量石棉绒混合,然后加热至无气体放出。若收集的气体体积换算为标准状况为VL,铁粉的转化率为(列出计算式即可)________________________ 。
③为了证明反应后的固体混合物中含有+3价的Fe,该同学取出少量混合物于试管中,加入足量的盐酸,溶解后过滤,立即向溶液中滴加KSCN溶液,结果观察到溶液的颜色没变化。经过思考,该同学认为此现象不能说明反应后的固体混合物中不含有+3价Fe。他的理由是:______________ 。

已知B中放入的是铁与石棉绒的混合物,C中放的是干燥剂,E为酒精喷灯,G为带有铁丝网罩的酒精灯。
Ⅰ.对比两装置,回答下列问题:
(1)如何检查乙装置的气密性?
(2)乙装置中湿沙子的作用是
(3)B处发生反应的化学方程式:
(4)该同学认为欲在乙装置的尖嘴导管处点燃反应产生的气体,装置H必不可少,H的作用是
(5)对比甲、乙两装置的B和K,B的优点是
Ⅱ.某同学为了研究一定时间内铁粉的转化率,用上图中的甲装置设计了如下实验:准确称量一定质量的铁粉进行反应,收集并测量反应后生成的气体体积,计算铁粉的转化率。
①用排水法收集并测量气体体积可选下图中的

②称取mg铁粉与适量石棉绒混合,然后加热至无气体放出。若收集的气体体积换算为标准状况为VL,铁粉的转化率为(列出计算式即可)
③为了证明反应后的固体混合物中含有+3价的Fe,该同学取出少量混合物于试管中,加入足量的盐酸,溶解后过滤,立即向溶液中滴加KSCN溶液,结果观察到溶液的颜色没变化。经过思考,该同学认为此现象不能说明反应后的固体混合物中不含有+3价Fe。他的理由是:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】乳酸亚铁晶体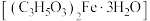 是一种吸收效果很好的食品铁强化剂,易溶于水,难溶于乙醇。某兴趣小组用废铁屑(部分被氧化)制备
是一种吸收效果很好的食品铁强化剂,易溶于水,难溶于乙醇。某兴趣小组用废铁屑(部分被氧化)制备 ,再与乳酸反应制得乳酸亚铁晶体。
,再与乳酸反应制得乳酸亚铁晶体。
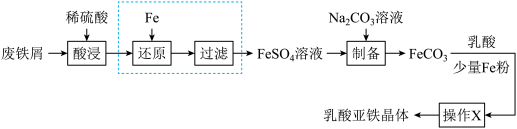
(1)“酸浸”时, 单质发生反应的离子方程式有
单质发生反应的离子方程式有___________ 。
(2)向酸浸液中滴加___________ (填化学式)溶液可判断是否要进行“还原”、“过滤”操作;在实验室中进行过滤操作需要的玻璃仪器有___________ 。
(3)制备过程中将 溶液加入
溶液加入 溶液中制得
溶液中制得 。
。
①该反应的离子方程式为___________ 。
②若 置于空气中时间过长,表面生成
置于空气中时间过长,表面生成 ,其原因是
,其原因是___________ (用化学方程式表示)。
(4) 与乳酸反应过程中加入少量铁粉的目的是
与乳酸反应过程中加入少量铁粉的目的是___________ 。
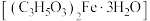 是一种吸收效果很好的食品铁强化剂,易溶于水,难溶于乙醇。某兴趣小组用废铁屑(部分被氧化)制备
是一种吸收效果很好的食品铁强化剂,易溶于水,难溶于乙醇。某兴趣小组用废铁屑(部分被氧化)制备 ,再与乳酸反应制得乳酸亚铁晶体。
,再与乳酸反应制得乳酸亚铁晶体。
(1)“酸浸”时,
 单质发生反应的离子方程式有
单质发生反应的离子方程式有(2)向酸浸液中滴加
(3)制备过程中将
 溶液加入
溶液加入 溶液中制得
溶液中制得 。
。①该反应的离子方程式为
②若
 置于空气中时间过长,表面生成
置于空气中时间过长,表面生成 ,其原因是
,其原因是(4)
 与乳酸反应过程中加入少量铁粉的目的是
与乳酸反应过程中加入少量铁粉的目的是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
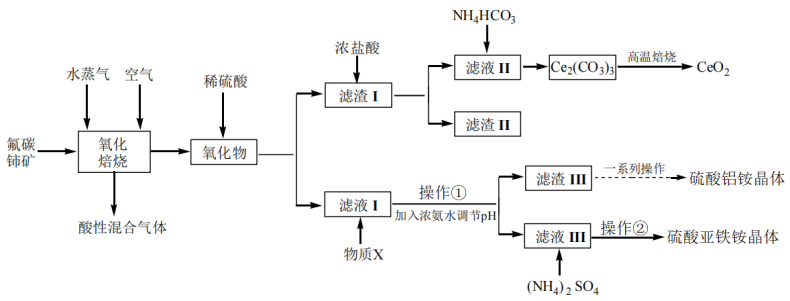
【推荐3】二氧化铈可用在化妆品中起到抗紫外线作用,工业上以氟碳铈矿(CeCO3F,含Fe2O3、SiO2、Al2O3等杂质)为原料制备二氧化铈、硫酸铝铵晶体 和硫酸亚铁铵
和硫酸亚铁铵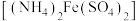 晶体,其工艺流程如图所示:
晶体,其工艺流程如图所示:
已知:①CeO2不溶于稀硫酸,也不溶于NaOH溶液,Ce2O3易溶于强酸。
②常见离子开始沉淀和完全沉淀pH表
回答下列问题:
(1)“氧化焙烧”时,气体与矿料逆流而行进行投料,其目的是___________ ,此时,发生化学方程式为___________ 。
(2)“滤渣Ⅰ”的主要成分是___________ 和___________ (填化学式)。虽浓盐酸价格便宜,但用于溶解“滤渣Ⅰ”的缺点是___________ ,若用稀硫酸和双氧水代替浓盐酸,则发生反应的离子方程式为___________ 。
(3)“滤液Ⅰ”中加入物质X的目的是___________ 。
(4)“操作①”加入浓氨水调节pH后,溶液pH范围是___________ 。
(5)“滤渣Ⅲ”在制备硫酸铝铵晶体过程中,理论上需加入稀硫酸和(NH4)2SO4的物质的量之比为___________ 。
 和硫酸亚铁铵
和硫酸亚铁铵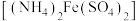 晶体,其工艺流程如图所示:
晶体,其工艺流程如图所示:
已知:①CeO2不溶于稀硫酸,也不溶于NaOH溶液,Ce2O3易溶于强酸。
②常见离子开始沉淀和完全沉淀pH表
| 离子 |  |  |  |
| 开始沉淀时的pH | 7.6 | 1.5 | 3.4 |
| 完全沉淀时的pH | 9.6 | 2.8 | 4.7 |
(1)“氧化焙烧”时,气体与矿料逆流而行进行投料,其目的是
(2)“滤渣Ⅰ”的主要成分是
(3)“滤液Ⅰ”中加入物质X的目的是
(4)“操作①”加入浓氨水调节pH后,溶液pH范围是
(5)“滤渣Ⅲ”在制备硫酸铝铵晶体过程中,理论上需加入稀硫酸和(NH4)2SO4的物质的量之比为
您最近一年使用:0次
【推荐1】 在工业上有广泛的用途。以硫铁矿(主要成分为
在工业上有广泛的用途。以硫铁矿(主要成分为 )为原料制备
)为原料制备 的工艺流程如下图:
的工艺流程如下图:_______ (写出一种)。
(2)“操作”在实验室的名称为_______ ,需用到的玻璃仪器是_______ 、玻璃棒和烧杯。
(3)黄铁矿焙烧后得到的主要固体为 ,写出“焙烧”的化学方程式为
,写出“焙烧”的化学方程式为_______ 。
(4)“……”表示的操作为在_______ 气流中蒸发浓缩、_______ 、过滤。
(5)为防治 引起的污染,某工厂设计了新的治污方法,同时可得到化工产品
引起的污染,某工厂设计了新的治污方法,同时可得到化工产品 。该工艺流程如图所示,过程中起催化作用的物质是
。该工艺流程如图所示,过程中起催化作用的物质是_______ ,生成化工产品 的化学方程式为
的化学方程式为_______ 。 生产硫酸。用
生产硫酸。用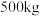 含
含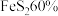 的硫铁矿,生产过程中硫损失
的硫铁矿,生产过程中硫损失 ,则可得
,则可得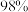 的硫酸
的硫酸_______  。
。
 在工业上有广泛的用途。以硫铁矿(主要成分为
在工业上有广泛的用途。以硫铁矿(主要成分为 )为原料制备
)为原料制备 的工艺流程如下图:
的工艺流程如下图: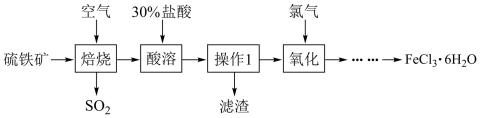
(2)“操作”在实验室的名称为
(3)黄铁矿焙烧后得到的主要固体为
 ,写出“焙烧”的化学方程式为
,写出“焙烧”的化学方程式为(4)“……”表示的操作为在
(5)为防治
 引起的污染,某工厂设计了新的治污方法,同时可得到化工产品
引起的污染,某工厂设计了新的治污方法,同时可得到化工产品 。该工艺流程如图所示,过程中起催化作用的物质是
。该工艺流程如图所示,过程中起催化作用的物质是 的化学方程式为
的化学方程式为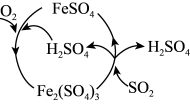
 生产硫酸。用
生产硫酸。用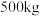 含
含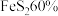 的硫铁矿,生产过程中硫损失
的硫铁矿,生产过程中硫损失 ,则可得
,则可得 的硫酸
的硫酸 。
。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】亚硫酰氯(SOCl2)又名氯化亚砜,是一种无色或淡黄色发烟液体,有强烈刺激性气味,其熔点-105℃,沸点79℃,140℃以上时易分解。遇水剧烈反应生成SO2和另一种酸性气体,常用作脱水剂,主要用于制造酰基氯化物,还用于医药、农药、染料等的生产。
实验室合成SOCl2的原理之一为SO2+Cl2+SCl2 2SOCl2,部分装置(夹持、加热装置略去)如图所示。
2SOCl2,部分装置(夹持、加热装置略去)如图所示。
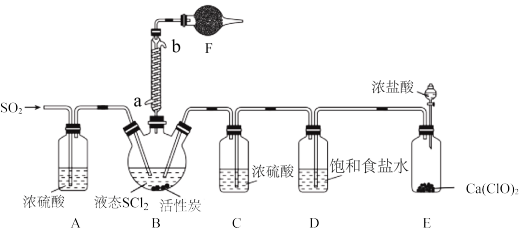
(1)①仪器F的名称为_______ ,所盛的试剂是______ ;
②装置A、C除干燥气体外,另一作用可能是__________________________________ ;
如果没有A、C,二氧化硫与氯气在装置B中会有副反应发生,该反应的离子方程式为_________
③E中反应的化学方程式:_______________________________ 。
(2)甲同学认为SOCl2和FeCl3∙6H2O混合加热可制得无水FeCl3,但乙同学认为该实验可能发生副反应使产品不纯。乙同学设计如下实验判断副反应的可能性:取少量FeCl3∙6H2O于试管中,加入足量SOCl2,充分反应后向试管中加水溶解,用四支试管各取溶解后的溶液少许,分别进行下列实验,通过现象能验证发生副反应的是_______ (填选项字母)。
a.滴加BaCl2溶液 b.滴加K3[Fe(CN)6]溶液
c.滴加酸性KMnO4溶液 d.滴加溴水
(3)分离产物后,向获得的SOCl2中加入足量NaOH溶液,振荡、静置得到无色溶液,检验该溶液中存在Cl-的需要用到的试剂是_______________________
实验室合成SOCl2的原理之一为SO2+Cl2+SCl2
 2SOCl2,部分装置(夹持、加热装置略去)如图所示。
2SOCl2,部分装置(夹持、加热装置略去)如图所示。
(1)①仪器F的名称为
②装置A、C除干燥气体外,另一作用可能是
如果没有A、C,二氧化硫与氯气在装置B中会有副反应发生,该反应的离子方程式为
③E中反应的化学方程式:
(2)甲同学认为SOCl2和FeCl3∙6H2O混合加热可制得无水FeCl3,但乙同学认为该实验可能发生副反应使产品不纯。乙同学设计如下实验判断副反应的可能性:取少量FeCl3∙6H2O于试管中,加入足量SOCl2,充分反应后向试管中加水溶解,用四支试管各取溶解后的溶液少许,分别进行下列实验,通过现象能验证发生副反应的是
a.滴加BaCl2溶液 b.滴加K3[Fe(CN)6]溶液
c.滴加酸性KMnO4溶液 d.滴加溴水
(3)分离产物后,向获得的SOCl2中加入足量NaOH溶液,振荡、静置得到无色溶液,检验该溶液中存在Cl-的需要用到的试剂是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
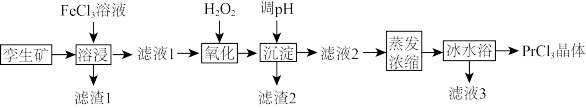
【推荐3】一种矿物的孪生矿含有Pr2S3、FeS、SiO2等,利用该矿制取PrCl3晶体的工艺流程如下:
已知:PrCl3(aq)+2Cl-(aq)
 (aq) ΔH>0.
(aq) ΔH>0.
(1)实验室用氯化铁固体配制氯化铁溶液的具体操作为_______ 。
(2)“溶浸”时Pr2S3可被FeCl3氧化,生成淡黄色的沉淀。写出Pr2S3被FeCl3氧化的离子方程式:_______ ;由于溶液酸性较强,该操作中易产生有毒气体,其化学式为_______ ,工业上可用_______ (填化学式)来吸收处理。
(3)"滤渣1”的主要成分有_______ (填化学式)。
(4)“调pH”时,可选用的试剂为_______ (填标号)。
(5)用化学平衡移动的原理解释使用冰水浴的原因:_______ 。

已知:PrCl3(aq)+2Cl-(aq)

 (aq) ΔH>0.
(aq) ΔH>0.(1)实验室用氯化铁固体配制氯化铁溶液的具体操作为
(2)“溶浸”时Pr2S3可被FeCl3氧化,生成淡黄色的沉淀。写出Pr2S3被FeCl3氧化的离子方程式:
(3)"滤渣1”的主要成分有
(4)“调pH”时,可选用的试剂为_______ (填标号)。
| A.Fe2O3 | B.稀盐酸 | C.Fe(OH)3 | D.稀硫酸 |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】pC类似pH,是指溶液中溶质物质的量浓度的常用对数的负值,如某溶液的浓度为1×10-2mol/L,则溶液中该溶质的pC=-lg1×10-2=2已知H2RO3溶液中存在的化学平衡为:RO2(g)+H2O  H2RO3
H2RO3  H+ +HRO3-,HRO3-
H+ +HRO3-,HRO3- H++RO32-下图为H2RO3饱和溶液的pC-pH图。请回答下列问题:
H++RO32-下图为H2RO3饱和溶液的pC-pH图。请回答下列问题:

(1)在pH=2~4时,H2RO3溶液中主要存在的离子为:_____ ;
(2)H2RO3一级电离平衡常数的数值Ka1≈_______ ;
(3)已知:298K时,H2RO3的电离常数Ka2=5.6×10-11。观察上图判断NaHRO3溶液呈_______ 性;再通过计算,利用电离、水解平衡常数说明理由____________ 。
(4)一定浓度的NaHRO3和Na2RO3混合溶液是一种“缓冲溶液”,在这种溶液中加入少量的强酸或强碱,溶液的pH变化不大,其原因是_________ 。
(5)一定温度下,三种盐MRO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解曲线如右图所示。已知:p(M2+)=-lg c(M2+),p(RO32-)= -lgc(RO32-)

①MgRO3、CaRO3、MnRO3的Ksp由大到小的顺序为_______________ 。
② a 点时c(Mg2+)_____ c(RO32-) (填“>”或“<”或“=”),此时MgRO3溶液_______ (填“已达饱和”或“未达饱和”)
③现欲将某溶液中的Mn2+以MnRO3盐的形式沉淀完全(溶液中Mn2+离子的浓度小于l×10-5mol/L),则最后溶液中的p(RO32-)的范围是_________________ 。
 H2RO3
H2RO3  H+ +HRO3-,HRO3-
H+ +HRO3-,HRO3- H++RO32-下图为H2RO3饱和溶液的pC-pH图。请回答下列问题:
H++RO32-下图为H2RO3饱和溶液的pC-pH图。请回答下列问题:
(1)在pH=2~4时,H2RO3溶液中主要存在的离子为:
(2)H2RO3一级电离平衡常数的数值Ka1≈
(3)已知:298K时,H2RO3的电离常数Ka2=5.6×10-11。观察上图判断NaHRO3溶液呈
(4)一定浓度的NaHRO3和Na2RO3混合溶液是一种“缓冲溶液”,在这种溶液中加入少量的强酸或强碱,溶液的pH变化不大,其原因是
(5)一定温度下,三种盐MRO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解曲线如右图所示。已知:p(M2+)=-lg c(M2+),p(RO32-)= -lgc(RO32-)

①MgRO3、CaRO3、MnRO3的Ksp由大到小的顺序为
② a 点时c(Mg2+)
③现欲将某溶液中的Mn2+以MnRO3盐的形式沉淀完全(溶液中Mn2+离子的浓度小于l×10-5mol/L),则最后溶液中的p(RO32-)的范围是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
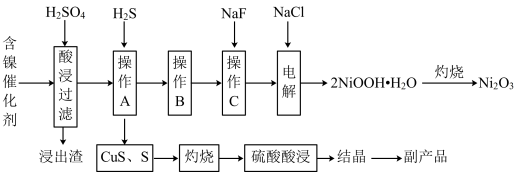
【推荐2】为回收利用废镍催化剂(主要成分为NiO,另含Fe2O3、CaO、CuO、BaO等),科研人员研制了一种回收镍的新工艺。工艺流程如图:
已知:①常温下,有关氢氧化物开始沉淀和沉淀完全的pH如表
②常温下,Ksp(CaF2)= 2.7×10-11
回答下列问题:
(1)加快酸浸速率的常用措施有_____________ (任写一条)。
(2)写出酸浸时Fe2O3和硫酸反应的离子方程式________________________________ 。
(3)浸出渣主要成分为CaSO4·2H2O和______________ 两种物质。
(4)操作B的过程是先在40~50℃加入H2O2,其作用是___________________________ (用离子方程式表示);再调节PH至3.7~7.7,操作B可除去溶液中的______ 元素(填元素名称)。
(5)操作C可除去溶液中的Ca2+,若控制溶液中F-浓度为3×10-3mol/L,则溶液中c(Ca2+):c(F-) =___________________ 。
(6)在碱性条件下,电解产生2NiOOH·H2O的原理分两步:
① Cl- 在阳极被氧化为ClO-,则阳极的电极反应为_____________________ 。
② Ni2+ 被ClO-氧化产生2NiOOH·H2O沉淀,则该步反应的离子方程式为______________ 。

已知:①常温下,有关氢氧化物开始沉淀和沉淀完全的pH如表
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
②常温下,Ksp(CaF2)= 2.7×10-11
回答下列问题:
(1)加快酸浸速率的常用措施有
(2)写出酸浸时Fe2O3和硫酸反应的离子方程式
(3)浸出渣主要成分为CaSO4·2H2O和
(4)操作B的过程是先在40~50℃加入H2O2,其作用是
(5)操作C可除去溶液中的Ca2+,若控制溶液中F-浓度为3×10-3mol/L,则溶液中c(Ca2+):c(F-) =
(6)在碱性条件下,电解产生2NiOOH·H2O的原理分两步:
① Cl- 在阳极被氧化为ClO-,则阳极的电极反应为
② Ni2+ 被ClO-氧化产生2NiOOH·H2O沉淀,则该步反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】Ⅰ.“一酸两浸,两碱联合”法是实现粉煤灰(含SiO2、Al2O3、Fe2O3、CaO、MgO等)综合利用的新工艺。聚合氯化铝铁(PAFC)化学式为:[Al2(OH)nCl6-n]m·[Fe2(OH)xCl6-x]y,是一种新型高效的净水剂。工业流程如下:

回答下列问题:
(1)实际工业中“酸浸”、“碱浸”均不能充分反应,滤渣A中主要含有SiO2、Al2O3。“纯碱混合焙烧”中,它们分别发生反应的化学方程式为_________________ 、_________________ 。
(2)滤液混合后“蒸发”的作用是________________________________ 。
(3)“电解”时阳极的电极反应式为________________ 。
(4)PAFC、无水AlCl3、FeCl3·6H2O用量均为25 mg·L-1时,处理不同pH污水的浊度去除率如图所示,PAFC的优点是___________________________ 。

Ⅱ.(5) 25℃时,用0.1mol/L的CH3COOH溶液滴定20mL0.1mol/L的NaOH溶液,当滴加VmLCH3COOH溶液时,混合溶液的pH=7。已知CH3COOH的电离平衡常数为Ka,忽略混合时溶液体积的变化,Ka的表达式为___________ 。
(6) 常温下,测得某纯CaSO3与水形成的浊液pH为9,已知Ka1(H2SO3)=1.8×10-2,Ka2(H2SO3)=6.0×10-9,忽略SO32-的第二步水解,则Ksp(CaSO3)=_________________ 。

回答下列问题:
(1)实际工业中“酸浸”、“碱浸”均不能充分反应,滤渣A中主要含有SiO2、Al2O3。“纯碱混合焙烧”中,它们分别发生反应的化学方程式为
(2)滤液混合后“蒸发”的作用是
(3)“电解”时阳极的电极反应式为
(4)PAFC、无水AlCl3、FeCl3·6H2O用量均为25 mg·L-1时,处理不同pH污水的浊度去除率如图所示,PAFC的优点是

Ⅱ.(5) 25℃时,用0.1mol/L的CH3COOH溶液滴定20mL0.1mol/L的NaOH溶液,当滴加VmLCH3COOH溶液时,混合溶液的pH=7。已知CH3COOH的电离平衡常数为Ka,忽略混合时溶液体积的变化,Ka的表达式为
(6) 常温下,测得某纯CaSO3与水形成的浊液pH为9,已知Ka1(H2SO3)=1.8×10-2,Ka2(H2SO3)=6.0×10-9,忽略SO32-的第二步水解,则Ksp(CaSO3)=
您最近一年使用:0次



