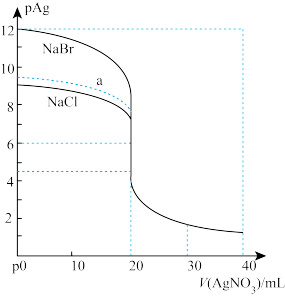
一定温度下,难溶电解质在水中存在沉淀溶解和生成的平衡,常用溶度积Ksp来表示溶解程度的大小,如Ksp(AgCl)=c(Ag+)·c(Cl—)。常温下用0.1000mol/L的AgNO3标准溶液(pH≈5)分别滴定20.00mL0.1000mol/L的NaCl溶液和NaBr溶液,混合溶液的pAg[定义为pAg=—lgc(Ag+)]与AgNO3溶液体积的变化关系如图所示。
下列说法不正确的是

下列说法不正确的是
| A.Ksp(AgCl)>Ksp(AgBr) |
| B.当V(AgNO3溶液)=20mL时,NaBr溶液中:c(Ag+)+c(H+)=c(Br—)+c(OH—) |
C.当V(AgNO3溶液)=30mL时,NaCl溶液中:c(NO )>c(Na+)>c(Ag+)>c(Cl—)>c(H+) )>c(Na+)>c(Ag+)>c(Cl—)>c(H+) |
| D.相同实验条件下,若改用10.00mL0.2000mol/LNaCl溶液,则滴定曲线(滴定终点前)可能变为a |
2021·浙江·三模 查看更多[6]
浙江省名校新高考研究联盟(Z20联盟)2021届高三第三次联考化学试题(已下线)【浙江新东方】高三化学20210527-004【2021】【高三下】【模拟考】【Z20】【高中化学】【李鼎收集】(已下线)第26讲 难溶电解质的溶解平衡(精练)-2022年高考化学一轮复习讲练测(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)专题12 水溶液中的离子平衡-备战2022年高考化学学霸纠错(全国通用)(已下线)考点29 沉淀溶解平衡-备战2023年高考化学一轮复习考点帮(全国通用)
更新时间:2021-06-02 22:02:54
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列液体均处于 ,有关叙述不正确的是
,有关叙述不正确的是
 ,有关叙述不正确的是
,有关叙述不正确的是A.向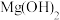 的悬浊液中加入少量的 的悬浊液中加入少量的 固体, 固体,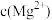 增大 增大 |
B.向 、 、 混合溶液中逐滴加入少量氨水,先生成 混合溶液中逐滴加入少量氨水,先生成 沉淀,说明 沉淀,说明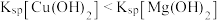 |
C. 在等物质的量浓度的 在等物质的量浓度的 和 和 溶液中的溶解度不相同 溶液中的溶解度不相同 |
D.将 与 与 饱和溶液等体积混合,再加入足量 饱和溶液等体积混合,再加入足量 溶液,生成的 溶液,生成的 少于 少于 |
您最近一年使用:0次
【推荐2】25℃,将0.1mol BaSO4粉末置于盛有500mL蒸馏水的烧杯中,然后烧杯中加入Na2CO3固体(忽视溶液体积的变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中正确的是
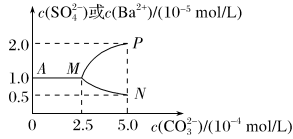

| A.25℃,Ksp(BaSO4)=1.5×10−9 |
| B.BaSO4在水中的溶解度、Ksp均比在BaCl2溶液中的大 |
C.反应BaSO4(s)+ (aq) (aq)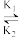 BaCO3(s)+ BaCO3(s)+ (aq)的K1=0.4 (aq)的K1=0.4 |
| D.若使0.1mol BaSO4全部转化为BaCO3,至少要加入2.6mol Na2CO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】根据下列实验操作和现象不能得到相应结论的是
| 选项 | 实验操作和现象 | 结论 |
| A | 乙醇钠的水溶液显强碱性 | C2H5O-结合H+的能力强 |
| B | 向KBrO3溶液中通入少量Cl2,然后再加入少量苯,有机层呈橙红色 | 氧化性:Cl2>Br2 |
| C | 向盛有KI3溶液的两支试管中,分别滴加淀粉溶液和AgNO3溶液,前者溶液变蓝,后者有黄色沉淀 | 溶液中存在平衡:  I2+I- I2+I- |
| D | 向等体积等浓度的稀硫酸中分别加入少许等物质的量的ZnS和CuS固体,ZnS溶解而CuS不溶解 | Ksp(CuS)<Ksp(ZnS) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验操作对应的现象与结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 常温下将Ba(OH)2·8H2O晶体与NH4Cl晶体在小烧杯中混合 | 烧杯壁变凉 | 该反应正向是熵增的反应 |
| B | 将充有NO2的密闭烧瓶放入热水中 | 烧瓶内气体颜色变深 | NO2生成N2O4的反应中,ΔH>0 |
| C | 将0.1mol/L的弱酸HA稀释成0.01mol/L,测量稀释前后溶液 pH | pH增大 | 稀释后HA电离程度减小 |
| D | 常温下向物质的量浓度均为0.1mol/L的NaCl和NaI混合溶液中逐滴滴入AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】探究卤族元素单质及其化合物的性质,下列方案设计、现象和结论都正确的是
| 实验方案 | 现象 | 结论 | |
| A | 向淀粉溶液中加适量稀硫酸,加热,冷却后滴加少量碘水 | 溶液变蓝 | 淀粉有剩余 |
| B | 用玻璃棒蘸取次氯酸钠溶液点在pH试纸上 | 试纸变白 | 次氯酸钠溶液呈中性 |
| C | 向2mL 0.1mol•L-1 AgNO3溶液中先滴加4滴0.1mol•L-1KCl溶液,再滴加4滴0.1mol•L-1KI溶液 | 先产生白色沉淀,再产生黄色沉淀 | AgCl转化为AgI,AgI溶解度小于AgCl溶解度 |
| D | 取两份新制氯水,分别滴加AgNO3溶液和淀粉KI溶液 | 前者有白色沉淀,后者溶液变蓝色 | 氯气与水的反应存在限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



